КРАСНОЯРСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ
АКАДЕМИЯ
На правах рукописи
Ланин Сергей Николаевич
НОВЫЙ МЕТОД ИНТЕРПРЕТАЦИИ РЕОГРАММ
ПРИ ПЕРВИЧНОЙ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМЕ
14.00.08 – Глазные болезни
Диссертация на соискание учёной степени
кандидата медицинских наук
Научный руководитель:
Заслуженный врач РФ,
доктор медицинских наук,
профессор Лазаренко В.И.
Научный консультант:
доктор медицинских наук,
профессор Россиев Д.А.
Красноярск – 2002
СОДЕРЖАНИЕ
ВВЕДЕНИЕ…………………………………………………………………………5
ГЛАВА I. Современное представление о методе исследования
кровообращения с помощью реографии и способах
обработки реограмм (Обзор литературы)……………….. ………10
I.1. Биофизические основы метода реографии…………………………………10
I.2. Способы оценки реограмм……………….………………………………….16
I.3. Применение вычислительной техники и преобразования Фурье
для обработки данных медицинских исследований………………...…….22
I.4. Искусственные нейронные сети в медицине………………………………27
ГЛАВА II. Материал и методы исследования……………………………….. 35
II.1. Характеристика объекта исследования……………………………………35
II.2. Методы исследования кровообращения глаза и мозга …………………..44
II.3. Математические методы исследования…………………………………...48
ГЛАВА III. Результаты собственных исследований…………………………61
III.1. Количественная оценка реограмм (РЭГ, РОГ) больных ПОУГ и
здоровых лиц……………………………………………………………….61
III.2.Результаты количественной обработки реоэнцефалограмм
с применением искусственных нейронных сетей..……………………..63
III.3. Результаты количественной обработки реоофтальмограмм
с применением искусственных нейронных сетей……………………....65
III.4. Результаты обработки реоэнцефалограмм с применением
дискретного преобразования Фурье и искусственных
нейронных сетей..…..……………………………………………………....68
III.5. Результаты обработки реоофтальмограмм с применением
искусственных нейронных сетей и дискретного преобразования
Фурье……………………………………………………………………….69
III.6. Сравнительная характеристика результатов обработки рео-
энцефало- и реоофтальмограмм с применением
количественного способа оценки…………………………..……………72
III.7. Сравнительная характеристика результатов обработки реоэнце-
фало - и реоофтальмограмм с применением дискретного преобра-
зования Фурье…………………………………………...…………………75
ГЛАВА IV. Обсуждение результатов исследования………………………….78
IV.1. Сравнительная характеристика количественного способа обработки и
Фурье-анализа реограмм с применением искусственных нейронных
сетей ………………………………………………………………………..78
IV.2. Диагностические возможности метода реографии при различных
способах обработки реограмм……………………………………………..84
ЗАКЛЮЧЕНИЕ…………………………………………………………………..96
ВЫВОДЫ…………………………………………………………………………103
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ………………………………………104
ЛИТЕРАТУРА…………………………………………………………………...105
СПИСОК СОКРАЩЕНИЙ
АД – артериальное давление
АРОК – автоматизированный реографический комплекс
АЦП – аналогово-цифровой преобразователь
БПФ – быстрое преобразование Фурье
ВГД – внутриглазное давление
ВГЖ – внутриглазная жидкость
ДПФ – дискретное преобразование Фурье
ИНС – искусственные нейронные сети
КГТУ – Красноярский Государственный Технический Университет
ККОКБ – Красноярская краевая офтальмологическая клиническая больница
КрасГМА – Красноярская Государственная Медицинская Академия
НВР – нейроваскулярная реакция
ПОУГ – первичная открытоугольная глаукома
РОГ – реоофтальмография
РЭГ – реоэнцефалография
УЗИ – ультразвуковое исследование
ФА – Фурье анализ
ЭВМ – электронно-вычислительная машина
ЭКГ – электрокардиография
ЭТГ – электротонография
ВВЕДЕНИЕ
АКТУАЛЬНОСТЬ ИССЛЕДОВАНИЯ
Существующие способы оценки реографических кривых, описательный и количественный, на протяжении многих лет остаются практически единственными в комплексной оценке реограмм. Результаты такой оценки служат лишь дополнительным инструментом в постановке диагноза.
Проводя анализ доступной нам литературы [33, 37, 42, 45, 46, 51, 55, 58, 60, 63, 67, 73, 78, 87, 88, 90, 92, 94, 95], мы не обнаружили иных способов обработки реографических кривых, кроме существующих, которые бы позволили повысить информативность методики.
Опыт применения реографии в клинической практике показал, что нет формы реограммы, а тем более коэффициентов, патогномоничных для какого-либо заболевания [78, 94, 95]. Присутствуют лишь симптомы, указывающие на изменение структуры и свойств сосудистой стенки, изменения интенсивности и уровня объёмного пульсового кровенаполнения, характерные для целого ряда патологических состояний.
Существует ряд признаков, отражаемых на реографической кривой, которые позволяют объяснить ту или иную степень изменения интенсивности и уровня суммарного кровенаполнения в исследуемой области: например – повышение тонуса сосудов характерно для гипертонической болезни; снижение эластичности сосудистой стенки - для атеросклероза и т.д. Но в большинстве случаев от исследователя скрыты истинные причины возникновения заболеваний, признаки которых видны на реограмме, что не позволяет поставить диагноз.
Хотя метод исследования кровообращения с помощью реографии несёт гораздо больше информации, скрытой в самой реограмме, она недоступна для обычных способов интерпретации. И не всегда понятно, за счёт каких механизмов происходит изменение гемодинамики в исследуемой области. Особенно, когда вопрос касается разницы между уровнем и интенсивностью кровообращения во внутренней сонной артерии и глазничной артерии, которая является её терминальной ветвью. Несмотря на наличие публикаций о влиянии церебрального кровотока на интраокулярный [32, 50, 81], этот вопрос недостаточно изучен.
Трудоёмкость математической обработки и необходимость проведения визуальной оценки реограмм квалифицированным врачом со специальной подготовкой, тем не менее, не избавляет комплексный анализ от определённого субъективизма, что в свою очередь, ведёт к возникновению ошибок в оценке уровня и интенсивности кровообращения, а по существу не отражает всех патологических изменений реографических кривых. В итоге это ведёт к неполному использованию информации, содержащейся в реограммах. Эти причины определили цель и задачи настоящей работы.
ЦЕЛЬ ИССЛЕДОВАНИЯ:
Разработка метода интерпретации реограмм с применением дискретного преобразования Фурье и нейронных сетей.
Для достижения этой цели были поставлены следующие задачи:
- Провести обработку реограмм (РЭГ, РОГ) с применением количественного способа оценки и искусственных нейронных сетей.
- Исследовать возможность интерпретации реограмм (РЭГ, РОГ) с помощью дискретного преобразования Фурье и искусственных нейронных сетей.
- Дать сравнительную характеристику Фурье-анализа реоэнцефалограмм и реоофтальмограмм.
- Провести сравнительный анализ между количественным способом обработки реограмм и методом дискретного преобразования Фурье с применением искусственных нейронных сетей.
- Показать диагностические возможности Фурье-анализа реограмм с применением нейронных сетей на примере больных первичной открытоугольной глаукомой.
НАУЧНАЯ НОВИЗНА ИССЛЕДОВАНИЯ
Впервые разработан метод оценки реографических кривых с применением дискретного преобразования Фурье и нейросетевых экспертных систем.
Впервые проведён сравнительный анализ между количественным способом обработки реограмм и методом дискретного преобразования Фурье с применением нейронных сетей.
Показана диагностическая значимость предлагаемого метода на примере реограмм больных первичной открытоугольной глаукомой, что может быть использовано в диагностике других глазных заболеваний.
ПРАКТИЧЕСКАЯ ЗНАЧИМОСТЬ РЕЗУЛЬТАТОВ ИССЛЕДОВАНИЯ
Внедрение в офтальмологическую практику предлагаемого способа Фурье-анализа реограмм больных первичной открытоугольной глаукомой позволяет повысить диагностическую значимость и точность исследования гемодинамики у них, тем самым, снижая вероятность возникновения ошибок, возможных при ранней диагностике заболевания.
Показана целесообразность исследования гемодинамики у лиц с подозрением на глаукому, что позволит сократить время обследования пациентов и начать функциональную терапию лицам с диагнозом «Первичная открытоугольная глаукома».
Предлагаемый метод оценки реограмм может быть использован для диагностики глазных заболеваний, как в стационаре, так и в поликлинике, где имеется возможность исследования кровообращения с помощью аппаратно-программного комплекса с применением компьютерной техники.
Основные положения работы используются на кафедре глазных болезней и глазных болезней ФПК и ППС КрасГМА, в глаукомном кабинете и отделении функциональной диагностики Красноярского межрегионального центра микрохирургии глаза имени П.Г. Макарова.
ОСНОВНЫЕ ПОЛОЖЕНИЯ, ВЫНОСИМЫЕ НА ЗАЩИТУ:
- Метод обработки реограмм с применением дискретного преобразования Фурье и искусственных нейронных сетей повышает диагностическую значимость метода реографии.
- Диагностическая ценность Фурье-анализа реоофтальмограмм при глаукоме выше, чем реоэнцефалограмм.
- Применение предлагаемого метода интерпретации реограмм обосновано при обследовании пациентов с подозрением на глаукому.
МАТЕРИАЛ И ОБЪЁМ ИССЛЕДОВАНИЯ
Клинические исследования, исследование церебральной и интраокулярной гемодинамики с изучением различных способов обработки реограмм, проведены у 67 больных первичной открытоугольной глаукомой в начальной стадии и у 59 человек, у которых данных за глаукому не выявлено. Записано и проанализировано с применением количественного способа обработки и дискретного преобразования Фурье с использованием искусственных нейронных сетей 216 реоэнцефалограмм и 170 реоофтальмограмм.
Статистическую обработку результатов проводили на персональном компьютере – “Celeron 566” с помощью программы “Statistics – 5,0 for Windows”, с использованием средней арифметической, средней ошибки, среднего квадратического отклонения, критерия различий Стьюдента, показателя достоверности (р). Различие считали достоверным при р < 0,05.
АПРОБАЦИЯ РАБОТЫ
Основные положения диссертации доложены и обсуждены на: заседаниях кафедры глазных болезней КрасГМА (1998-2002); VI Всероссийском семинаре «Нейроинформатика и её приложения», Красноярск (1998); I Всероссийском семинаре “Моделирование неравновесных систем”, Красноярск (1998); клинических конференциях офтальмологов Красноярского края (1999, 2001); VII съезде офтальмологов России, Москва (2000); VII международном конгрессе офтальмологов «Современные проблемы офтальмологии», София, Болгария (2000).
ПУБЛИКАЦИИ
По теме диссертации опубликовано 13 статей, методические рекомендации (1), рационализаторское предложение (1).
ГЛАВА I. СОВРЕМЕННОЕ ПРЕДСТАВЛЕНИЕ О МЕТОДЕ ИССЛЕДОВАНИЯ КРОВООБРАЩЕНИЯ С ПОМОЩЬЮ РЕОГРАФИИ И СПОСОБАХ ОБРАБОТКИ РЕОГРАММ (Обзор литературы)
I.1. Биофизические основы метода реографии
Метод исследования пульсовых колебаний кровенаполнения сосудов, различных органов и тканей, основанный на графической регистрации изменений полного электрического сопротивления живых тканей во время прохождения через них электрического тока, называется реография. С помощью реографии оценивается скорость движения крови в сосудах, их тонус, а также функциональное состояние резистивных и ёмкостных сосудов [12].
Развитие метода реографии связано с установлением зависимости между работой сердца и колебаниями сопротивления и ёмкости в тканях [84].
В 1935 году H.Mann впервые применил для измерения электропроводности переменный ток. Он обнаружил ритмические колебания электропроводности пальцев кисти, синхронные с пульсацией кровеносных сосудов, и предложил использовать это явление в качестве метода исследования периферического кровообращения в любой части тела. H.Mann выявил определённую корреляцию между формой регистрируемой кривой и объёмом циркулирующей крови.
Эти исследования заложили основу реографии и получили дальнейшее развитие в работах [45, 46, 47, 66].
Работы [40, 53, 60] в исследовании электропроводности, электрического сопротивления органов и частей тела, влияния на организм постоянного и переменного тока разной частоты, способствовали теоретическому обоснованию реографии.
Метод реоофтальмографии получил широкое распространение в практике, как позволяющий изучать гемодинамику глаза в условиях, близких к физиологическим и находит применение для оценки кровоснабжения глаза при глаукоме [44, 49, 50], близорукости [28, 51], острой сосудистой патологии [3, 89], отслойке сетчатки [62, 76], дистрофических заболеваниях [13, 14, 51, 80], травмах [2], системных заболеваниях организма [16, 43, 68, 85, 87].
При изучении гемодинамики глаза реографические показатели признаны высокоинформативными [42].
Многими авторами признается большая роль нарушений эластотонических свойств сосудов при различной офтальмопатологии (глаукома, диабетическая ретинопатия, макулодистрофия и т.д.).
С физической точки зрения живая ткань является проводником электрического тока. Её электрические свойства обусловлены содержанием в ней электролитов, белков и зависят от поляризационных свойств тканей [55].
Полное комплексное электрическое сопротивление живой ткани (импеданс) при пропускании через нее электрического тока слагается из 2-х основных компонентов:
- активного омического сопротивления, обусловленного электролитным составом тканей и наличием высокомолекулярных комплексов (ионной проводимостью)
- реактивным (емкостным, поляризующим) сопротивлением, обусловленным явлениями поляризации - образованием в момент прохождения тока (вследствие наличия электролитов) двойных электронных слоев на границах различных тканевых структур и клеточных мембран, что придает тканям диэлектрические свойства (явление поляризации).
Это явление создает дополнительное сопротивление постоянному электрическому току и уменьшает электропроводность тканей (Г.А. Красина, 1980) (цит. по В.И. Лазаренко) [55].
Зависимость импеданса (общего сопротивления) от его компонент выражается формулой: ![]()
![]() , где Z - импеданс, R - резистивное сопротивление, X - емкостное сопротивление.
, где Z - импеданс, R - резистивное сопротивление, X - емкостное сопротивление.
A. Spiegel et al. (1945) выявили различия проводимости клеток при высоких и низких частотах переменного тока (цит. по Б.И. Мажбич) [57].
Увеличение частоты переменного тока приводит к снижению емкостной составляющей, т.е. уменьшаются явления поляризации, мешающие реографическим исследованиям. Это позволяет выделить из общего электрического сопротивления очень малую переменную часть импеданса тканей, обусловленную колебаниями кровенаполнения [94].
Таким образом, увеличивая частоту переменного тока, можно уменьшить влияние емкостного сопротивления. Для реографии целесообразно использовать ток высокой частоты от 20 кГц до 200 кГц. В этом диапазоне наблюдаются максимальные величины изменений электрических параметров исследуемой области тела, связанные с гемодинамическими сдвигами [66].
Преимуществом высоких частот перед низкими является и то, что наиболее равномерное распределение тока в тканях происходит в данном диапазоне [137]. В результате величина импеданса будет определяться только омическим сопротивлением, зависящим от ионной проводимости.
Активное омическое сопротивление состоит из постоянной, обусловленной общим кровенаполнением, и переменной составляющей, вызванной кровенаполнением во время сердечного цикла. При увеличении кровенаполнения, т.е. в момент систолы, электрическое сопротивление падает (электропроводность увеличивается), а при уменьшении кровенаполнения, т.е. в момент диастолы, возрастает (электропроводность падает). Эти колебания обусловлены тем, что кровь обладает более высокой электропроводностью, чем остальные ткани, т.к. представляет собой раствор электролитов.
Регистрация переменной величины активного сопротивления представляет особый интерес, т.к. она дает косвенные представления об объемных изменениях сосудов в течение сердечного цикла и позволяет судить о кровоснабжении исследуемого участка тела.
Переменные токи высокой и малой силы не являются патологическими раздражителями и пропускание их через живые ткани не вызывает какой-либо реакции и абсолютно безвредно.
Выделенная переменная компонента омической составляющей, усиление и графическая регистрация ее составляет техническую основу метода реографии.
Реоэнцефалография (РЭГ) считается одним из признанных методов исследования гемодинамики головного мозга и широко применяется в клинической практике [17, 33, 34, 36, 42].
РЭГ позволяет в физиологических условиях получить количественные и качественные показатели, дополняющие клинические данные при оценке функционального состояния системы кровообращения как в целом, так и в отдельных его звеньях. Метод даёт достаточно полное представление о величине кровотока в изучаемом участке сосудистого русла и свидетельствует о состоянии сосудистой стенки (тонусе, напряжении и эластичности) [17, 42, 91].
И.В. Запускалов (1994) считает, что РЭГ достаточно информативна как при функциональных нарушениях мозгового кровообращения, так и при органических поражениях сосудов головного мозга. РЭГ с фронтомастоидальным наложением электродов отражает суммарное состояние экстракраниальных и интракраниальных сосудов преимущественно в бассейне внутренних сонных артерий [35].
Реоофтальмография - объективный метод исследования интенсивности внутриглазного кровотока [42, 87, 96, 105]. Принципиальных различий в способах регистрации реоофтальмограммы не существует (рис. 1).
По мнению Л.А. Кацнельсона (1977), И.К. Чиберене (1975), Ersler (1965), реоофтальмограмма в основном отражает кровенаполнение увеального тракта [42, 87, 114].
Реоофтальмография (РОГ) позволяет оценить приток и отток крови из структур глаза, получить представление о тонусе и эластичности внутриглазных сосудов и получить количественные данные о состоянии кровообращения глаза в норме и при патологических состояниях [33, 34, 68].
РОГ является достаточно объективным и информативным методом изучения кровотока глаза и, следовательно, вполне может быть использована при изучении регионарной интраокулярной гемодинамики и состояния сосудов глаза [35].
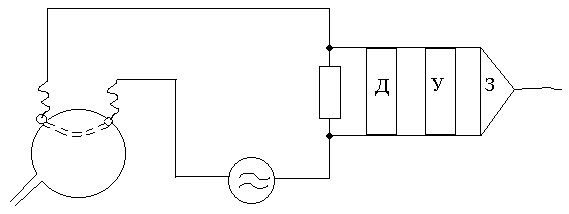
Рис. 1. Регистрация реоофтальмограммы.
Д – детектор
У – усилитель
З – записывающее устройство
Было показано, что кровообращение глаза непосредственно связано с церебральной гемодинамикой [32, 50, 81].
При проведении реоэнцефалографических и ультразвуковых исследований гемодинамики у больных глаукомой был обнаружен параллелизм между выраженностью атеросклеротических изменений сосудов головного мозга и тяжестью глаукомы [43].
Было установлено, что при снижении интенсивности мозгового кровообращения, экскавация диска зрительного нерва отличается значительной глубиной и площадью [44].
Определением интенсивности кровотока в мозговых сосудах методом радиоциркулографии у больных глаукомой выявлено замедление его скорости на стороне больного глаза, особенно в развитой и далекозашедшей стадии заболевания [85].
Также было установлено выраженное влияние состояния церебральной гемодинамики на кровоснабжение глаз больных глаукомой с гипертоническим типом и гипоперфузионным вариантом гипотонического типа нейро-васкулярной реакции. При нормотоническом и гипотоническом типах нейро-васкулярной реакции это влияние не обнаружено [50].
И.Г. Завгородняя, Л.Г. Кашинцева (1999) изучали патологию мозгового кровообращения у больных первичной открытоугольной глаукомой и её роль в развитии патогенетических механизмов заболевания [32].
Е.В. Сидоренко (1999) установила, что цереброваскулярная патология является причиной прогрессирования первичной открытоугольной глаукомы после успешных антиглаукоматозных операций [81].
Метод реоофтальмографии является одним из наиболее информативных методов исследования уровня объёмного пульсового кровенаполнения в бассейне глазничных артерий у больных открытоугольной глаукомой [42]. Однако, существующие методы интерпретации реограмм не позволяют при этом выявить характерные для первичной открытоугольной глаукомы признаки.
I.2. Способы оценки реограмм
До настоящего времени существовало всего лишь два способа оценки реографических кривых. Это описательный или качественный и математический или количественный способ.
Описательный метод основывается на оценке формы кривой. Если в реоэнцефалографических исследованиях форме кривой придаётся большое значение и уже по одной форме реоволны можно сделать заключение о состоянии сосудистой системы, то при реоофтальмографии по форме кривой вряд ли можно определить характер исследуемого процесса. Это связано прежде всего с тем, что на реоофтальмографической кривой, как правило, отсутствует дикротический зубец [41] выраженность или местоположение которого характеризуют различные состояния кровоснабжения мозга и периферических сосудов (рис. 2).
Визуальный анализ позволяет довольно быстро оценить состояние гемодинамики, качество записи, выбрать наиболее типичные участки реограммы для последующей математической обработки, но при всём этом несёт в себе определённые черты субъективизма.
При этом виде анализа выделяют крайние точки реоволны: начало и окончание волны, угол наклона восходящей части волны (анакроты), форму вершины, выраженность и расположение инцизуры и дикротического зубца на нисходящей части волны (катакроте), оценивают максимальную амплитуду волны по сравнению со стандартным калибровочным сигналом.
Проводя визуальный анализ реоэнцефалограмм, можно получить информацию о состоянии тонуса мозговых сосудов, об относительной величине пульсового кровенаполнения, о состоянии внутричерепного давления, изменениях венозного тонуса и о влиянии на них функциональных нагрузочных и медикаментозных проб.
2
РЭГ
4
3
6 7
1 5
2
РОГ
6 7
1 5
1. начало волны
2. вершина волны
3. инцизура
4. дикротический зубец
5. окончание волны
6. амплитуда волны
7. калибровочный сигнал
Рис. 2. Реокривые, калибровочный сигнал.
Таким образом, визуальный анализ позволяет оперативно получить сведения о состоянии сосудов и характере кровообращения в исследуемой области, но вместе с тем этот способ субъективен и требует квалификации и практичес- кого опыта врача. Поэтому, важное место занимает анализ расчётных показателей реограммы.
Математическая обработка реографических данных позволяет не только объективизировать информацию, полученную при визуальном анализе, но и получить дополнительные сведения о состоянии гемодинамики, например – характеристику периферического сосудистого сопротивления, тонуса сосудов; документально подтвердить динамику гемодинамических процессов при проведении функциональных и фармакологических проб; целенаправленно осуществлять подбор вазоактивных препаратов; контролировать эффективность проводимого лечения.
Начальной точкой отсчёта всех рассчитываемых параметров является кардиоимпульс. При расчёте также используются данные первой производной (дифференциальной) реограммы (рис. 3).
Количество и вид показателей, расчёт которых производится математическим путём, зависит от цели исследования [38, 71, 78].
Н.М. Юргевичене изучала хориоидальную микроциркуляцию с использованием девяти реогрфических показателей [92].
Хотя имеется немало публикаций, авторы которых используют только один показатель реоофтальмографии – реографический коэффициент, в качестве одного из методов оценки гемодинамики хориоидеи у больных сахарным диабетом при проведении хирургических вмешательств [30, 48, 59], лазеркоагуляции сетчатки [8, 61, 74, 79, 82], применении лекарственных препаратов [4, 27, 65, 77], считая реоофтальмографию адекватным методом изучения гемодинамики.
Реографический коэффициент (![]() ) по Yantch, рассчитывается по формуле:
) по Yantch, рассчитывается по формуле:
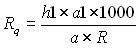 ‰, где: h1 – амплитуда реоволны, мм; а1 – калибровоч-
‰, где: h1 – амплитуда реоволны, мм; а1 – калибровоч-
ный импульс, Ом; а – калибровочный импульс, мм; R – сопротивление между электродами, Ом.
A
A1 Д Реограмма
B
И
X К
T4
ta1
Первая производная
к1
tx t td
ta tb
ЭКГ
Ts
Рис. 3. Реограмма, первая производная, кардиосигнал.
Для обработки реоофтальмограмм на полуавтоматизированном реографическом комплексе И.М. Корниловский, В.И. Лазаренко, Е.Н. Комаровских (1975 – 1991) применяли следующие показатели:
- пульсовой объём глаза;
- объёмный кровоток;
- реографический индекс;
- реографический коэффициент;
- показатель эластичности сосудов.
Для повышения точности и достоверности исследования гемодинамики глаз, а также для ускорения процесса обработки реографических кривых, в 1993 году был впервые разработан и применён на практике автоматизированный реографический комплекс – АРОК (Панкеев В.С., Ильенков С.С., Полынцев Л.А. и др., 1993; Панкеев В.С., Ильенков С.С., Дробова Н.Ю. и др., 1994; Лазаренко В.И., Комаровских Е.Н., Ильенков С.С. и др., 1996) [70]. В результате появилась возможность расчёта до 10 показателей:
- реографический индекс;
- реографический коэффициент;
- дикротический коэффициент;
- диастолический коэффициент;
- период быстрого наполнения;
- период максимального наполнения;
- показатель замедления кровенаполнения;
- время запаздывания реоволны;
- максимальная скорость наполнения;
- показатель модуля упругости.
Эти показатели использовали в своих работах Г.Ф. Алексеева, Л.Л. Алексеева, И.В. Давыдова, С.С. Ильенков, Л.А. Полынцев, Л.А. Черных [2, 3, 26, 38, 71, 86].
С 1998 года в Красноярском межрегиональном центре микрохирургии глаза проводится исследование гемодинамики головного мозга и глаза на аппаратно-программном реографическом комплексе «Мицар-Рео-201» производства ООО «Мицар» (Санкт-Петербург).
Существует возможность расчёта до 40 коэффициентов [56, 58, 63, 67, 90, 95].
Полученные коэффициенты сравниваются с нормативными значениями и делается заключение о характере гемодинамических процессов в исследуемой области.
Однако, даже комплексная оценка реографической кривой с применением этих методов обработки не позволяет поставить диагноз заболевания, так как не существует формы реографической кривой, а тем более коэффициентов, патогномоничных для какого-либо заболевания.
I.3. Применение вычислительной техники и преобразования Фурье в обработке данных медицинских исследований
В биомедицинских исследованиях часто имеют дело с сигналами, изменяющимися во времени. Подобные сигналы можно представить в виде зависимости амплитуды от времени. Такое представление называют функцией во временной области. Сигнал также можно представить в виде зависимости амплитуды от частоты. Тогда это называют функцией в частотной области, или спектральным представлением. Для любой функции во временной области можно найти соответствующую единственную функцию в частотной области.
В естественных условиях преобразование Фурье имеет место в зрительной системе человека: «На первый взгляд разбиение изображения на его компоненты Фурье может показаться операцией, которая, будучи математически оправданной, всё же не слишком приспособлена для представления информации содержащейся в изображении. Однако некоторые удивительные результаты, полученные при исследовании сенсорного восприятия, свидетельствуют о том, что это не так. Оказалось, что зрительная система млекопитающих, человека и животных осуществляет гармоничный анализ образа, используемый для упорядочения воспринимаемого внешнего мира. Ещё в 1966 году английский нейрофизиолог Кэмпбелл доказал, что зрительная система работает как многоканальный Фурье-фильтр, в котором каждый канал настроен на выделение решётки с определённой пространственной частотой» [69].
«Если проходить микроэлектродом по столбу нейронов, то выявляются рецептивные поля, настроенные на разные пространственные частоты. Поля столба проецируются на один участок зрительного поля. На этот же участок направлены рецептивные поля соседних столбов с другой ориентацией. В целом такая группа столбов представляет собой конструкцию, осуществляющей двумерное Фурье-разложение изображения. Возбуждения выходных нейронов сложных полей соответствуют значениям Фурье-коэффициентов. Согласно такому представлению происходит переход от поточечного описания изображения в сетчатке и наружном коленчатом теле к распределённому описанию квазиголографического типа в зрительной коре. О голографическом описании можно говорить потому, что распределение возбуждений в объёме коры соответствует не распределению освещённости на рецепторах сетчатки, а набору коэффициентов базисных функций. Мы рассмотрели работу одного участка зрительной коры, составленного несколькими столбами и обслуживающего кусок зрительного поля. Всё зрительное поле покрыто такими участками, и кора, таким образом, осуществляет кусочное Фурье-преобразование изображения – локальный спектральный анализ» [11].
A.P. Ginsburg, J.V. Carl рассматривали модель зрительного восприятия человека, согласно которой преобразование изображения на пути от сетчатки к зрительной коре мозга человека представляется как двумерное преобразование Фурье или Уолша [122].
При обсуждении вопросов обработки медицинских графических данных с помощью ЭВМ, ещё в 1979 году отмечена целесообразность применения спектральных компонентов преобразования Фурье при обработке флюорограмм грудной клетки и рентгенограмм сосудов головного мозга [93].
Н.Ахмед и К.Р. Рао описали эксперимент, проведённый с целью создания системы автоматического распознавания патологических кардиограмм и кардиограмм, принадлежащих здоровым людям. Они использовали дисперсионный критерий отбора признаков [7].
В 1983 году было высказано предположение о том, что данные, получаемые при спектральном анализе пульса человека, отражают не только работу сердца, но и состояние всего организма: нервной системы, мышц, стенок кровеносных сосудов, крови и других систем [132].
Е.А. Андреева, О.Е. Хуторская использовали быстрое преобразование Фурье (БПФ) при спектральном анализе электромиограмм, проведённом с целью изучения процессов управления мышцами в норме и патологии [6].
В. Каппелини, А. Дж. Константинидис, П. Эмилиани использовали цифровую фильтрацию и быстрое преобразование Фурье при обработке биомедицинских сигналов и биомедицинских изображений, а также осуществляемой с помощью ЭВМ – томографии [39].
Применение программ с цифровой фильтрацией для автоматической обработки электрокардиограмм, электромиограмм и электроэнцефалограмм применяли S. Cerutti, E. Gatti [108].
П.Т. Жиго при анализе клинического материала исходов ранений сердца и перикарда использовал современные математические методы максимального правдоподобия для дискретных и непрерывных признаков. Целью было выявление основных прогностических предикторов с их балльной оценкой тяжести для составления атласа номографических карт, позволяющих выявить зоны благоприятных и неблагоприятных исходов [31].
Ю.Л. Гоголицин, С.Г. Данько, Ю.Л. Каминский разработали на основе применения дискретного преобразования Фурье метод изучения искусственно вызываемых изменений биоэлектрических процессов в мозге человека [19].
Анализу изменений частоты разрядов нейронов мозга человека при выполнении психологических проб посвящены работы Ю.Л. Гоголицина, С.В. Пахомова [20].
В работе M. Juhola, V. Jantti с соавт. предложено использовать нерекурсивный адаптивный цифровой фильтр для изучения с помощью ЭВМ прерывистых (саккадических) движений глаза, которые, как указывается, дают важную информацию о строении нейронной системы. Оценке Фурье-критерия сходства изображений и методам регистрации движений глаз посвящены работы Ю.В. Алексеева с соавт., Ю.К. Аллика, Н.П. Березина, В.П. Смирнова [1, 5, 83, 129].
Исследованием информативности показателей гемодинамики глаза в постановке диагноза глаукомы и глазной гипертензии с применением метода линейных дискриминантных функций и пакета прикладных программ МЕДСТАТ-Д занимались С.Н. Басинский c соавт.. В результате обработки данных на ЭВМ была выявлена информативность каждого из 17 исследуемых показателей гемодинамики [9].
Н.А. Листопадовой в 1985 году было исследовано состояние зрительного нерва при глаукоме, норме и гипертензии глаза. Собранная информация о состоянии диска зрительного нерва была закодирована и обработана на ЭВМ с использованием как обычных статистических методов, так и метода линейных дискриминантных функций с помощью пакета прикладных программ для автоматизации статистической обработки медицинских измерений и медицинской диагностики «МЕДСТАТ-Д».
Этим же методом С.Н. Басинский исследовал информативность показателей офтальмосфигмографии в оценке гемодинамики глаз здоровых лиц, пациентов с глазной гипертензией и больных глаукомой. Был определён минимальный набор параметров куда вошли четыре наиболее информативных признака: анакрота, отношение А/К, угол спада волны глазного пульса и систолический прирост пульсового объёма крови. Предлагаемый нобор параметров позволял теоретически правильно классифицировать исследуемые офтальмо-сфигмограммы в 76% случаев. Эти признаки использовались для оценки гемодинамики глаза и в дифференциальной диагностике глазной гипертензии и глаукомы [9].
Таким образом, несмотря на широкое применение реографии для исследования гемодинамики, далеко не вся информация, содержащаяся в реографических кривых, была полностью использована. Это было связано с отсутствием в широкой клинической практике компьютерных методов регистрации и обработки реографических кривых. С появлением относительно недорогой вычислительной техники и разработке методов анализа периодических колебаний с помощью Фурье-преобразования появилась возможность более широко использовать данные, содержащиеся в реограммах. В доступной нам литературе не было найдено ни одного источника по применению дискретного преобразования Фурье для обработки реоофтальмограмм.
Поэтому, нами была предпринята попытка с помощью дискретного преобразования Фурье и нейросетевых экспертных систем объективизировать результаты реографических исследований для расширения диагностических возможностей метода реографии.
I.4. Искусственные нейронные сети в медицине
Область работ, связанная с созданием способов по переработке информации на основе принципов функционирования естественных нейронных систем, относится к области нейроинформатики или нейровычислений. Традиционной областью применения нейропроцессоров остаются задачи распознавания изображений, речи, радарных сигналов [29].
Основой работы самообучающихся нейропрограмм являются нейросети, представляющие собой совокупность нейронов, связанных между собой определённым образом (рис. 4).
Рис. 4. Сеть с 6 нейронами.
Нейроны и нейронные связи могут задаваться программно на обычном компьютере или быть реализованы в виде микросхемы и применяться в специально созданных нейрокомпьютерах.
Нейрон состоит из двух функциональных блоков: входного сумматора и собственно нейрона или преобразователя (рис. 5).
Структура взаимосвязей между нейронами аналогична таковой в биологических объектах. Искусственный нейрон имеет связи с другими нейронами через синапсы, передающие сигналы к нему – дендриты или от него - аксоны. Несколько нейронов, связанных между собой с помощью синапсов, образуют нейронную сеть.
Рис. 5. Структура нейрона.
Искусственная нейросеть, также как и биологический аналог, должна иметь каналы для связи с внешним миром. Поэтому, одни нейроны сети рассматриваются как входные, другие как выходные.
Через входные синапсы на нейрон подаются сигналы от других нейронов или из внешнего мира, представляющие собой либо набор чисел (вектор), либо одно число. Каждый синапс имеет параметр, называемый весом синапса, также представляющий собой какое-либо число. Сигнал, проходящий через синапс, умножается на его вес и в зависимости от веса может быть усилен либо ослаблен. Сигналы от всех синапсов, ведущих к данному нейрону, принимает сумматор, который суммирует все пришедшие сигналы и подаёт на нейрон полученную сумму. Таким образом, это число зависит как от величин исходных сигналов, так и от веса синапсов [24, 25, 75].
Нейрон, получивший это число, преобразует его согласно своей функции и отправляет по аксону другим нейронам. Последующие нейроны производят с полученными сигналами такие же операции, с тем отличием, что веса их синапсов могут быть уже другими, а они могут иметь другой вид функции преобразования. Чаще всего это одна и та же функция. Мы применяли характеристическую функцию (f) вида: ![]() где: X – сигнал, поступающий с сумматора; С – константа, называемая характеристикой нейрона. Оптимальный диапазон характеристики для решения большинства задач составляет 0,1-0,8 [75]. График характеристической функции представлен на рисунке 6.
где: X – сигнал, поступающий с сумматора; С – константа, называемая характеристикой нейрона. Оптимальный диапазон характеристики для решения большинства задач составляет 0,1-0,8 [75]. График характеристической функции представлен на рисунке 6.
1,0
0,8
0,6
0,4
0,2
-0,2
-1 -0,5 -0,4 0,5 1
-0,6
-0,8
-1,0
Рис. 6. График характеристической функции.
В конечном итоге нейросеть, получившая на входе какой - либо сигнал, способна после прохода его по нейронам выдавать на выходе определённый ответ, который зависит от весовых коэффициентов всех нейронов и от самого сигнала.
Чтобы добиться выдачи сетью нужного результата, необходимо её обучить путём настраивания весовых коэффициентов нейронов на конечное выходное число. Этот процесс происходит автоматически. Для обучения нейросети необходима обучающая выборка, состоящая из примеров. Каждый пример представляет собой задачу одного и того же типа с определённым набором входных параметров и заранее известным ответом. В качестве входных параметров могут использоваться данные обследования пациента, тогда заранее известным ответом в этом примере будет диагноз.
Для обучения нейросети необходимо наличие примеров, относящихся к разным классам, т.е. имеющих разные диагнозы. Несколько примеров с разными ответами образуют задачник. Задачник находится в базе данных, каждая запись которой является примером. После успешного обучения нейросеть должна правильно распознавать примеры с неизвестными ответами, т.е. условно говоря, поставить диагноз [75].
При создании нейроэкспертных программ сразу бывает сложно собрать достаточное количество данных для хорошего обучения нейросети. Поэтому, создавая нейросистему, исследователи определяют наилучшие параметры нейросетей и проводят начальное обучение. В последующем происходит доучивание системы в условиях реальной работы и реальных данных.
Система никогда не создаётся сразу готовой и никогда не является полностью законченной, продолжая накапливать опыт в процессе работы.
Тестирование примеров нейросетью может иметь две цели:
- проверка того, как обучилась нейросеть;
- решение конкретных задач.
Первая цель - тестирование выборки с заранее известными ответами примеров, т.е. можно проверить, правильно ли сеть определяет классы всех примеров и насколько уверенно она это делает. Определенный сетью класс примера сравнивается с заранее известным. Сначала тестирование проводят по выборке, на которой обучалась сеть. Если она обучилась полностью, то при тестировании этой обучающей выборки классы всех примеров будут определяться правильно. Но больший интерес представляет тестирование выборки с заранее известными ответами, примеры которой не участвовали в обучении сети.
Для практического здравоохранения наиболее интересными представляются нейросетевые системы, решающие задачи диагностики, прогнозирования и коррекции лечения. В качестве исходных данных могут использоваться результаты функциональной, лабораторной, лучевой диагностики, данные анамнеза, физикального осмотра, жалобы пациента, а также субъективные категории, например в психиатрии.
Наиболее широко идёт развитие направлений по применению нейросетей в кардиологии.
Проводятся комплексные исследования по диагностике инфаркта миокарда [102], прогнозированию его осложнений и исходов [22, 139]. Это связано с наличием возможностей для предупреждения и лечения целого ряда осложнений в случае своевременного их прогнозирования [128, 131].
Прогнозирование необходимо при определении больных в группы высокого и низкого риска, что позволяет оптимизировать лечебно-диагностическую тактику при формировании групп реабилитации [136].
Некоторые авторы считают, что показатели прогноза должны определять сроки лечения в клинике и темпы физической реабилитации [130].
Проводились исследования по установлению диагностической значимости клинических параметров [102].
Нейросетевой анализ акустических сигналов позволяет проводить диагностику клапанных шумов сердца и оценивать систолическую и диастолическую фазы сердечных сокращений с постановкой предварительного диагноза [100].
Одной из самых главных проблем в кардиологии остаётся расшифровка электрокардиограмм (ЭКГ), требующая опыта квалифицированного врача [141].
В Великобритании сотрудники Университета Глазго ведут исследования по применению самообучающихся нейронных сетей для диагностики инфаркта миокарда по данным электрокардиографии [143]. Входными данными для сетей являются избранные параметры 12-канальной электрокардиограммы и 12-канальной векторкардиограммы.
Они же применили искусственные нейронные сети для дифференциальной диагностики фибрилляции предсердий и желудочковых и наджелудочковых экстрасистолий, возникающих на фоне синусового ритма.
Интерпретация электрокардиограмм с помощью нейросетей [104, 111, 112] была применена для диагностики злокачественных желудочковых аритмий [126].
Эти же авторы применили нейросети для интерпретации ЭКГ в диагностике кардиомиопатий.
В других работах описывается нейросетевая интерпретация электрокардиограмм, для распознавания фибрилляции предсердий [144] и других аритмий [116], дифференциальной диагностики синусового и желудочкового ритма [115].
W. Dassen и соавт. использовали нейронные сети для диагностики нижнего инфаркта миокарда. Для обучения использовались 57 различных электрокардиограмм, остальные 40 выполняли роль тестирующей выборки. Обученные нейронные сети показали высокий процент распознавания (до 90 - 95%) [111, 112].
Т.Yang и соавт., используя данные 360 электрокардиограмм, обучили нейронные сети различать инфаркт миокарда на электрокардиограмме, гипертрофию левого желудочка и нормальную ЭКГ. Контрольное тестирование проводилось на материале 493 ЭКГ [142, 143, 144, 145].
В работе E. Bertolucci, R. Mariotti, O. Biadi описывается нейронная сеть для диагностики коронарного атеросклероза на ранних стадиях. Диагноз выставлялся на основании таких параметров как пол, возраст, вес, рост, данных семейного анамнеза, наличия у обследуемого диабета, показателей систолического и диастолического артериального давления, уровня холестерина и липопротеидов различных классов в крови [103].
Широко применяются нейросети для диагностики атеросклероза [119].
Во всех перечисленных случаях основой обучения искусственных нейронных сетей составляли результаты диагностических исследований, а также данные анамнеза.
Проводится нейросетевая диагностика и определение стадии атеросклероза по рентгенологическим данным [118], акустическим сигналам [97].
Существует метод выявления атеросклеротических бляшек в артериях. Для этого используют нейронные сети, интерпретирующие флюорисцентные спектры, получаемые при исследовании тканей с помощью лазера [121].
Аналогичным образом проводится диагностика заболеваний периферических сосудов [98], таких как определение форм артериита [99].
Описывается нейросетевая диагностика заболеваний мышц по данным мышечной биопсии [120].
В области нейрофизиологии применение искусственных нейронных сетей строится на принципах функционирования нервных структур живых организмов [133].
С помощью нейросетей осуществлена попытка моделирования простейшей нервной системы [140] и ассоциативной памяти [107], изучения моторных функций мозга [117], моделирование связей мозга [109] и памяти [124], изучение функции глазодвигательных мышц [110, 113] и распознавания движущихся образов [125].
Нейросети используются терапевтами для дифференциальной диагностики заболеваний печени и желчного пузыря по лабораторным данным и данным УЗИ [138].
Проводились исследования по разработке системы назначения оптимальной стратегии лечения больных облитерирующим тромбангиитом и прогнозирования его непосредственных исходов [65].
Самообучающиеся нейронные сети также могут с успехом работать с медицинскими данными, относящимся к субъективным категориям, таким как психиатрия [135].
В офтальмологии нейросети использованы для интерпретации данных периметрии при диагностике глаукомы [123].
Е.В. Бутакова, А.С. Миньков применили нейросетевые экспертные системы для диагностики увеальных меланом. Для этого на основе обучения искусственных нейронных сетей была разработана компьютерная программа, позволяющая выставлять предварительный диагноз с определённой долей вероятности (в %) для каждого больного индивидуально [15].
Как видно, идёт активное внедрение в практику здравоохранения экспертных систем на основе самообучающихся искусственных нейронных сетей, однако в офтальмологии их применение явно ограничено. А в области обработки реографических кривых с применением дискретного преобразования Фурье и искусственных нейронных систем исследования вообще не проводились.

