Изучение развития и экспериментальной патологии нейронов в органотипических роллерных культурах структур мозга и сетчатки млекопитающих
На правах рукописи
АЛЕКСАНДРОВА
ОЛЬГА ПЕТРОВНА
ИЗУЧЕНИЕ РАЗВИТИЯ И ЭКСПЕРИМЕНТАЛЬНОЙ ПАТОЛОГИИ НЕЙРОНОВ В ОРГАНОТИПИЧЕСКИХ РОЛЛЕРНЫХ КУЛЬТУРАХ СТРУКТУР МОЗГА И СЕТЧАТКИ МЛЕКОПИТАЮЩИХ
03.00.25 – гистология, цитология, клеточная биология:
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата биологических наук
Москва – 2009
Работа выполнена в лаборатории экспериментальной нейроцитологии Научного Центра Неврологии РАМН.
Научный руководитель доктор биологических наук,
профессор Илья Васильевич Викторов.
Официальные оппоненты: доктор биологических наук
Элеонора Норайровна Григорян
кандидат биологических наук
Наталья Игоревна Калинина
Ведущая организация: Учреждение Российской академии наук Институт молекулярной генетики РАН.
Защита диссертации состоится _____________________ часов на заседании диссертационного совета Д 002.238.01 в Учреждении Российской академии наук Институте биологии развития им. Н.К. Кольцова РАН по адресу:
119334, Москва, ул. Вавилова, д. 26.
Сайт: http://idbras.comcor.ru/; e-mail: [email protected].
Автореферат разослан «___»_________________2009 года.
Ученый секретарь диссертационного совета,
кандидат биологических наук Абрамова Е.Б.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы.
В последние годы в экспериментальной цитологии значительное внимание уделяется разработке методов культивирования, при которых сохраняется трехмерная органотипическая структура соматических тканей с характерными для них межклеточными взаимодействиями. В международной номенклатуре эти методы культивирования обозначаются как 3D-система (three dimensional system).
Создана и апробирована специальная аппаратура для длительного культивирования таких культур в условиях искусственно созданной невесомости (Schwarz, Wolf, 1991; Schwarz, Wolf, and Trinh, 1991). Изучение 3D-цитосфер, независимо от методов их культивирования, направлено на получение возможно более полных данных о развитии и патологии клеток в изолированных тканевых системах, максимально соответствующих данным о процессах их развития и патологии in vivo.
При изучении структур центральной и периферической нервной системы широко используются методы органотипического культивирования срезов пренатального мозга, спинно- мозговых и симпатических ганглиев в камерах Максимова, постнатального мозга 7-8-суточных крыс культивируемых на покровных стеклах во вращающихся пробирках (Gahwiller,1981; 1984) и на полупроницаемых поликарбонатных мембранах (Stoppini at al., 1991), которые позволяют изучать условно трехмерные (плоскостные) культуры. Органотипические 3D-агрегаты были получены в реагрегированных культурах свободно плавающих клеток (DeLong 1970; DeLong, Sidman 1970; Layer P.G. et al. 2001; Nakagava S. 2003) и при культивировании диссоциированных клеток в гелевых матриксах (3D-коллаген, Матригель) (Cukierman et al., 2001; Chatterjee, Noldner, 1994).
Главным преимуществом метода органотипического культивирования ткани мозга является возможность длительного поддержания её гистотипической организации. Это позволяет изучать нервные и глиальные клетки, не изолируя их от локального окружения и не нарушая установленных или возникающих при культивировании нейронно-глиальных взаимоотношений. Организация структур ЦНС изменяется с возрастом животных. Так ткань, выделенная от эмбрионов и перинатальных животных, характеризуется начальными стадиями гистотипической организации. Во время культивирования в результате гибели части нервных клеток в срезах могут проходить изменения архитектоники тканевого эксплантата, что, однако, не препятствует дифференцировке сохранившихся нейронов и процессам синаптогенеза (Sassoe-Pognetto et al., 1996). Помимо этого, в изолированных эксплантатах вследствие утраты афферентных связей и эфферентных связей с клетками-мишенями внутренние межнейронные связи тканевого эксплантата реорганизуются, что сопровождается образованием дополнительных синапсов (Zimmer and Gahwiler, 1984).
Для органотипического культивирования используется, преимущественно, ткань эмбрионов и животных на ранних стадиях постнатального развития, в которой продолжаются процессы дифференцировки и созревания нейронов (Gahwiler et al.,1991; Feigenspan et al., 1993; Johansson et al., 2000). Т.о. для изучения этих процессов в ткани критичным является возраст животных-доноров. Например, для клеток-зёрен мозжечка это время ограничено концом второй недели постнатального развития, а для ткани гиппокампа 6-7 сут постнатального развития (Gahwiler et al.,1991; Фрумкина и др., 2001). При выделении гиппокампа у более взрослых крыс (старше 10 сут.) культуры не сохраняют своей жизнеспособности в течение достаточно долгого срока. С другой стороны, существует огромный пласт задач, которые необходимо решать при помощи экспериментов на дифференцированной ткани с установившимися характерными для нее межклеточными взаимодействиями. Поэтому, чрезвычайно актуальным является разработка методов органотипического культивирования нервной ткани взрослых животных, при которых трехмерная цитоархитектоника сохраняется и может поддерживаться достаточно длительное время.
Цели исследования: модификация и исследование возможностей использования метода роллерного органотипического культивирования для изучения развития и экспериментальной патологии нейронов структур головного мозга и сетчатки постнатальных и взрослых млекопитающих.
Исходя из этого, были поставлены следующие задачи:
1. Определить оптимальные условия для успешного роллерного органотипического культивирования свободноплавающих срезов, полученных из тканей постнатального мозга и сетчатки глаза крыс.
2. Изучить клеточную организацию 3D-сфероидов, формирующихся в роллерных культурах неокортекса, гиппокампа мозга и сетчатки глаза гистологическими, иммуногистохимическими методами и методом электронной микроскопии.
3. Установить оптимальные сроки культивирования структур постнатального мозга и сетчатки, в течение которых поддерживается жизнеспособность клеток и сохраняется органотипическая архитектоника, формирующихся 3D-сфероидов.
4. Используя 3D-сфероиды как модельную систему, изучить патоморфологические изменения нейронов в культурах головного мозга и сетчатки при экспериментальной ишемии и воздействии ряда нейротоксинов.
Научная новизна и практическая значимость работы.
1. Впервые получены органотипические 3D-культуры из постнатальных, дифференцированных тканей ЦНС на основе оригинального метода роллерного культивирования свободноплавающих срезов в быстровращающемся минироллере, разработанного в нашей лаборатории (Викторов и др., 1985).
2. Впервые показано, что дифференцированные ткани, выделенные из неокортекса, гиппокампа и сетчатки глаза способны формировать 3D-структуры в данных условиях культивирования. Трехмерная структура сфероидов позволяет поддерживать необходимые условия микроокружения для длительного переживания дифференцированных нервных клеток.
3. Впервые показано, что клетки, формирующие сфероиды, полученные на основе срезов сетчатки и гиппокампа, проявляют наибольшую жизнеспособность и пластические потенции к формированию органоспецифической структуры по сравнению с таковыми из неокортекса.
4. Впервые показана возможность неоангиогенеза в 3D-структурах (ретинальных сфероидах), образующихся при культивировании сетчатки постнатальных и взрослых крыс in vitro, за счет образования новых капилляров.
5. Использованная система культивирования дает возможность получать значительное число сфероидов, сохраняющих жизнеспособность клеток в течение 10-20 суток, что позволяет использовать их в качестве модельной системы, как для фундаментальных исследований, так и для скрининга нейротоксинов и лекарственных препаратов.
Личное участие автора.
Все работы по модификации метода роллерного органотипического культивирования, проведение основной части экспериментов по изучению влияния ишемии и нейротоксинов на исследуемые культуры, приготовление гистологических препаратов и их окраске, обработка полученных результатов, выполнены непосредственно автором. Основная часть работ по проведению иммуноцитохимических и электронно-микроскопических исследований выполнена при непосредственном участии автора.
Апробация работы. Основные результаты диссертационной работы были представлены на Всероссийской конференции по теме «Организация и пластичность коры больших полушарий головного мозга», Москва, 2001 г., на Всероссийской конференции по теме «Механизмы синаптической передачи», Москва. 2004г., на Всероссийской конференции по теме «Нейрохимия: фундаментальные и прикладные аспекты», Москва, 2005.
Публикации. По материалам диссертации опубликовано 9 статей, из них 5 – в изданиях, рекомендованных ВАК, и 7 тезисов в трудах международных и российских конференций.
Структура и объем работы. Диссертационная работа изложена на …….страницах, содержит... рисунка и состоит из следующих разделов: введения, обзора литературы, материалов и методов, результатов исследования, обсуждения результатов, выводов и списка литературы, включающего 268 цитируемых источника.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ.
Животные Исследования проводили на крысах линии Вистар на 6-9 сут постнатального развития для выделения гиппокампа, на 2-10 сут для выделения новой коры (неокортекса) и от 7 сут до 1 года для выделения сетчатки. В экспериментах использовано 550 животных. Все эксперименты проводили с соблюдением «Правил проведения работ с использованием экспериментальных животных» и, в частности, в соответствии с требованием положений Ассоциации по Исследованию Зрения и Офтальмологии ARVO (The Association for Research in Vision and Ophthalmology) при использовании животных в офтальмологических исследованиях.
Оборудование: суховоздушный инкубатор (35.5 оС), горизонтальный быстровращающийся минироллер (60 об/мин), флаконы из стекла Пирекс (50-100 мл) с силиконовыми пробками, стерильные инструменты для препарирования (пинцеты, ножницы, скальпели и т.д.), стеклянная и пластиковая посуда.
Среды и реактивы: -среда для инкубирования: МЕМ – 90% (Biochrom. Berlin. Germany), фетальная сыворотка крупного рогатого скота – 5% (Gibco), плацентарная сыворотка человека – 5%, глутамин –2 мМ, глюкоза – 0.8%, инсулин – 0.2 ед/мл, HEPES – 25 мМ, рН=7.2;
-фосфатный буфер Дульбекко (ФБД, Sigma),
-сбалансированный солевой раствор: NaCl –143.4 мM, HEPES – 5 мM, KCl – 5.4 мM, MgSO4 – 1.2 мM, NaH2PO4 – 1.2 мM, CaCl2 – 2.0 мМ, D-глюкоза – 10 мМ, феноловый красный – 10 мг/л.
-сбалансированный солевой раствор для проведения кислородноглюкозной депривации (КГД): NaCl – 143.4 мМ, HEPES – 5 мМ, KCl – 5.4 мМ, NaH2PO4 – 1.2 мМ, CaCl2 – 2.0 мМ, феноловый красный – 10 мг/л.
-фиксация культур: модифицированный фиксатор Теллесницкого-Лилли (ФУС): формалин 38% - 20%, этиловый спирт 96 – 70%, ледяная уксусная кислота – 10%; этиловый спирт.
Приготовление срезов для культивирования. Крыс анестезировали эфиром, декапитировали и далее головы стерилизовали 70% раствором этилового спирта. Мозг выделяли набором специальных инструментов и помещали в охлажденный фосфатный буфер Дульбеко (ФБД). Гиппокамп и неокортекс выделяли из обоих полушарий мозга и помещали в охлажденный раствор ФБД. Срезы, толщиной 300-500 мкм приготовляли при помощи бритвенного лезвия, скальпеля или чоппера. Срезы промывали в новой порции ФБД и переносили в питательную среду. Глаза крысы энуклеировали в стерильных условиях и переносили в стерильный раствор ФБД. Через циркулярный разрез роговицы удаляли хрусталик и стекловидное тело, выделяли сетчатку, дважды промывали её в ФБД и разрезали скальпелем на прямоугольные фрагменты размером 1-2 мм2, которые переносили в питательную среду. В один флакон с 10 мл среды помещали 20-30 срезов 2-3 сетчаток.
Культивирование срезов. Срезы гиппокампа, неокортекса (НК) и сетчатки переносили во флаконы (V= 50, 25, 15 мл) с питательной средой для культивирования (V= 10, 6, 3 мл соотв.), закрывали силиконовой пробкой, помещали на роллер в инкубатор при температуре 35.5 оС (рис.1) и культивировали при постоянном вращении (60 об/мин) в течение 10-15суток.

Рис. 1. Минироллер с флаконами для культивирования.
Смену среды производили 1-2 раза в неделю, заменяя 1/3 среды свежей средой. На различных сроках культивирования из флаконов в стерильных условиях отбирали фрагменты (2-3 шт.) для проведения гистологического контроля за состоянием культур. Контроль рН среды во время культивирования определяли по изменению цвета фенолового красного в составе среды. При закислении заменяли 1/3 среды свежей средой.
Гистологическая обработка. Приготовление парафиновых срезов культур, окрашивание по методу Ниссля крезиловым фиолетовым прочным и толуидиновым синим, гематоксилином-ванадиевым кислым фуксином и эозином, импрегнацию серебром производили по стандартным методикам (Viktorov, 1969; Viktorov et al., 2000).
Электронная микроскопия. Заливку культур для ультраструктурных исследований, приготовление полутонких и ультратонких срезов производили по стандартной методике. Исследования были выполнены в отделе электронной микроскопии Института физико-химической биологии им. А.Н. Белозерского Московского Государственного университета им. М.В. Ломоносова. Электронный микроскоп HU-12 (Hitachi).
Иммуноцитохимические исследования. Все ретинальные тельца (РТ) из каждого флакона промывали в ФБД и фиксировали в 4% растворе параформальдегида в ФБД (pH 7.4) или в фиксаторе Дэвидсона. Удаляли фиксатор и во флаконы заливали ФБД.
Половину РТ из каждого флакона использовали для гистологических исследований. Вторую половину замораживали и приготавливали серийные срезы на криостате, толщиной 20 мкм. Срезы монтировали на стёкла Super-Frost plus Slides и хранили при -200С. Для иммуноцитохимического анализа использовали стёкла, содержащие срезы только центральной части РТ, что определяли по окрашиванию сестринских срезов толуидиновым синим. Замороженные срезы инкубировали в блокирующем растворе, содержащем 5 % бычьего сывороточного альбумина (Sigma) и 0.5% Тритон Х-100 в ФБД.
Срезы инкубировали с первичными антителами (а.т.) в течение ночи в разведении: 1:2000 поликлональные кроличьи а.т. (Dako, Германия) к GFAP (глиальный фибриллярно-кислый белок), 1:500 мышиные моноклональные а.т. (Roche, Германия) к MAP2 (белок, ассоциированный с микротобулином-2) (mouse monoclonal; Roche, Mannheim, Germany), 1:200 мышиные моноклональные а.т. (Roche, Германия) к Thy-1 антигену ганглиозных клеток сетчатки и 1:500 а.т. к фактору Фон Виллебранта (Dako), выявляющего васкулярные структуры. Исключение первичных антител служило негативным контролем. Вторичные антитела, коньюгированные с красителем Texas-red (Leiden, Голландия), добавляли в разведении 1:200 на 1 ч. при комнатной температуре.
Метод TUNEL (TdT-опосредованное мечение dUTP конца) был проведён с использованием In Situ Cell Death Detection Kit, Fluorescein (Roche). Инкубирование срезов с раствором без терминальной трансферазы служило негативным контролем. В качестве контрастирующего ядерного окрашивания использовали DAPI (4-6-диамино-2-фенилиндол, флюорохром), в концентрации 0.001 мг/мл Н2О на 5 минут.
Микроскопия и анализ изображения. Для анализа полученных результатов использовали флуоресцентный микроскоп, оснащенный фотокамерой (Solms, Leica, Германия). Обработку результатов проводили с использованием программы Photoshop.
Моделирование ишемии. Кислородно-глюкозная депривация достигалась при помощи пропускания аргона в течение 5-7 мин. через сбалансированный солевой раствор, не содержащий глюкозу. Среду для культивирования удаляли из флаконов и сохраняли, а срезы промывали полученным сбалансированным раствором. Затем срезы заливали10-15 мл ишемического раствора и через раствор пропускали аргон в течение 3-5 минут. Флаконы, закрытые пробкой, помещали на роллер в инкубатор (35.5o C) на 1-2 ч., после чего раствор для КДГ удаляли из флаконов, а срезы заливали исходной средой. Через среду пропускали газовую смесь, содержащую 5% кислорода, затем флаконы помещали в инкубатор на 35.5 oС. Спустя 20 ч. после реоксигенации срезы промывали в ФБД и фиксировали для дальнейшей гистологической обработки.
Воздействие нейротоксинами. На роллерные культуры воздействовали следующими веществами в конечных концентрациях: глутамат (Глу) - 30 мкМ на культуры гиппокампа, 5 мМ на культуры сетчатки; НМДА – 60 мкМ на культуры неокортекса (НК), 250 мкМ на культуры сетчатки; клобензорекс – 100-500 мкМ на культуры НК; гомоцистеин -20 мМ на культуры сетчатки.
На 10-14 сутки культивирования (в случае сетчатки начиная с седьмых суток) из каждого флакона равные количества сфероидов и среды переносили в два новых флакона (один из которых служил контролем). В экспериментальные флаконы добавляли нейротоксины и нейропротектор, разведенные в среде.
Глутамат - наиболее распространенный возбуждающий нейромедиатор ЦНС (Fonnum, 1984; McGeer et al., 1987), способен взаимодействовать с несколькими типами мембранных рецепторов N-метил-D-аспартатным, каинатным и АМРА (a-амино-3-гидрокси-5-метил-4-изоксазол пропионовая кислота), специфическими агонистами которых являются соответственно N-метил-D-аспартат (НМДА), каиновая кислота и a-амино-3-гидрокси-5-метил-4-изоксазолпропионат (АМРА) (Watrins and Overman, 1987; Young and Fagg, 1990; Nedergaard, 2002). Длительное и интенсивное действие глутамата или его аналогов ведет к стойкой деполяризации клеточной мембраны нейронов, результатом которой является изменение проницаемости мембраны, нарушение внутриклеточного ионного баланса и энергозависимых систем, способных в норме восстановить ионный гомеостаз. Однако в результате непрекращающегося потока ионов из наружной среды происходит истощение энергетических ресурсов клеток, вывод ионов становится недостаточным и нарушение ионного баланса приводит к гибели клеток. Гомоцистеин – возбуждающая аминокислота, гомолог цистеина, является метаболитом метионина. Вызывает селективную стимуляцию НМДА-рецепторов и повреждение ДНК, активирует продукцию свободных радикалов и каспаз, что вызывает гибель нервных клеток ЦНС по механизмам апоптоза (Kim, Pae, 1996; Lipton et al., 1997; Kruman et al., 2000; Moore et al., 2001; Zieminska et al., 2003). Клобензорекс (2-хлорбензиламфетамин) – аналог амфетамина (Valtier, Cody, 1999). обладает свойствами стимуляции центральной нервной системы, хотя и более слабыми, чем сам амфетамин (Young, et al., 1997).
Нейропротектор абекарнил, b-карболин, действует как частичный бензодиазепиновый агонист и приблизительно в 100 раз более мощный, чем диазепам (Stephens et al., 1990). Абекарнил напрямую изменяет ГАМК-рецепторы (Pribilla et al., 1993) и, предполагается, что он действует по антиглутаматэргической модели (Vorobjev et al., 1995).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ ИССЛЕДОВАНИЯ.
- Органотипическое роллерное культивирование гиппокампа крысы.
В сфероидах, формирующихся при роллерном культивировании, органотипическая архитектоника дорзального гиппокампа крыс наиболее полно сохранялась при выделении материала у крыс на 6-8-сут. постнатального развития и содержания в культуре в течение 2-х недель (рис. 2 А, Б). Это согласуется с данными, полученными методами органотипического культивирования срезов гиппокампа постнатальных крыс по методу Гевиллера и методу Стоппини (Gahwiller, 1984; Stoppini at al., 1991).
На гистологических препаратах, окрашенных по методу Ниссля, как в контрольных (некультивированных, рис. 2 А) срезах, так и в культивированных сфероидах (рис. 2 Б), отчётливо видны дифференцированные нейроны полей СА1, СА2, СА3 и формаций – медиального и латерального лимбов зубчатой извилины гипокампа (ЗИГ), хилуса (Х), содержащего нейроны полиморфного слоя (ПС).
Полученные данные свидетельствуют о том, что в процессе культивирования фрагментов гиппокампа, выделенного на данном сроке постнатального развития крысы, происходят компенсаторные процессы, приводящие к восстановлению структуры и функции ткани in vitro, в основе которых лежит свойство нейрональной пластичности.




Рис.2. Роллерная органотипическая культура гиппокампа, выделенного из крысы на 7 сут постнатального развития. А - срез гиппокампа без культивирования. Б - 13 сут культивирования. Представлены поля гиппокампа: СА1, СА2, СА3, зубчатая извилина гиппокампа (ЗИГ), хилус (Х), полиморфный слой (ПС). В - дегенерация нейронов в полях СА1 и СА3 после воздействия на 12 сутки культивирования 30 мкМ Глу. Г - дегенерация нейронов в поле СА1 и зубчатой извилины и частичная - в поле СА3 после КГД. Масштаб: 0.5 мм. A-Г: окраска крезиловым фиолетовым.
Действие ишемии и глутамата. Результаты воздействия глутамата и ишемии на роллерные органотипические культуры гиппокампа крыс на 6-10 сутки постнатального развития показаны на рис.2 В, Г.
После длительного воздействия (20 ч.) низкими концентрациями глутамата (30-50 мкМ) наблюдалась полная нейрональная дегенерация в поле СА1 и частичные нейрональные нарушения в полях СА2 и СА3 гиппокампа (рис. 2 В). В условиях кислородно-глюкозной депривации в течение 2-х ч. и последующей реоксигенацией в течение 20 ч. наблюдалась нейрональная дегенерация в поле СА1, СА2 гиппокампа, частично поля СА3 и зубчатой извилины (рис. 2 Г).
Т.о., воздействие на роллерные культуры гиппокампа глутаматом и КГД показало, что наиболее чувствительными являются пирамидные нейроны поля СА1 аммонова рога, что согласуется с данными других авторов (Kirino, 1982; Фрумкина и др. 2002).
2. Органотипическое культивирование неокортекса мозга крысы.
Изучение динамики развития культур свободноплавающих срезов неокортекса (НК) крыс, выделенных на 6-8 сут постнатального развития, показало, что на начальных этапах адаптации к условиям культивирования (3-5 сут) часть нейронов дегенерирует в результате механической травмы и разрыва аксонов этих клеток, выходящих за пределы сформированной коры. В тоже время, на этой стадии развития культур продолжается миграция нейробластов и дифференцирующихся нейронов, поскольку НК еще находится в периоде активного гистогенеза (Berry, 1974). Этот процесс, при отсутствии экстракортикальных афферентных волокон и нарушении структуры радиальных глиоцитов, не обладает той строгой упорядоченностью, которая характерна для развивающейся in vivo новой коры головного мозга. Помимо этого, отсутствие экстракортикальных афферентных волокон и сопутствующая деафферентация части дифференцированных нейронов приводит к их гибели механизмом апоптоза.
Кортикальные срезы в процессе культивирования в течение 12-20 сут трансформируются в шаровидные структуры (сфероиды) (рис. 3 А). На их поверхности находится монослой глиоцитов (аналог glia limitans externa), за которым следует слой, включающий единичные клетки нейроглии (аналог молекулярного слоя коры) и корковая формация, образованная дифференцированными нейронами веретенообразной, пирамидной и полигональной формы, с типичным для зрелых нейронов крупным центрально расположенным ядром, содержащим интенсивно окрашенное ядрышко. Цитоплазма этих клеток содержит сформированную субстанцию Ниссля. Нейроны корковой формации, составляющие многоклеточный слой, не образуют, однако, типичной для новой коры шестислойной структуры. Подкорковый отдел, занимающий центр шаровидных кортикальных структур и сформированный глиоцитами, и не содержит нейронов (рис. 3 Б).
Анализ клеточного состава роллерных сфероидов НК свидетельствует о том, что при культивировании, в результате описанных выше процессов, сохраняется лишь часть нейронов исходной корковой пластинки и нарушается формирование характерной для этой структуры in vivo 6-слойной организации. НК приобретает вид монослойной структуры, образованной радиально ориентированными пирамидными и веретенообразными нейронами, что придает ей сходство с филогенетически более древними аллокортикальными корковыми формациями головного мозга (Zilles, Wree, 1985; Provis, 2002).
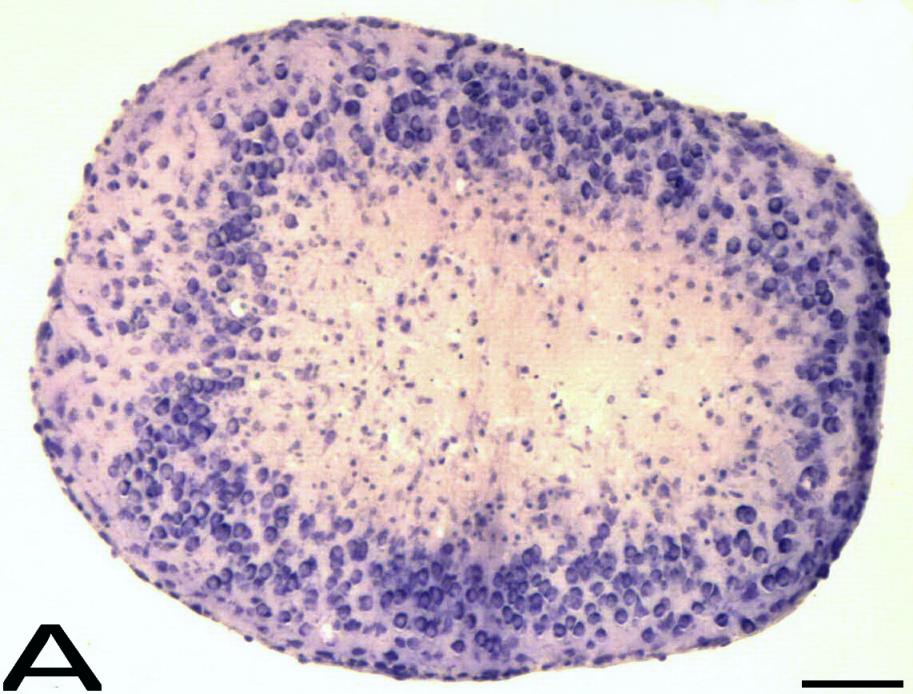



Рис.3. Роллерная органотипическая культура сенсомоторной коры 6-суточной крысы, 11сут культивирования. А, Б - контроль. В - дегенерация нейронов после воздействия 100 мкМ клобензорекса в течение 24 ч. Г- дегенерация нейронов после воздействия 60 мкМ НМДА в течение 24 ч. Окраска крезиловым фиолетовым по методу Ниссля. Масштаб: А- 100 мкм, Б, В, Г- 40 мкм.
В то же время на основании электронно-микроскопического исследования можно говорить о высокой степени клеточной дифференцировки этих структур и о формировании в них межнейронных синаптических связей (рис. 4).
Т.о. формирование внутрикортикальных межнейронных связей в изолированных in vitro фрагментах постнатального НК можно рассматривать, на ряду с морфогенетическими потенциями нейронов, в качестве одного из факторов цито- и гистотипической дифференциации культивируемой нервной ткани.
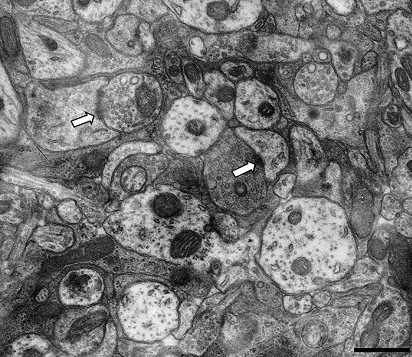
Рис. 4. Роллерная органотипическая культура новой коры мозга 8-сут крысы после 12 сут культивирования. Стрелка – синаптический аксодендритный контакт. Масштаб: 2 мкм.
Воздействие нейротоксинов. При воздействии клобензорексом (2-хлорбензиламфетамин) в течение 24 ч в концентрации 100-250 мкМ наблюдали появление погибших нейронов с пикнотическими ядрами (рис. 3, В), а повышение концентрации нейротоксина до 500-1000 мкМ приводило к полной дегенерации ткани. Эти данные указывают на то, что клобензорекс может метаболизироваться до d-амфетамина in vitro и вызывать нейрональную токсичность, подобную, описанной нейротоксичности амфетамина в культурах новой коры крыс (Stumm et al., 1999). Длительное воздействие (20-24 ч) НМДА в концентрации 30-60 мкМ также сопровождалось частичной нейрональной дегенерацией и появлением пикнотических ядер в сфероидах сенсомоторной коры (рис. 3, Г).
3. Органотипическое роллерное культивирование сетчатки крыс.
Наиболее полные данные, иллюстрирующие особенности формирования и динамики развития органотипической цитоархитектоники, были получены на роллерных культурах сетчатки взрослых крыс.
В органотипических культурах из плоских срезов сетчатки, размеры которых не превышают 1-2 мм2, формируются ретинальные тельца (РТ), которые имеют круглую или эллипсоидную форму и сохраняются в течение всего срока культивирования (рис. 5 А). На поперечном срезе РТ можно наблюдать циркулярные замкнутые слои сетчатки, полностью сохраняющие свою цитоархитектонику, характерную этой структуре in vivo. Фоторецепторы образуют наружный слой сетчатки, который покрыт монослоем пигментного эпителия. Внутри от наружного клеточного слоя располагается наружный сетчатый (плексифорный) слой, сформированный клеточными отростками горизонтальных и биполярных клеток и аксонными окончаниями фоторецепторов. Внутренний нуклеарный слой включает ядра нескольких клеточных типов (биполярные, Мюллеровские, горизонтальные и амакриновые клетки). В состав внутреннего сетчатого (плексифорного) слоя входят аксоны биполярных клеток и дендриты ганглиозных клеток. Самый внутренний уровень сетчатки образован ганглиозным клеточным слоем, который в основном состоит из тел ганглиозных клеток, также здесь находятся тела части амакриновых клеток (рис. 5 Б).


Р
Рис. 5. Роллерная органотипическая культура сетчатки, выделенная у крыс после 7 суток постнатального развития. Клеточная структура РТ. 8 суток культивирования. Окраска: А - гематоксилин-эозином, Б – толуидиновым синим. Масштаб: А - 200 мкм, Б - 20 мкм.
В некоторых РТ постнатальных крыс были обнаружены единичные розетки, образованные слоем фоторецепторов (рис. 6 А, Б). Формирование части розеток происходило в местах локального повреждения наружного ядерного слоя или пигментного эпителия, при этом на поверхности сетчатки вначале появлялась ямка, которая затем углублялась, её края смыкались, и образовывалась циркулярная розетка (рис.6 В). In vivo ретинальные розетки можно наблюдать при различных патологиях или в экспериментальных условиях. Формирование розеток наблюдали и в органных культурах (культивирование цельных структур) эмбриональной и постнатальной сетчатки (Liljenist-Larsson et al., 2003; Ogilvile et al., 1999). По данным патогистологических исследований (Milam, 1998), розетки образуются в результате нарушений развития глаза в онтогенезе, а также при отслойке и пигментной дистрофии сетчатки, что указывает на связь формирования розеток с повреждением пигментного эпителия и наружного ядерного слоя (Shimada et al., 1973; Liu et al., 1986; Layer et al., 2001).



Рис. 6. Роллерная органотипическая культура сетчатки, выделенной у крыс после 7сут постнатального развития. 12 сут культивирования. Формирование розеток в наружном ядерном слое, фоторецепторными клетками. Окраска крезиловым фиолетовым по методу Ниссля. Масштаб: А- 100 мкм; Б, В- 50 мкм.
На начальных стадиях культивирования (1-3 сут) часть РТ содержит внутреннюю полость, которая позднее полностью исчезает в результате роста аксонов ганглиозных клеток, пролиферации и миграции клеток глии и фибробластов, которые образуют центральное тканевое ядро РТ. Это можно наблюдать на препаратах, полученных с помощью метода импрегнации серебром, выявляющего нервные волокна (рис. 7 А). В центральном ядре отдельных РТ при помощи иммунофлуоресцентной реакции с использованием антител к фактору Фон Виллебранта, позволяет визуализировать клетки сосудистого эндотелия, были выявлены новообразованные капилляры (рис. 7 В). Данные, полученные гистологическими и иммуноцитохимическими методами, нашли подтверждение при исследовании РТ при помощи электронно-микроскопических методов. На рисунке 7 Г виден новообразованный капилляр.




Рис. 7. Органотипическая роллерная культура сетчатки взрослой крысы.: А - 3 сут. культивирования, внутренняя полость в РТ. Б, В, Г - 7 сут. культивирования. Стрелками указаны капилляры. Окраска: А, Б – импрегнация серебром, В - иммунофлуоресцентная реакция к фактору Фон Виллебранта. Масштаб: А, В – 200 мкм, Б – 50 мкм. Г – электронная микрофотография. Масштаб – 8 мкм.
Использование антител к МАР-2 подтвердили данные, полученные гистологическими методами, и свидетельствующие о росте регенерирующих аксонов ганглиозных клеток к центру РТ, где формируется плотный нейропиль (рис. 8 А). Для идентификации ганглиозных клеток были использованы специфические для этих клеток антитела к Thy-1. Как видно на рис 8 Б, в РТ выявляется большое количество ганглиозных клеток, меченных антителами к Thy-1. При использовании антител, специфических к GFAP было показано, что каркас РТ образует сложный глиальный матрикс, включающий тела и отростки Мюллеровских клеток (рис. 8 В). Радиально ориентированные апикальные отростки Мюллеровских клеток и астроцитов, локализованы как в наружном ядерном слое, так и в других слоях РТ, включая центральную область нейропиля (рис. 8 В). Во внутреннем плексифорном слое отростки глиальных клеток формируют плотное сплетение, в котором глиальные волокна ориентированны, преимущественно, параллельно поверхности РТ, в то время как в центральной части РТ глиальные волокна образуют плотную сеть.
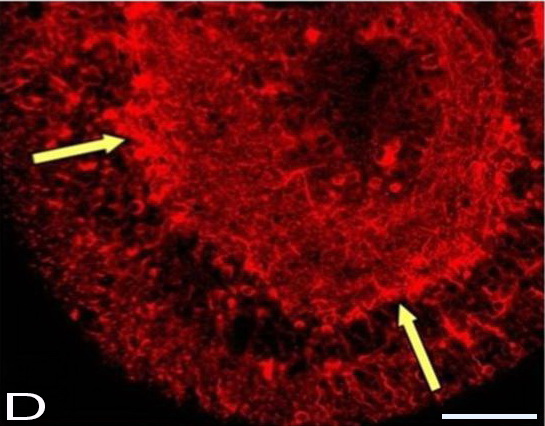


Рис. 8. Роллерная культура сетчатки взрослой крысы. Иммуноцитохимические реакции: А - к GFAP, Б – к Thy-1, В - к MAP-2. Стрелками указан слой ганглиозных клеток. Масштаб: А, В – 100 мкм, Б – 500 мкм.
Таким образом, проведены исследования гистологическими, ультраструктурными и иммуноцитохимическими методами серийных срезов РТ, образующихся после культивирования из сетчатки постнатальных и взрослых крыс. Показано, что стенка РТ представляет собой структуру, сходную с клеточной структурой сетчатки, взятой на том же сроке развития крыс. Сохранность структуры фоторецепторов, нейронов внутреннего ядерного и ганглиозного слоёв поддерживается вплоть до 3-х недель in vitro (рис. 8).
Воздействие ишемии и нейротоксинов. В роллерной органотипической культуре сетчатки, выделенной из глаза крысы после 8 сут постнатального развития, исследовано повреждение нейронов в результате ишемического воздействия (рис. 9 А, Б). Наблюдалась выраженная дегенерация нейронов ганглиозного и внутреннего ядерного слоёв. При окраске гематоксилин/ эозином/трипановым синим, можно наблюдать многочисленные пикнотические и набухшие ядра. На препаратах сетчатки взрослой крысы после воздействия гипоксии при импрегнации серебром, также была выявлена дегенерация нейронов во всех слоях сетчатки (рис. 9 В, Г).
Было изучено воздействие 250 мкМ НМДА на роллерные органотипические культуры сетчатки взрослой крысы. На срезах можно было наблюдать практически полную дегенерацию нейронов ганглиозного слоя, наличие пикнотических и набухших ядер во внутреннем ядерном слое.
Гомоцистеин в конечной концентрации 20 мМ вызывал нейродегенерацию в ганглиозном и внутреннем ядерном слоях, что является подтверждением имеющихся данных о токсичности гомоцистеина для клеток ганглиозного слоя. При введении в стекловидное тело глаза мыши гомоцистеин вызывал частичную гибель ганглиозных клеток по механизму апоптоза (Moore et al., 2001). Кроме того, по результатам исследований других авторов, нейроцитотоксическое действие гомоцистеинимии является одним из факторов повреждения сетчатки при ряде заболеваний (Mattson, Shea, 2003).




Рис. 9. Роллерная органотипическая культура сетчатки, культивирование 8 сут. Ишемическое повреждение нейронов. А, Б – культура сетчатки, выделенная у крысы после 8 - сут. постнатального развития. В, Г – культура сетчатки, выделенная у взрослой крысы. Окраска: А, Б - гематоксилин/эозин – трипановый синий, В, Г – импрегнация серебром. Масштаб: 50 мкм.
Также было изучено токсическое воздействие Глу на роллерных культурах сетчатки взрослой крысы. Специфическим для выявления апоптоза иммуноцитохимическим методом TUNEL было показано, что в культурах, обработанных Глу выявляется значительно большее число TUNEL-положительных клеток (рис. 10 В, Г), чем в контрольных культурах (рис. 10 А, Б).

Рис.10. Роллерная органотипическая культура сетчатки взрослой крысы. Воздействие 5 мМ Глу. Мечение методом TUNEL для выявления апоптоза клеток и DAPI для контрастирования ядер. А, Б, В – контроль (1.7 ± 0.8%). Г, Д, Е – воздействие Глу (25.3 ± 1.06%). Масштаб: А, Б, Г, Д – 300 мкм, В, Е – 25 мкм. Вычисляли стандартное отклонение и среднюю величину. Статистическое сравнение было проведено односторонним анализом среднего квадратичного отклонения ANOVA. Значение 0.05 считали статистически достоверным.
На культурах сетчатки взрослой крысы было изучено предполагаемое нейропротекторное действие абекарнила (b-карболина) (Stephens et al., 1990). Введение нейропротектора абекарнила в концентрации от 1 нМ до 100 нМ, совместно с Глу, не сопровождалось выраженным нейропротекторным эффектом. Более того, при повышении концентрации абекарнила до 10-100-500 мкМ мы наблюдали усугубление токсичности Глу и полную дегенерацию культивируемой ткани сетчатки. Таким образом, по нашим данным в роллерных культурах сетчатки крыс абекарнил не препятствует дегенерации нейронов при нейроцитотоксическом воздействии Глу. Хотя на нейроны коры головного мозга, культивированные на стёклах и обработанные глутаматом, этот препарат оказывал нейропротекторное действие (Ruscher et al., 2007). Это противоречие, возможно, объясняется различиями нейрохимических свойств нейронов (различиями в экспрессии нейромедиаторных рецепторов, в восприимчивости нейронов на разных стадиях развития) и различиями межнейронных связей коры головного мозга и сетчатки. Полученные нами данные говорят о том, абекарнил не может рассматриваться как нейропротектор при патологии сетчатки.
Таким образом, оригинальный метод органотипического роллерного культивирования свободноплавающих фрагментов мозга и сетчатки млекопитающих позволяет создать условия, максимально приближенные к условиям in vivo по сравнению с другими методами культивирования. Он может найти широкое применение в исследованиях развития и дифференцировки нервной ткани, а также в экспериментальной нейропатологии и изучении свойств биологически активных нейропротекторных препаратов. Особенно важно использование таких методов исследования для медицины при моделировании различных патологических состояний мозга и сетчатки: ишемия мозга, болезнь Альцгеймера, глаукома, дистрофия, отслоение сетчатки и др.
ВЫВОДЫ.
1. Впервые показана возможность использования метода органотипического культивирования для изучения процессов развития и экспериментальной патологии нейронов головного мозга и сетчатки постнатальных и взрослых животных.
2. Определены экспериментальные условия, в том числе возраст животных, способы выделения ткани, среды и сроки культивирования, необходимые для выполнения экспериментальных исследований с использованием метода органотипического роллерного культивировании нервной ткани постнатальных и взрослых животных
3. Преимущество метода роллерного культивирования состоит в возможности одновременного культивирования большого числа фрагментов нервной ткани в идентичных условиях, что обеспечивает статистическую достоверность полученных результатов.
4. Показано, что исходно уплощенные срезы ткани головного мозга и сетчатки формируют in vitro сфероиды с трехмерной организацией, характерной для соответствующих отделов ЦНС in vivo.
5. Схранность трехмерной цитоархитектоники в роллерных культурах гиппокампа, неокортекса и сетчатки определяется межнейронными и нейроглиальными отношениями, сформировавшимися к началу культивирования и специфическими для конкретных изученных структур ЦНС.
6. Впервые показано образование новых капилляров (неоангиогенез) в роллерных культурах сетчатки постнатальных и взрослых крыс с помощью гистологических, ультраструктурных и иммуноцитохимических исследований.
7. Показана возможность использования метода роллерного культивирования, как адекватной модели для изучения влияния нейропротекторов при патогистологических изменениях нейронов.
Список публикаций.
Статьи:
- Victorov I.V., Lyjin A.A., Aleksandrova O.P. A new method of organotypic brain cultures: free-floating slices of postnatal rat hippocampus. // Brain. Res. Prot. 2001. Vol. 7. P. 30-37.
- Александрова О.П., Лыжин А.А., Викторов И.В. Гистогенез гиппокампа и новой коры головного мозга постнатальных крыс в органотипических роллерных культурах свободноплавающих срезов мозга. // Бюлл. экспер. биол. и мед. 2001. № 9. C. 333-337.
- Востриков В.М., Коломеец Н.С., Александрова О.П., Викторов И.В., Уранова Н.А., Сухих Г.Т. Органотипические культуры свободноплавающих срезов продолгованого мозга эмбрионов человека. // Морфология. 2003. №4. С. 41-47.
- Викторов И.В., Лыжин А.А., Александрова О.П., Фрайер Д., Дирнагль У. Роллерные органотипические культуры сетчатки постнатальных крыс. // Бюлл. эксперим. биол. и мед. 2004. Т. 137. №4. С. 476-480.
- Александрова О.П., Лыжин А.А., Викторов И.В. Особенности развития сенсомоторной коры 7-8 дневных крыс в роллерных культурах свободноплавающих срезов мозга. // Морфология. 2004. Т. 125. №1. С. 12-15.
- Викторов И.В., Александрова О.П., Алексеева Н.Ю., Лыжин А.А. Роллерные органотипические культуры сетчатки постнатальных и взрослых крыс, как экспериментальная модель для изучения ретинопатий. // Морфология. 2004. Т. 125. №1. С. 124-125.
- Aleksandrova O.P., Lyzhin A.A., Victorov I.V. Characteristics of the sensomotor cortex in rats aged 7-8 days in roller cultures of free-floating brain slices. // Neurosci. Behav. Phisiol. 2005. V. 35. P. 9-15.
- Vostrikov V.M., Kolomeets N.S., Aleksandrova O.P., Viktorov I.V., Uranova N.A., Sukhikh G.T. Organotypic cultures of free-floating slices of human embryo metulla oblongata. // Neurosci. Behav. Physiol. 2005. V. 35. P. 9-15.
- Rzeczinski S., Victorov I.V., Lyjin A.A., Aleksandrova O.P., Harms C., Kronenberg G., Freyer D., Scheibe F., Priller J., Endres M., Dirnagl U. Roller culture of free-floating retinal slices: a new system of organjtypic cultures of adult rat retina. // Ophthalmic Research. 2006. Vol. 38. P. 263-269.

