Полиморфизм гена mdr1 : популяционные и фармакогенетические аспекты
на правах рукописи
ИГНАТЬЕВ ИЛЬЯ ВЛАДИМИРОВИЧ
Полиморфизм гена MDR1: популяционные и фармакогенетические аспекты
03.00.15. – генетика
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата биологических наук
- Москва 2007 -
Работа выполнена в лаборатории лекарственного мониторинга филиала «Клиническая фармакология» ГУНЦ Биомедицинских технологий РАМН, г. Москва
Научный руководитель:
Доктор медицинских наук, доцент Сычев Д.А.
Официальные оппоненты:
Доктор биологических наук Поляков А.В.
Кандидат биологических наук Аксенова М.Г.
Ведущая организация: кафедра Фармакогенетики Медико-биологического факультета Российского Государственного Медицинского Университета (РГМУ)
Защита диссертации состоится « » мая 2007 г. в ____ на заседании Диссертационного совета Д 217.013.01 при Государственном научно-исследовательском институте генетики и селекции промышленных микроорганизмов по адресу: 117545, г. Москва, 1-й Дорожный проезд, д.1.
С диссертацией можно ознакомиться в библиотеке ФГУП «ГосНИИ генетика».
Автореферат разослан « » апреля 2007 г.
Ученый секретарь
Диссертационного совета,
кандидат биологических наук Заиграева Г.Г.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Прогресс в медицине ведет к непрерывному усложнению и детализации методологии. По мере увеличения количества лекарственных средств (ЛС), усложняются подходы к их применению. Современная стратегия разработки ЛС сводится к поиску первопричины заболевания и воздействия на неё, препараты становятся более узконаправленными, специфичными.
Фармакокинетические процессы находятся под генетическим контролем. Большинство ЛС воспринимаются организмом как ксенобиотики. В геноме человека с биотрансформацией ксенобиотиков связано от 500 до 1200 различных генов [Sakaeda et al., 2004]. Поэтому индивидуальные генетические различия между людьми являются серьезным фактором, который становится причиной многих нежелательных лекарственных реакций (НЛР), в том числе приводящих к гибели или инвалидизации пациентов (кровотечения, поражения печени, почек, костного мозга и т.д.). Изучение индивидуальных генетических различий, лежащих в основе вариабельности ответа организма на тот или иной препарат, приобретает первостепенное значение для оптимизации фармакотерапии.
Индивидуализация фармакотерапии, которой занимается фармакогенетика, состоит из выявления полиморфных маркеров, ассоциированных с изменением реакции организма на ЛС, разработки методов генотипирования больных (выявлению аллельных вариантов полиморфных маркеров) и внедрения этого подхода в практическую медицину.
Транспортный белок, гликопротеин Р, кодируемый геном MDR1, играет ключевую роль в выведении целого ряда ЛС, включая дигоксин. Исходя из этого, влияние генетического полиморфизма гликопротеина Р на фармакокинетику дигоксина должно приводить к важным клиническим последствиям [Hoffmeyer et al., 2000; Marsolini, Kim, 2002, 2004]. В настоящее время изучено много полиморфных маркеров в гене MDR1 [Woodahl et al., 2004], но предпочтения по исследованию ассоциаций отдаются трем из них (C1236T, G2677T/A и C3435T). Остальные, как правило, встречаются с низкой частотой, которая не позволяет объяснить широко распространенные нарушения «работы» гликопротеина Р. Предполагают, что полиморфные маркеры C3435T и С1236Т приводят к снижению экспрессии гена MDR1, а «кажущееся» влияние полиморфного маркера G2677T/A объясняют эффектом сцепления [Sai et al., 2003].
Субстрат гликопротеина Р, дигоксин, широко применяется в клинической практике в течение более чем 200 лет. В настоящее время дигоксин назначается пациентам с хронической сердечной недостаточностью (ХСН), с постоянной формой мерцательной аритмии (ПФМА), эффективность его доказана в мультицентровом исследовании DIG. Являясь ЛС с узкой терапевтической широтой, дигоксин вызывает НЛР в виде гликозидной интоксикации в 10-30% случаев [Bertilsson, Kalow, 1993]. Таким образом, по прежнему существует реальная потребность в оптимизации фармакотерапии дигоксином, которую можно осуществить путем индивидуализации выбора его режима дозирования на основании генотипирования.
Известно, что представители различных этнических групп могут различаться по характеру ответа на лекарственное воздействие [Wielandt et al., 2004]. Поскольку существенная роль в развитии НЛР принадлежит генетическим факторам [Kewal, 2002], многие авторы полагают главной причиной возникновения вариаций при ответе на фармакотерапию генетические межпопуляционные различия. Начиная с первой работы, в которой изучались межэтнические различия в частотах аллелей и генотипов полиморфных маркеров гена MDR1 [Ameyaw et al., 2000], начались исследования полиморфизма данного гена сначала среди европеоидов [Gascorbi et al., 2001], а потом и среди представителей других рас [Chelule et al., 2003; Li et al., 2006].
В России этот вопрос практически не разработан. Изучены частоты аллелей и генотипов ряда полиморфных маркеров гена MDR1 только у русских [Goreva et al., 2004], причем авторы сосредоточили свое внимание на вопросах, в первую очередь, канцерогенеза. Для внедрения результатов изучения зависимости возникновения НЛР от генотипа пациента необходимо дальнейшее исследование частот аллелей и генотипов гена MDR1 в различных этносах нашей страны.
Изучение ассоциации полиморфных маркеров с нарушениями фармакокинетических процессов, сопряженное с выявлением межэтнических различий в распределении аллелей и генотипов данных маркеров, позволит оптимизировать фармакотерапию, что будет способствовать повышению эффективности и безопасности таковой.
Цели и задачи работы. Целью данной работы являлось изучение ассоциации полиморфных маркеров С1236Т и С3435Т гена MDR1, кодирующего гликопротеин Р, с развитием дигиталисной интоксикации и повышением равновесной концентрации дигоксина в крови у больных мерцательной аритмией при терапии дигоксином, а также выявление межэтнических различий в частотах аллелей и генотипов данных полиморфных маркеров в четырех различных этнических группах.
В ходе работы были решены следующие задачи:
- Оценена ассоциация полиморфных маркеров С1236Т и С3435Т гена MDR1 с развитием гликозидной интоксикации у больных с постоянной формой мерцательной аритмии, длительно принимающих дигоксин.
- Сопоставлена равновесная концентрация дигоксина в плазме крови больных с носительством аллелей или генотипов полиморфного маркера С3435Т гена MDR1.
- Изучено распределение аллелей и генотипов полиморфных маркеров С1236Т и С3435Т гена MDR1 в случайных выборках коренного и некоренного населения Чукотского Автономного Округа и этнических казахов, сопоставлены межэтнические различия.
Научная новизна работы. В данной работе впервые в России изучается полиморфизм гена MDR1, кодирующего гликопротеин Р, как фактор, влияющий на безопасность фармакотерапии дигоксином. Выявлена ассоциация полиморфного маркера С3435Т и отсутствие таковой для полиморфного маркера С1236Т с развитием симптомов гликозидной интоксикации. Обнаружена ассоциация полиморфного маркера С3435Т с изменением равновесной концентрации дигоксина в плазме крови у больных ХСН с ПФМА, проживающих в Москве. Впервые в России изучены межэтнические различия в распределении аллелей и генотипов двух полиморфных маркеров данного гена.
Практическая ценность работы. Проведение генотипирования больных по полиморфному маркеру С3435Т гена MDR1 рекомендуется проводить всем больным, которым планируется назначение или уже назначается дигоксин. Разработан алгоритм выбора начальной дозы дигоксина в зависимости от результатов генотипирования по полиморфному маркеру С3435Т гена MDR1 для повышения безопасности фармакотерапии.
Результаты данной работы в области изучения межэтнических различий в частотах аллелей и генотипов гена MDR1 могут послужить основой для региональных рекомендаций по применению дигоксина.
Апробация работы. Основные результаты доложены и обсуждены на совместной научно практической конференции филиала «Клиническая фармакология» ГУ НЦ БМТ РАМН и кафедры клинической фармакологии и пропедевтики внутренних болезней ММА им. И.М. Сеченова (сентябрь 2006 г.), V Международной конференции «Клинические исследования лекарственных средств» (ноябрь 2005 г.), VII Ежегодной конференции Общества специалистов по сердечной недостаточности «Сердечная недостаточность» (Москва, декабрь 2005 г.), IV Съезде Российских ревматологов (Казань, май 2005 г.), II Всероссийском съезде фармацевтических работников (Сочи, июнь 2005 г.), I Съезде клинических фармакологов Сибирского округа (Барнаул, май 2006 г.), Конференции «Проблемы клинической фармакологии и моделирования в фармакологии и биомедицине» (Ростов-на-Дону, сентябрь 2006 г.).
Публикации. По материалам работы опубликовано 10 печатных работ в журнала и сборниках материалов конференций.
Структура и объем диссертации. Диссертация состоит из следующих разделов: введение, обзор литературы, описание использованных материалов и методов, результаты и их обсуждение, заключение, выводы и список литературы. Материал диссертации изложен на 107 страницах машинописного текста и содержит 22 таблицы и 8 рисунков.
СОДЕРЖАНИЕ РАБОТЫ
ОБЪЕКТЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Описание клинической группы. В исследование были включены 103 больных ХСН с ПФМА. Критерии включения: давность мерцательной аритмии не менее 1 года, прием дигоксина (0,25 мг/сутки) более 1 месяца, наличие ХСН функционального класса I-III, стабильность состояния не менее месяца, фракция выброса левого желудочка ниже 40% (по данным эхокардиографии), подписанное информированное согласие об участии в исследовании. Критерии исключения: нарушения функции печени, почек, гипокалиемия, ХСН IV функционального класса, пороки сердца (кроме относительной митральной и/или трикуспидальной недостаточности, но не более 2 степени), острые коронарные синдромы в предшествующие 3 месяца, тяжелые сопутствующие заболевания, сахарный диабет, наличие противопоказаний к назначению дигоксина.
Описание популяционных групп. Популяционные группы набирали из подростков, содержащихся в школах-интернатах Чукотского Автономного Округа во время планового медицинского осмотра в 2004 году, а также из студентов Карагандинской медицинской академии в 2005 году на добровольной основе. Национальность устанавливали со слов обследованных. Группа чукчей включала в себя 77 человек, группа эвенов – 48 человек, группа русских – 124 человека и группа казахов – 100 человек. Все включенные в исследование индивиды не имели на момент обследования каких-либо серьезных заболеваний или отклонений в развитии.
Выделение ДНК. ДНК выделяли стандартным фенольным методом с протеиназой К [Budowle, Baechtel, 1990].
Определение равновесной концентрации дигоксина. Венозная кровь для определения концентрации дигоксина отбиралась в количестве 10 мл в сухие пробирки с гепарином, утром натощак, перед плановым приемом очередной дозы дигоксина. Концентрацию дигоксина в плазме крови определяли методом поляризационного флуоресцентного иммунологического анализа на приборе и с помощью реактивов фирмы Abbot Inc. (США).
Генотипирование. Генотипирование проводили методом ПЦР-ПДРФ (полимеразная цепная реакция и полиморфизм длин рестрикционных фрагментов). На первой стадии выбранные фрагменты гена, содержащие полиморфные участки, амплифицировали путем ПЦР на программируемом термостате «Терцик МС2», производства НПФ ДНК-Технология (Россия). Затем продукты ПЦР подвергали обработке эндонуклеазами рестрикции II типа (рестриктазами). Специфичные праймеры и рестриктазы для каждого полиморфного маркера приведены в таблице 1. Праймеры для ПЦР подобраны с помощью программы PrimerSelect 4.05©1993-2000 DNASTAR Inc. и синтезированы в ЗАО «Синтол» (Россия). Рестриктазы закуплены у ЗАО «Хеликон» (Россия). Промежуточные (контроль прохождения ПЦР) и окончательные (длины продуктов расщепления рестриктазами) результаты выявляли с помощью электрофореза в вертикальных акриламидных гелях (5% гель длиной 5 см для продуктов амплификации и 10% гель длиной 15 см для продуктов расщепления рестриктазами, напряженность электрического поля 10 В/см). Время, необходимое для разделения фрагментов ДНК подбирали экспериментально. Длины фрагментов анализировали путем сравнения с маркерной ДНК (ДНК плазмиды pUC19, расщепленная рестриктазой MspI, или стандартный маркер 100 b.p.™SibEnzyme). После окончания фореза гели окрашивали раствором бромистого этидия (50 нг/мл) и анализировали в ультрафиолетовом свете (312 нм).
Таблица 1.
Праймеры и рестриктазы для идентификации полиморфных маркеров гена MDR1
| Замена | Последовательность праймеров | Рестрик- таза | Размеры продуктов рестрикции |
| С1236Т | M1236-1 (прямой) 5’-CCACCGTCTGCCCACTCTGC-3’ M1236-2 (обратный) 5’-GGCCATCTATCCACCTATCTAA-3’ | HaeIII | 426 п.н. + 35 п.н. |
| C3435T | MDR1for (прямой) 5’-GATGGCAAAGAAATAAAGCGACTG-3’ MDR1rev (обратный) 5’-ACCAGCCCCTTATAAATCAAACTA-3’ | MboI | 147 п.н. + 133 п.н. |
Статистическая обработка результатов. Статистический анализ проводился с использованием статистической программы Past, version 1.34 (http://folk.uio.no/ohammer/past). Для определения статистической значимости различий частот аллелей и генотипов в группах больных применялся критерий 2, для аллелей применялась поправка Йейтса на непрерывность (вводилась вручную, поскольку компьютерной программой не предусмотрена). Относительные риски рассчитывались с помощью стандартной программы-калькулятора [Bland, Douglas, 2000]. Статистическую значимость различий в концентрации дигоксина в плазме крови в группах больных определяли с помощью непараметрического метода Манна-Уитни. Значения чувствительности, специфичности, предсказательной ценности положительного (PPV) и отрицательного (NPV) результатов теста рассчитывались по общепринятым формулам [Флетчер Р., 1998].
Проведение исследования одобрено этическим комитетом ГКБ № 23 им. «Медсантруд» г. Москвы, комитетом по этике Департамента здравоохранения и социального развития ЧАО и признано легитимным Комитетом по этике Ассоциации медицинских и фармацевтических вузов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
1. Взаимосвязь полиморфизма гена MDR1 с возникновением НЛР при приеме дигоксина у больных с постоянной формой мерцательной аритмии.
Мы изучали группу больных с ПФМА, которым была показана терапия дигоксином. Симптомы гликозидной интоксикации (снижение аппетита, тошнота, рвота, желудочковая экстрасистолия) были выявлены у 26 пациентов (25%).
Частоты аллелей и генотипов по полиморфному маркеру С1236Т в группах больных с симптомами гликозидной интоксикации и без таковых приведены в таблице 2. Частоты аллелей и генотипов полиморфного маркера С1236Т достоверно не различались между группами больных с гликозидной интоксикацией и без таковой.
Иная картина наблюдалась при анализе частот аллелей и генотипов полиморфного маркера С3435Т (Таблица 3). Из таблицы 3 видно, что имеется четкая ассоциация генотипа ТТ и аллеля Т полиморфного маркера С3435Т с развитием гликозидной интоксикации.
Таблица 2.
Частоты аллелей и генотипов полиморфного маркера С1236Т гена MDR1 в группах больных с симптомами гликозидной интоксикации (СГИ+) и без таковых (СГИ-)
| Аллель / генотип | СГИ+ n = 20 | СГИ- n = 65 | 2 | р |
| С | 21 | 78 | 0,401 | 0,515 |
| Т | 19 | 52 | ||
| СС | 4 | 23 | 1,860 | 0,395 |
| СТ | 13 | 32 | ||
| ТТ | 3 | 10 |
Таблица 3.
Частоты аллелей и генотипов полиморфного маркера С3435Т гена MDR1 в группах больных с симптомами гликозидной интоксикации (СГИ+) и без таковых (СГИ-)
| Аллель / генотип | СГИ+ n = 26 | СГИ- n = 77 | 2 | р |
| С | 12 | 83 | 13,643 | <0,001 |
| Т | 40 | 71 | ||
| СС | 2 | 18 | 20,897 | <0,001 |
| СТ | 8 | 47 | ||
| ТТ | 16 | 12 |
Мы определили равновесную концентрацию дигоксина в плазме крови у 29 случайно выбранных больных. Из них генотип СС имели 6 пациентов, СТ – 18 пациентов, ТТ – 5 пациентов. Наиболее высокая концентрация дигоксина наблюдалась у пациентов с генотипом ТТ по сравнению с пациентами, имеющими генотипы СС и СТ (2,03 ± 0,14 vs 1,09 ± 0,15, р = 0,008 и 2,03 ± 0,14 vs 1,54 ± 0,23, р = 0,001 соответственно), при этом пациенты с генотипом СТ занимали промежуточное положение и достоверно отличались от пациентов с генотипом СС (1,54 ± 0,23 vs 1,09 ± 0,15, р = 0,001) [рисунок 1]. Можно предположить, что повышение концентрации дигоксина в крови пациентов было главной причиной, приводящей к развитию гликозидной интоксикации.
Генотип ТТ достоверно чаще встречался в группе пациентов, у которых развивалась гликозидная интоксикация, по сравнению с группой без таковой (61% vs. 16%, р<<0,05). Это позволяет нам говорить об ассоциации между полиморфным маркером С3435Т и развитием гликозидной интоксикации, т.е. генотип ТТ и аллель Т являются генетическими факторами риска (OR равен 8,67 и 3,90 при доверительных интервалах 3,18-23,60 и 1,90-8,00, соответственно), предрасполагающими к развитию гликозидной интоксикации при приеме дигоксина у больных с ПФМА.
Рисунок 1.
Зависимость средней равновесной концентрации дигоксина в плазме крови от генотипа пациента по полиморфному маркеру С3435Т гена MDR1
Нами была изучена возможность использования выявления носительства генотипа ТТ для прогнозирования развития симптомов гликозидной интоксикации. Чувствительность выявления генотипа ТТ для прогнозирования развития симптомов гликозидной интоксикации составила 30%, специфичность – 94%. Прогностическая ценность (PPV) положительного результата в случае выявления генотипа ТТ составила 42%. Прогностическая ценность отрицательного результата (NPV) в случае выявления генотипов СС и CТ составила 80%.
Таким образом, в нашем исследовании, у больных с генотипом ТТ чаще возникали симптомы гликозидной интоксикации, кроме того именно у этой группы пациентов регистрировались более высокие концентрации дигоксина в плазме крови, по сравнению с пациентами с генотипами СС и СТ.
Связь между концентрацией дигоксина в плазме крови и возникновением симптомов гликозидной интоксикации очевидна и доказана в мультицентровом исследовании DIG. Полученные нами результаты можно объяснить снижением у пациентов с генотипом ТТ количества гликопротеина Р в клеточных мембранах, что является следствием снижения стабильности и, как следствие, срока жизни мРНК. А это, в свою очередь, приводит к тому, что дигоксин плохо выводится почками и накапливается в кровотоке. Результаты нашего исследования хорошо согласуются с данными ряда авторов [Hoffmeyer et al., 2000; Kurata et al., 2002; Verstuyft et al., 2003], которые, анализируя фармакокинетику дигоксина после его однократного приема в исследованиях у здоровых добровольцев, показали, что максимальная концентрация дигоксина в плазме крови лиц с генотипом ТТ достоверно выше по сравнению с индивидуумами, имеющим генотип СС. В отличие от перечисленных исследований, в нашей работе участвовали пациенты, длительно применяющие дигоксин. Объем нашей клинической выборки позволил включить довольно небольшое число пациентов с выявленными симптомами гликозидной интоксикации, мы не изучали другие широко распространенные полиморфные маркеры гена MDR1, кроме того, концентрация дигоксина в плазме крови определялась не всем пациентам. Тем не менее, наши данные позволяют выдвинуть предположение о необходимости назначать дигоксин пациентам с генотипом ТТ в более низкой дозе (0,125 мг/сутки) и корректировать ее под контролем данных терапевтического лекарственного мониторинга. Для подтверждения этого предположения необходимо проведение клинических исследований, в которых сравнивались бы эффективность и безопасность дигоксина при его назначении в средней терапевтической дозе (0,25 мг/сутки) с учетом генотипа по полиморфному маркеру С3435Т гена MDR1.
2. Межэтнические различия в частотах аллелей и генотипов полиморфного маркера С1236Т гена MDR1.
Мы изучили частоты аллелей и генотипов полиморфного маркера С1236Т гена MDR1 в случайных выборках из четырех этнических групп: чукчей, эвенов, русских и казахов. Данные по частотам аллелей и генотипов полиморфного маркера С1236Т гена MDR1, приведены на рисунках 2 и 3, а также в таблице 4.
Частоты генотипов данного полиморфного маркера не различались во всех изученных группах. Частоты аллелей различались между коренным (чукчи) и некоренным (русские) населением Чукотского АО, а также между русскими и казахами, причем эти различия были на грани статистической достоверности.
Таблица 4.
Различия в частотах аллелей и генотипов полиморфного маркера С1236Т гена MDR1 между изученными выборками
| Русские | Чукчи | Эвены | |||||
| 2 | р | 2 | р | 2 | р | ||
| Чукчи | генотипы | 4,261 | 0,042 | ||||
| аллели | 5,802 | 0,055 | |||||
| Эвены | генотипы | 0,826 | 0,345 | 0,402 | 0,496 | ||
| аллели | 1,100 | 0,577 | 2,093 | 0,351 | |||
| Казахи | генотипы | 4,962 | 0,029 | 0,008 | 0,915 | 0,440 | 0,493 |
| аллели | 5,384 | 0,068 | 0,351 | 0,839 | 1,197 | 0,550 | |
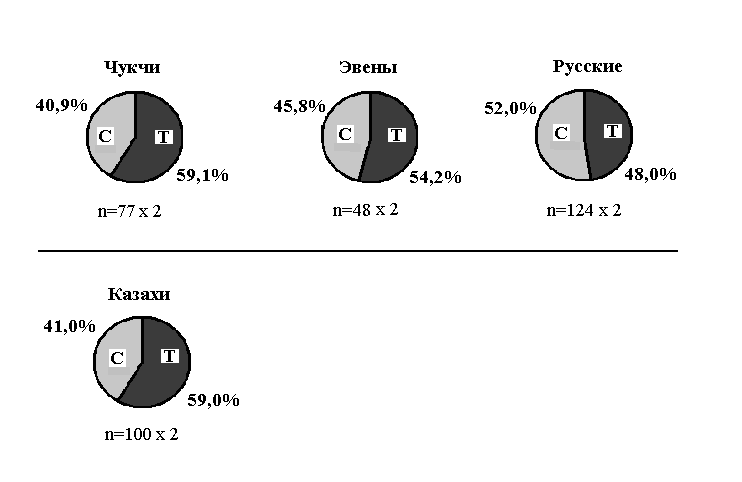
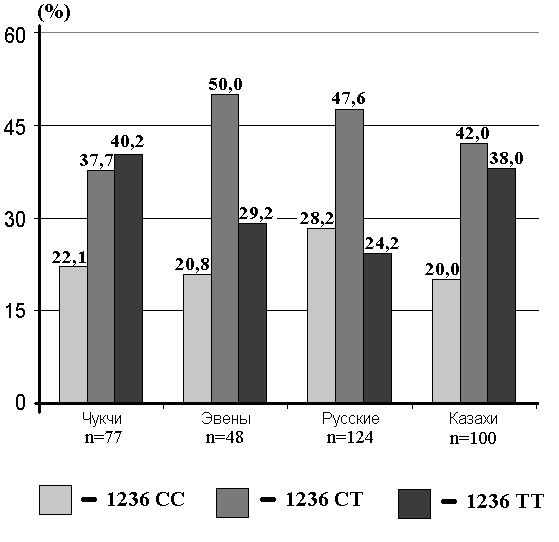
Рисунок 3
Частоты генотипов полиморфного маркера С1236Т гена MDR1 в изученных выборках
Полученные результаты можно объяснить следующим. Поскольку полиморфный маркер С1236Т, согласно нашим результатам, не влияет на эффективность «работы» гликопротеина Р, можно предположить, что носительство того или иного генотипа никак не отражается на приспособительных способностях индивида.
Чукчи с эвенами принадлежат к монголоидной расе. Русские же являются европеоидами. Казахи представляют собой смешанный монголоидно-европеоидный этнос. Именно этим фактом можно объяснить различия в частотах аллелей данного полиморфного маркера.
3. Межэтнические различия частот аллелей и генотипов полиморфного маркера С3435Т гена MDR1.
Сравнение частот аллелей и генотипов полиморфного маркера С3435Т гена MDR1 дало несколько иные результаты, чем в случае полиморфного маркера С1236Т. Данные приведены в таблице 5 и рисунках 4 и 5.
Наблюдаемые распределения частот аллелей носят практические зеркальный характер. Значительные различия наблюдаются у коренных жителей Чукотки по сравнению с русскими и с казахами. Соответственно, различий между русскими и казахами не наблюдается.
Частота аллеля Т практически в полтора раза выше у коренных жителей Чукотки (63,6%) по сравнению с русскими (49,6%) и с казахами (44,0%).
Также и генотип ТТ встречается у них почти в два раза чаще (42,4%), чем у русских (26,6%) и у казахов (25,0%).
Таблица 5.
Различия в частотах аллелей и генотипов полиморфного маркера С3435Т гена MDR1 между изученными выборками
| Русские | Чукчи | Эвены | |||||
| 2 | р | 2 | р | 2 | р | ||
| Чукчи | генотипы | 4,609 | 0,032 | ||||
| аллели | 5,048 | 0,080 | |||||
| Эвены | генотипы | 8,438 | 0,004 | 0,866 | 0,316 | ||
| аллели | 8,971 | 0,011 | 3,010 | 0,222 | |||
| Казахи | генотипы | 1,178 | 0,281 | 9,435 | 0,002 | 13,670 | 0,0002 |
| аллели | 2,487 | 0,288 | 8,259 | 0,016 | 14,063 | 0,001 | |
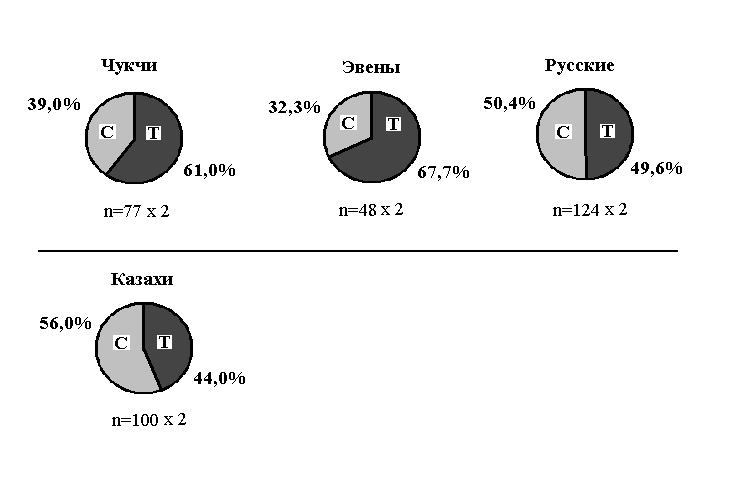
С популяционной точки зрения этот феномен можно объяснить, по всей видимости, тем, что условия жизни (распространенные инфекции, климат, водный режим, температурный режим, инсоляция и пр.) на территориях проживания русских и казахов схожи в большей степени, чем на Чукотке. Вероятно условия, в которых на протяжении многих поколений выживали коренные народы Крайнего Севера, настолько экстремальны, что происходил отбор по иным признакам, чем в более мягком климате.
Для более детального объяснения данного феномена необходимо дальнейшее изучение частот аллелей и генотипов полиморфного маркера С3435Т гена MDR1 в различных этнических группах.
Почти двукратное преобладание генотипа ТТ по полиморфному маркеру С3435Т гена MDR1 среди коренного населения Чукотского АО по сравнению с русскими и казахами позволяет предположить, что риск развития симптомов гликозидной интоксикации при приеме дигоксина у чукчей и эвенов значительно выше, чем у русских с казахами, что необходимо учитывать при составлении региональных рекомендаций по использованию данного ЛС.
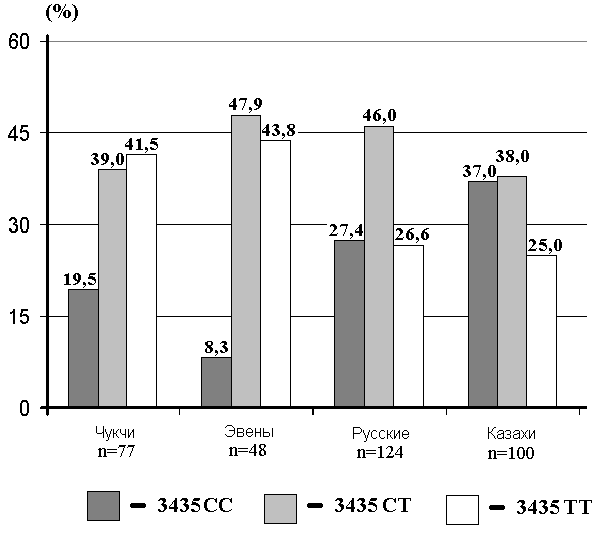
Рисунок 5
Частоты генотипов полиморфного маркера С3435Т гена MDR1 в изученных выборках
ВЫВОДЫ
- Обнаружена ассоциация полиморфного маркера С3435Т гена MDR1 с возникновением симптомов гликозидной интоксикации при приеме дигоксина у больных с ПФМА; генотип ТТ и аллель Т являются генетическими факторами риска (OR равен 8,67 и 3,90 при доверительных интервалах 3,18-23,60 и 1,90-8,00, соответственно).
- Прогностическая ценность генотипирования по полиморфному маркеру С3435Т гена MDR1 для прогнозирования гликозидной интоксикации составила 42% для положительного результата в случае выявления генотипа ТТ и 80% для отрицательного результата в случае выявления генотипов СС или CТ.
- Полиморфный маркер С3435Т гена MDR1 ассоциирован с повышением уровня равновесной концентрации дигоксина в крови; концентрация дигоксина достоверно выше у пациентов с генотипом ТТ по сравнению с пациентами, имеющими генотипы СС и СТ.
- Межэтнические различия в частотах аллелей полиморфного маркера С1236Т гена MDR1 наблюдались между казахами и русскими и между русскими и чукчами; различий в частотах генотипов по данному полиморфному маркеру в изученных группах не наблюдалось.
- Частоты аллелей и генотипов полиморфного маркера С3435Т гена MDR1 не различались между русскими и казахами, но существенно различались между русскими и коренным населением Чукотского АО, а также между казахами и коренным населением Чукотского АО.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ.
- Сычев Д.А., Игнатьев И.В., Раменская Г.В., Колхир С.В., Кукес В.Г. Значение полиморфизма гена MDR1, кодирующего гликопротеин-Р, для индивидуализации фармакотерапии. // Клиническая фармакология и терапия. –2005. -т.14. №1. –с.92-96.
- Игнатьев И.В., Сычев Д.А., Андреев Д.А., Жукова Э.Э., Колхир С.В., Кукес В.Г. Ассоциация полиморфного маркера С3435Т гена MDR1, кодирующего гликопротеин-Р, с развитием симптомов дигиталисной интоксикации и повышением концентрации дигоксина в плазме крови пациентов с постоянной формой мерцательной аритмии. // Медицинская генетика. – 2005. – т.4. №12. – с.568-572.
- Сычев Д.А., Игнатьев И.В., Андреев Д.А., Пошукаева Л.Г., Колхир П.В., Жукова Э.Э., Кукес В.Г. Значение фармакогенетических исследований гликопротеина-Р для индивидуализации фармакотерапии дигоксином: новый подход к старой проблеме. // Российский кардиологический журнал. -2006. №4 (60).- с. 64- 68.
- Сычев Д.А., Андреев Д.А., Игнатьев И.В., Жукова Э.Э., Суслов Л.С., Семенов А.В., Кукес В.Г. Влияние генетического полиморфизма гликопротеина-Р (MDR1) на уровень дигоксина в плазме крови больных хронической сердечной недостаточности и постоянной формой мерцательной аритмии. // V ежегодная конференция общества специалистов по сердечной недостаточности «Сердечная недостаточность 2004». Материалы докладов. – 2004. – с.33.
- Сычев Д.А., Андреев Д.А., Игнатьев И.В., Жукова Э.Э., Суслов Л.С., Семенов А.В., Кукес В.Г. Уровень дигоксина в плазме крови у больных постоянной формой мерцательной аритмии в зависимости от носительства полиморфного аллеля гена гликопротеина-Р (MDR1) C3435T: результаты фармакогенетического исследования. // XII российский национальный конгресс «Человек и лекарство». Материалы докладов. – 2005. – с.256.
- Кукес В.Г., Сычев Д.А., Раменская Г.В., Игнатьев И.В., Казаков Р.Е. Показания для использования генотипирования пациентов по ферментам биотрансформации и транспортерам при проведении клинических исследований новых лекарственных средств. // Материалы II Всероссийского съезда фармацевтических работников (Сочи, 5-7 июня 2005). – Сочи, 2005. – с. 93.
- Сычев Д.А., Игнатьев И.В., Андреев Д.А., Жукова Э.Э., Пошукаева Л.Г., Кукес В.Г. Роль полиморфного маркера С3435Т гена MDR1 в прогнозировании развития гликозидной интоксикации у больных постоянной формой мерцательной аритмии, длительно принимающих дигоксин. // IV международный конгресс. Доказательная медицина – основа современного здравоохранения. Материалы докладов. – 2005. – с.250-251.
- Игнатьев И.В., Коман И.Э., Сычев Д.А., Казаков Р.Е., Фалынскова И.Н., Кукес В.Г. Сравнительный анализ распределения частот генотипов полиморфного маркера С3435Т гена MDR1, кодирующего транспортер лекарственных средств гликопротеин-Р, в трех этнических группах чукотского АО. // V международная конференция «Клинические исследования лекарственных средств». Материалы конференции. – 2005. – с.82-83.
- Сычев Д.А., Игнатьев И.В., Андреев Д.А., Жукова Э.Э., Пошукаева Л.Г., Кукес В.Г. Носительство полиморфного маркера С3435Т гена MDR1 как фактор риска развития гликозидной интоксикации у больных хронической недостаточностью, длительно принимающих дигоксин. // VI ежегодная конференция общества специалистов по сердечной недостаточности «Сердечная недостаточность 2005» Материалы докладов. – 2005. – с.9-10.
- Сычев Д.А., Игнатьев И.В., Кукес В.Г. Значение генетических исследований для повышения эффективности и безопасности фармакотерапии кардиотропными лекарственными средствами. // Материалы научной программы XII Международной специализированной выставки «Аптека 2005» (Москва, 25-28 октября 2005). – 2005. – с. 4.
Список сокращений
ХСН – хроническая сердечная недостаточность
ПФМА – постоянная форма мерцательной аритмии
ЛС – лекарственное средство
НЛР – нежелательные лекарственные реакции
СГИ – симптомы гликозидной интоксикации («+» – наличие, «-» – отсутствие)
ПЦР – полимеразная цепная реакция
ПДРФ – полиморфизм длин рестриктазных фрагментов
п.н. – пара нуклеотидов – мера длины фрагмента двунитевой ДНК

