Разработка mini-mu системы для эффективной интеграции и амплификации генетического материала в хромосому бактерии e. coli в отсутствие селективного маркера.
На правах рукописи
Саврасова Екатерина Алексеевна
Разработка mini-Mu системы для эффективной интеграции и амплификации генетического материала в хромосому бактерии
E. coli в отсутствие селективного маркера.
03.00.03 - Молекулярная биология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата биологических наук
- Москва 2007 -
Работа выполнена в лаборатории №3 Закрытого Акционерного общества «Научно-исследовательский институт Аджиномото-Генетика» (ЗАО «АГРИ»).
Научный руководитель:
доктор биологических наук В.З. Ахвердян
Официальные оппоненты:
доктор биологических наук, профессор Р.С. Шакулов
ФГУП ГосНИИгенетика
кандидат биологических наук, Г.И. Каратаев
старший научный сотрудник
НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи РАМН
Ведущая организация: Институт общей генетики РАН
Защита диссертации состоится «___» ________ 2007 года в 1400 на заседании Диссертационного совета Д 217.013.01 при ФГУП «Государственный научно-исследовательский институт генетики и селекции промышленных микроорганизмов» по адресу: 117545, г. Москва, 1-й Дорожный проезд, д. 1.
С диссертацией можно ознакомиться в библиотеке ФГУП «ГосНИИгенетика»
Автореферат разослан «___» ________ 2007 г.
Ученый секретарь
Диссертационного совета,
кандидат биологических наук Г.Г. Заиграева
Общая характеристика работы
Актуальность проблемы. При конструировании штаммов-продуцентов различных биологически активных веществ, в частности аминокислот, широко используется амплификация целевых генов в составе плазмид. Данный подход имеет ряд недостатков, связанных с последующим использованием плазмидных штаммов в производстве: законодательные ограничения; потенциальная нестабильность плазмидных штаммов при росте в неселективных условиях; сложность создания больших групп независимо экспрессирующихся генов в составе одного вектора.
В настоящее время предпочтительным является использование бесплазмидных штаммов-продуцентов. При конструировании таких штаммов на первоначальном этапе осуществляется создание в составе плазмид интегративных кассет, содержащих целевые гены или опероны биосинтеза с оптимизированным уровнем экспрессии, затем проводится интеграция данных кассет в бактериальную хромосому с использованием различных механизмов рекомбинации. Интеграция генетического материала возможна по механизму общей рекомбинации бактериальной клетки, при условии наличия достаточно протяженной области фланговой гомологии, а также по механизму сайт-специфической рекомбинации, например, бактериофага (Datsenko K.A. et al., 2000). Другим подходом является использование свойств транспозирующихся элементов.
Транспозоны являются превосходными и широко используемыми генетическими инструментариями. К настоящему времени разработано много различных типов специализированных производных транспозонов. Наиболее широко используемыми являются конструкции, полученные на основе элементов Tn5, Tn10 и бактериофага Mu, также используются конструкции, основанные на элементах Tn3 и. Транспозоны разнообразны по своей природе и свойствам, среди них наиболее хорошо изученным является фаг-транспозон Mu. На основе данного элемента были разработаны системы для получения транскрипционных и трансляционных фьюзов, клонирования in vivo, картирования хромосомы (Groisman E.A. et al., 1984; Casadaban M. J. et al., 1986; Lawes M. et al., 1995).
Разработка нового генетического инструментария, использующего транспозиционные свойтва фага-транспозона Mu, позволяющего эффективно интегрировать генетический материал в хромосому E. coli в отсутствие антибиотических маркеров в составе mini-Mu векторов, является актуальной и практически значимой для биотехнологии, поскольку в настоящее время предъявляются повышенные требования к промышленным штаммам-продуцентам, одним из которых является отсутствие каких-либо антибиотических маркеров в хромосоме штаммов.
Цели и задачи работы. Диссертационная работа посвящена разработке эффективной генетической системы на основе фага-транспозона Mu и ее применению для конструирования штаммов-продуцентов различных аминокислот.
В ходе работы решались следующие задачи:
- Сравнительная оценка эффективности транспозиции транспозонов: Tn5, mini-Tn10, MD4041 и MD4041-thrA*BC.
- Оценка возможности использования выбранного транспозона для прикладных задач. Конструирование модельного штамма-продуцента треонина с использованием транспозонов MD4041-thrA*BC. Проверка характеристик полученных штаммов: стабильность продукции и число копий mini-Mu кассет.
- Конструирование на основе элемента mini-Mu MD4041 векторов, содержащих антибиотический маркер, обеспечивающих как эффективную интеграцию и амплификацию генов, так и стабильность полученных штаммов.
- Создание на основе mini-Mu MD4041 новой линии интегративных векторов (малокопийных, безмаркерных), необходимых для решения ряда задач при конструировании штаммов-продуцентов, соответствующих повышенным требованиям.
- Оценка эффективности использования элементов генетической системы в неселективных условиях.
- Применение данной системы при конструировании бесплазмидного безмаркерного штамма-продуцента валина.
Научная новизна и практическая ценность работы. Разработана генетическая система для эффективной интеграции и амплификации генетического материала в хромосому E. coli в отсутствие антибиотического маркера на основе фага-транспозона Mu. Данная система является удобным генно-инженерным инструментарием, прикладным назначением которого является конструирование бесплазмидных штаммов-продуцентов биологически активных веществ на основе бактерии E. coli.
Осуществлено конструирование новых линий интегративных векторов, несодержащих антибиотический маркер внутри mini-Mu, и показана эффективность их использования при интеграции и последующей амплификации. Осуществлено клонирование ряда генов центрального метаболизма и оперонов биосинтеза различных аминокислот, проведено конструирование двух линии интегративных векторов, которые нашли непосредственное применение при создании ряда штаммов-продуцентов.
Разработанная система, в частности, малокопийные безмаркерные mini-Mu векторы были успешно использованы в работах НИИ «Аджиномото - Генетика» при конструировании высокопродуктивных штаммов-продуцентов различных аминокислот.
Публикации и апробация работы. По теме диссертации опубликовано 2 печатных работы в отечественном журнале, два тезисных сообщения в материалах научных конференций и три патента. Материалы диссертации докладывались на Смотрах-конкурсах работ сотрудников ЗАО «АГРИ» в июне 2004 и июне 2005 года. Диссертационная работа была апробирована на совместном семинаре ЗАО "АГРИ" и секции по молекулярной биологии Ученого Совета ФГУП ГосНИИгенетика 12 апреля 2007 года.
Структура и объем работы. Диссертация состоит из 6 разделов: «Введение», «Обзор литературы», «Материалы и методы», «Результаты и обсуждение», «Выводы» и «Список цитируемой литературы». Работа изложена на 158 страницах, включая 53 рисунка и 23 таблицы. Список цитируемой литературы содержит 215 источников, в том числе 5 на русском языке.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
1. Сравнительная оценка эффективности транспозиции транспозонов Tn5, mini-Tn10, mini-Mu (MD4041), MD4041-thrA*BC. Высокоэффективная транспозиция вектора mini-Mu (MD4041).
На первом этапе данной работы была поставлена задача сравнения эффективности применения широко используемых транспозонов. Для сравнительной оценки эффективности транспозиции были взяты транспозоны Tn5, mini-Tn10 и mini-Mu (MD4041). Также был сконструирован ряд производных транспозона MD4041, содержащих в своем составе гены треонинового оперона thrA*BC с различной локализацией и ориентацией инсерции внутри mini-Mu, которые были проверены на эффективность использования. Данная группа транспозонов была названа MD4041-thrA*BC.
1.1 Оценка эффективности транспозиции транспозонов.
Перечисленные выше транспозоны были проверены на предмет эффективности транспозиции: Tn5, mini-Tn10, mini-Mu (MD4041) и MD4041-thrA*BC. Была осуществлена транспозиция данных транспозонов в хромосому штамма E. coli C600. Данный эксперимент был проведен при двух температурах 30°C и 37°C. Результаты экспериментов по сравненительной оценке эффективности транспозиции приведены в таблице 1.
Таблица 1. Эффективность транспозиции Tn5, mini-Tn10, mini-Mu (MD4041) и MD4041-thrA*BC в хромосому штамма E. coli С600.
| Транспозоны | Наличие термо- чувствительных генов | Эффективность транспозиции при температуре | Отношение эффективности транспозиции 37°C/30°C | |
| 30°C | 37°C | |||
| Tn5 | - | 10-5 – 10-6 | 10-5 – 10-6 | 1 |
| mini-Tn10 | - | 10-4 – 10-5 | 10-4 – 10-5 | 1 |
| mini-Mu(MD4041) | cts62 | 10-5 – 10-6 | 10-7 – 10-8 | 10-2 |
| MD4041- thrA*BC | cts62 | 10-5 – 10-6 | 10-7 – 10-8 | 10-2 |
Из полученных данных видно, что при температуре 30°C эффективность транспозиции Tn5, mini-Mu (MD4041) и MD4041-thrA*BC была одинакового порядка 10–5 – 10–6, в то время как для mini-Tn10 она была на порядок выше. При этом наблюдаемая эффективность транспозиции MD транспозонов при температуре 37°C ниже, чем у транспозонов Tn5 и mini-Tn10. Проведенное исследование показало, что эффективность транспозиции MD4041 и MD4041-thrA*BC снижается на два порядка при повышении температуры с 30°C до 37°C, тогда как у транспозонов Tn5 и mini-Tn10 она не меняется. Наблюдаемая зависимость эффективности транспозиции mini-Mu элементов от температуры объясняется тем, что в составе mini-Mu содержится термочувствительный ген с фага Mu, кодирующий синтез белка репрессора. Данный ген содержит мутацию cts62, приводящую к частичной инактивации репрессорного белка при температуре 37°C (Vogel J.L. et al., 1991).
Другим важным критерием эффективности процесса транспозиции является число копий транспозона, встроившихся в хромосому бактерии в течение одного акта транспозиции. Для ответа на данный вопрос была проведена работа по определению числа копий транспозонов в хромосомах штаммов, которые содержали встройки элементов Tn5, MD4041 и MD4041-thrA*BC. В данном эксперименте mini-Tn10 не рассматривался, поскольку он показал эффективность транспозиции на одном уровне с Tn5. Данные эксперименты проводились методом ДНК-гибридизации по Саузерну. Результаты экспериментов суммированы в таблице 2.
Таблица 2. Эффективность транспозиции Tn5, mini-Mu (MD4041), MD4041-thrA*BC и число копий этих элементов, встроенных в хромосому бактерий (30°C).
| Транспозоны | Эффективность транспозиции | Число копий |
| Tn5 | 10-5 – 10-6 | 1 - 2 |
| mini-Mu (MD4041) | 10-5 – 10-6 | >10 |
| MD4041-thrA*BC | 10-5 – 10-6 | >10 |
Как видно из данной таблицы, число копий Tn5 составило 1-2 единицы на хромосому, в то время как для MD4041 и MD4041-thrA*BC наблюдаемое число копий было больше 10 при равной эффективности транспозиции 10-5 – 10-6 при 30C. Таким образом, из полученных данных видно, что истинная эффективность транспозиции значительно больше у mini-Mu элементов, чем у Tn5.
1.2. Стабильность полученных штаммов.
Одним из важных свойств штаммов, содержащих инсерции транспозонов в хромосоме, является их стабильность, которую возможно оценить по выживаемости бактерий. Данное свойство является важным при дальнейшем использовании транспозонов в качестве генетического инструментария при конструировании штаммов бактерий с заданными характеристиками. С данной целью была проведена оценка стабильности штаммов E. coli, содержащих в хромосоме копии транспозонов Tn5, MD4041 и MD4041-thrA*BC, при температурах 30°С и 37°С. Результаты экспериментов приведены в таблице 3.
Таблица 3. Стабильность штаммов E. coli, содержащих элементы Tn5, mini-Tn10, mini-Mu (MD4041) и MD4041-thrA*BC, интегрированные в хромосому, при 30°С и 37°С.
| Штаммы бактерий E. coli | Выживаемость бактерий при температуре | Число копий транспозонов в хромосоме бактерии после выращивания при температуре | ||
| 30°С | 37°С | 30°С | 37°С | |
| C600::Tn5 | 1,0 | 1,0 | 1 | 1 |
| MG1655::Tn5 | 1,0 | 1,0 | 1 | 1 |
| C600::MD4041 | 1,0 | 10-4 | >10 | > 200 |
| C600::MD4041-thrA*BC | 1,0 | 10-4 | >10 | > 200 |
Как видно из данной таблицы, выживаемость штаммов, содержащих в хромосоме копии Tn5, не менялась в зависимости от температуры. Штаммы, содержащие в хромосоме копии mini-Mu элементов, вели себя иначе. При повышении температуры до 37°С титр бактерий падал на 4 порядка. Полученные в проведенном эксперименте результаты хорошо коррелировались с данными по числу копий транспозонов в хромосоме бактерий, выращенных при разных температурах. Данное исследование проводилось методом ДНК-гибридизации по Саузерну. При увеличении температуры до 37°С число копий Tn5 в хромосоме бактерии не изменилось и составило единицу. Напротив, число копий MD4041 и MD4041-thrA*BC возросло на несколько порядков при увеличении температуры, что отрицательно сказалось на выживаемости бактерий (табл.3). Данное явление связано с частичной температурной инактивацией репрессорного гена cts62 при температуре 37°С, приводящей к повышенной активности транспозиционных генов, входящих в состав данного транспозона, и, как следствие, к нерегулируемой репликативной транспозиции mini-Mu транспозонов в хромосомах штаммов, что приводит к гибели бактерий.
2. Конструирование продуцента треонина с использованием
интегративных векторов MD4041-thrA*BC.
Проведенные эксперименты показали, что полученные характеристики относительно транспозонов группы MD соответствуют возможности использования данных элементов в качестве генетического инструментария при конструировании штаммов бактерий с заданными характеристиками, а именно, с повышенной продуктивностью различных аминокислот.
Сконструированные интегративные mini-Mu векторы группы MD4041-thrA*BC, содержащие в своем составе гены треонинового оперона thrA*BC, были использованы для создания продуцента треонина на основе штамма бактерии E. coli TDH6 (BKПМ В-3420).
2. 1. Конструирование продуцента треонина.
Была осуществлена интеграция данных конструкций в хромосому штамма TDH6. Практически во всех случаях наблюдалась эффективная интеграция транспозона, что сопровождалось накоплением продукции треонина в ферментационной среде (30°С, 48 ч, среда с сахарозой). В результате проведенных экспериментов были отобраны штаммы 6,12,17,18, обладающие повышенным уровнем синтеза треонина (табл.4). Данные штаммы показали продукцию треонина в пределах от 12,0 до 19,5 г/л, а контрольный штамм TDH6 с плазмидой pVIC40 (содержащей гены треонинового оперона thrA*BC) - 20,4 г/л треонина. Число копий данной плазмиды, приходящееся на хромосому, равняется 10 (репликон RSF1010). Определение числа копий треонинового оперона в хромосомах данных штаммов методом ДНК-гибридизации по Саузерну показало, что оно составило больше 10 единиц (табл.4). Таким образом, посредством интеграции треонинового оперона thrA*BC в составе векторов группы MD4041-thrA*BC в хромосому штамма TDH6, были получены бесплазмидные штаммы, уровень продукции которых был сопоставим с уровнем плазмидного штамма В-3996(TDH6/pVIC40).
2.2. Проверка стабильности штаммов-продуцентов.
Была проверена стабильность продукции треонина и числа копий интегрированных кассет MD4041-thrA*BC у полученных штаммов. Для этого штаммы отобранной группы инкубировали при температуре 37°С и после рассева на чашках Петри был отобран ряд клонов, которые были обозначены цифрами с дополнительными индексами (например, производные штамма 12 были обозначены как 12-1,12-2,12-6). В отобранной группе штаммов была определена продукция треонина и число копий транспозона методом ДНК-гибридизации по Саузерну. Проведенные работы показали, что штаммы, полученные в данном эксперименте, ведут себя неодинаково. На основании полученных результатов штаммы были разделены на две группы по признаку увеличения или снижения продукции треонина (табл.4).
Таблица 4. Характеристика штаммов-продуцентов треонина, отобранных после инкубации при температуре 37°С.
| Штамм | Число интегрированных копий MD4041-thrA*BC | Треонин, г/л | |
| 17* 17-1 | >10 | 18.9 | |
| >10 | 19.5 | ||
| 18* 18-1 | >10 | 19.3 | |
| >10 | 21.5 | ||
| 6 * 6-0 | >10 | 16.5 | |
| 4 | 9.7 | ||
| 12* 12-1 12-2 12-6 | >10 | 17.4 | |
| >10 | 17.6 | ||
| 7 | 12.5 | ||
| 7 | 13.2 | ||
* Родительские штаммы не подвергали инкубации при 37°С.
Увеличение продукции треонина в первой группе штаммов (17,17-1,18,18-1) коррелировало с увеличением числа копий треонинового оперона в хромосоме бактерий. Результаты ДНК-гибридизации по Саузерну другой группы штаммов (6,6-0,12,12-1,12-2,12-6), в которой наблюдалось уменьшение продукции треонина, показали, что наблюдаемое явление связано с уменьшением числа копий треонинового оперона в хромосоме штаммов. В результате проведенных экспериментов был сделан вывод о том, что наблюдаемая нестабильность штаммов при температуре 37°С связана с экспрессией генов транспозазы, входящих в состав транспозона MD4041. Таким образом, полученные результаты свидетельствовали о необходимости контролирования процесса транспозиции в целях получения стабильных штаммов-продуцентов. Решению данной задачи был посвящен следующий раздел данной работы.
3. Конструирование на основе элемента mini-Mu MD4041 векторов, обеспечивающих эффективную интеграцию и амплификацию генов, а также стабильность полученных штаммов.
Задача контролирования процесса транспозиции может быть решена путем разделения функций, кодируемых транспозоном mini-Mu MD4041, на два отдельных модуля: интеграционный и транспозиционный. Интеграционный модуль (mini-Mu вектор) должен содержать минимальные сайты, необходимые для интеграции (attL- и attR-сайты фага Mu), а транспозиционный (плазмида, конторлирующая синтез транспозазы А и белка-активатора В) – функции необходимые для транспозиции.
Создание двухплазмидной системы было осуществлено в несколько этапов: 1) конструирование плазмиды – помощницы, заключающей в себе транспозиционный модуль; 2) конструирование различного вида mini-Mu векторов; 3) проверка эффективности использования разработанной системы.
3.1. Конструирование транспозиционного модуля.
Плазмида, используемая в качестве экзогенного источника транспозазы, не должна быть способна к независимой транспозиции, поэтому она не должна содержать оба att-сайта фага Mu. Для эффективной интеграции генов, находящихся под контролем сильного PR-промотора фага, который предполагалось использовать в составе интегративных векторов, необходимо присутствие на транспозазной плазмиде гена, кодирующего термочувствительный репрессор фага, cI857. Кроме того, транспозазная плазмида должна быть совместима по репликону с интегративным вектором mini-Mu (репликон рМВ1). В качестве подходящего вектора для транспозиционного модуля нами была выбрана плазмида pсI857, ранее полученная в нашей лаборатории. Плазмида pсI857 содержит термочувствительный репрессор фага cI857 на репликоне p15A (pACYC177), совместимом с pMB1. Конструирование транспозазной плазмиды pMH10 было осуществлено посредством клонирования транспозиционного модуля из плазмиды pMud4041 в вектор pсI857. Таким образом, полученная транспозазная плазмида-помощник pMH10 содержит attL-сайт, репрессорные гены cts62 и ner, гены А и В фага Mu, контролирующие синтез транспозазы и кофактора транспозиции, соответственно (рис.1). При наличии только одного из att сайтов транспозиция данного вектора не может осуществляться. При повышенной температуре 42С индуцируется экспрессия транспозазы A и белка активатора B, которые необходимы для транспозиции mini-Mu вектора.
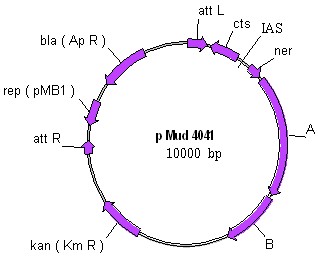
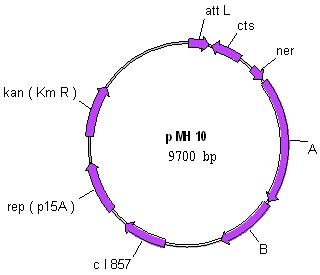
Рисунок 1.Схемы плазмид pMud4041 и рМН10.
3.2. Конструирование mini-Mu векторов, содержащих
антибиотический маркер.
Конструирование минимальных mini-Mu векторов было выполнено также на основе плазмиды рMud4041 путем удаления внутренней последовательности между attL- и attR-сайтами фага Mu. В результате проведенной работы были получены два вектора pM-cts-IAS и pM (рис.2). Вектор pM-cts-IAS содержит в своем составе attL- (445 п.н.) и attR- сайты (118 п.н.), репрессорный ген cts62, IAS-элемент и маркер антибиотической устойчивости к канамицину внутри mini-Mu. В экспериментах in vivo было показано, что IAS-элемент повышает эффективность транспозиции в 100 раз (Harshey R.M. et al., 1989). В ходе работы предполагалось проверить, окажет ли положительный эффект присутствие IAS-элемента в составе интегративного вектора на процесс транспозиции в условиях данной двухплазмидной системы. Другой вектор, pM, содержит только attL- и attR-сайты фага Mu, а также маркер устойчивости к канамицину (рис.2). Таким образом, были сконструированы минимальные mini-Mu векторы, которые способны осуществлять транспозицию только в присутствии плазмиды рМН10, несущей транспозазный модуль. Клонирование в данные векторы предполагалось осуществлять с заменой маркера антибиотической устойчивости, поскольку он совпадает с маркером транспозазной плазмиды pMH10.


3.3 Оценка эффективности интеграции векторов, содержащих антибиотический маркер.
Полученные векторы были проверены на способность к осуществлению интеграции. С этой целью в данные mini-Mu векторы pM и pM-cts-IAS было проведено клонирование генов треонинового thrA*BC и лейцинового оперонов leuA*BCD, находящихся под регуляцией собственных промоторов и PR- промотора фага. В результате проведенных работ были получены плазмиды: pMcts-thrA*BC-СmR, pM-thrA*BC-CmR, pMcts-PR-thrA*BC-CmR, pM-PR-thrA*BC-CmR, pMcts-PR-leuA*BCD-CmR и pM-PR-leuA*BCD-CmR. Данные конструкции были интегрированы с использованием транспозазной плазмиды pMH10 в модельные штаммы-продуценты треонина и лейцина в идентичных условиях по стандартной методике (Ахвердян В.З. и др., 2007). В качестве реципиента треонинового продуцента был использован штамм TDH6, а в качестве реципиента лейцинового продуцента - штамм С600. Была проведена оценка эффективности интеграции mini-Mu векторов среди бесплазмидных клонов на основании устойчивости к антибиотическому маркеру, находящемуся внутри mini-Mu. Полученные данные суммированы в таблице 5.
При использовании разработанной системы интеграции необходимо введение в реципиентный штамм двух плазмид, поэтому оценка эффективности интеграции проводилась следующим образом: “Эффективность интеграции mini-Mu” определена как отношение числа интегрантов среди проверенных клонов (по маркеру антибиотической устойчивости внутри mini-Mu или методом ДНК-гибридизации по Саузерну) к общему числу проверяемых клонов, выраженное в процентах. Проверка осуществлялась соответственно после этапов излечивания от обеих плазмид согласно стандартной методике.
Таблица 5. Зависимость эффективности интеграции mini-Mu с удаленными генами, кодирующими транспозазу (A) и активатор транспозиции (B), от присутствия репрессора cts62 и сайта ias, активирующего транспозицию в cis-положении.
| Вектор mini-Mu | Сохраненные сайты и гены Mu | Удалены гены Mu | Эффективность интеграции, % |
| MD4041-thrA*BC-KmR | attL cts62 ias ner A B attR | - | 10-5 |
| Mcts-thrA*BC-CmR | attL cts62 ias attR | ner, A, B | 2 |
| Mcts-PR-thrA*BC-CmR | attL cts62 ias attR | ner, A, B | 3 |
| Mcts-PR-leuA*BCD-CmR | attL cts62 ias attR | ner, A, B | 2 |
| M-thrA*BC -CmR | attL attR | cts62, ias, ner, A, B | 99 |
| M-PR-thrA*BC -CmR | attL attR | cts62, ias, ner, A, B | 98 |
| M-PR-leuA*BCD -CmR | attL attR | cts62, ias, ner, A, B | 100 |
Из данных таблицы 5 видно, что разделение модулей интеграции и транспозиции, а именно, использование двухплазмидной системы привело к значительному увеличению эффективности интеграции (на несколько порядков). Удаление из состава вектора репрессорного гена cts62 и IAS-элемента привело к увеличению эффективности интеграции в 33-50 раз. Полученная в данном эксперименте группа штаммов была проверена с использованием метода Саузерна путем гибридизации с меченой ДНК треонинового thrA*BC и лейцинового leuA*BCD оперонов для определения числа копий интегрированных генов. Результаты проведенных экспериментов суммированы в таблице 6 и на рисунке 3(а,б).
Таблица 6. Зависимость числа интегрированных копий mini-Mu элементов от присутствия репрессора cts62 и сайта ias, активирующего транспозицию в cis-положении.
| Вектор mini-Mu | Наличие в mini-Mu гена cts62 и сайта ias | Эффективность интеграции mini-Mu, в % | Число копий mini-Mu, интегрированных в хромосому бактерии |
| Mcts-thrA*BC -CmR | cts62 ias | 2 | 1 |
| Mcts-PR-thrA*BC-CmR | 3 | 1 | |
| Mcts-PR-leuA*BCD -СmR | 2 | 1 | |
| M-thrA*BC -CmR | - | 99 | 1 - 5 |
| M-PR-thrA*BC -CmR | 98 | 1 - 5 | |
| M-PR-leuA*BCD -CmR | 100 | 1 - 5 |
Из данных, приведенных в таблицах 5 и 6 видно, что присутствие в составе интегративного вектора IAS-элемента не оказывает положительного влияния при наличии репрессорного гена cts62, который отрицательно влияет не только на эффективность интеграции, но и на число копий транспозона, интегрированного в хромосому. При наличии репрессорного гена cts62 эффективность интеграции векторов составила 2-3%, а число копий mini-Mu кассет в хромосомах проверяемых штаммов равнялось единице (рис.3а). Удаление гена сts62 и IAS- элемента из состава вектора привело к увеличению числа копий mini-Mu (M-thrA*BC-CmR, M-PR-thrA*BC-CmR, M-PR-leuA*BCD-CmR), интегрированных в хромосому бактерии. Как показали проведенные эксперименты, количество интегрированных копий mini-Mu в хромосомах изучаемых штаммов варьировало от 1 до 5 единиц (рис.3б). Количество копий оценивали по числу полос на радиоавтографах и их интенсивности.
1 2 3 4 5 6 7 8 9 10 1 2 3 4 5 6 7 8 9 10 11
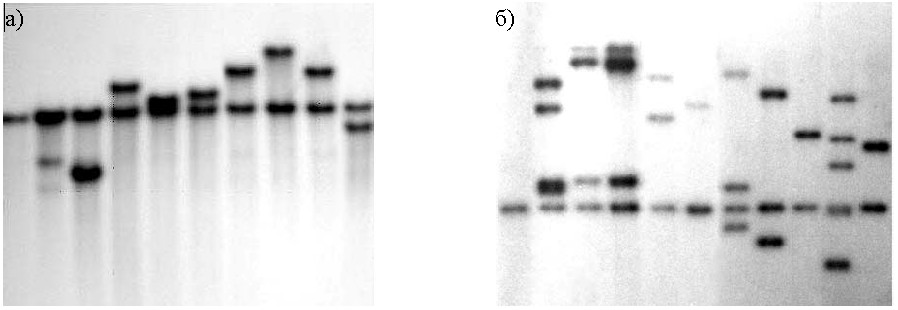
Рисунок 3. Результаты гибридизации по Саузерну: а) штаммы, содержащие копии треонинового оперона thrA*BC, интегрированного в составе вектора pM-cts-IAS: 1- контроль TDH6, 2-10- изучаемые штаммы (TDH6::Mcts-thrA*BC-CmR); б) штаммы, содержащие копии лейцинового оперона leuA*BCD, интегрированного в составе вектора pM: 1 - контроль С600, 2-11 - проверяемые штаммы (С600::M-PR-leuA*BCD-CmR).
Таким образом, разделение модулей интеграции и транспозиции элемента MD4041 привело к повышению эффективности интеграции mini-Mu векторов. Удаление из состава интегративного вектора репрессорного гена cts62 привело к увеличению эффективности процесса интеграции и достигло практически 100%.
Другим важным свойством разработанной двуплазмидной системы является возможность контролируемого увеличения числа копий mini-Mu вектора, интегрированного в хромосому бактерии, при использовании только транспозазной плазмиды. Для этой цели в полученные на предыдущем этапе штаммы-продуценты треонина и лейцина, содержащие в хромосоме интегрированные копии векторов mini-Mu двух видов, была введена транспозазная плазмида pMH10 и проведена температурная индукция синтеза транспозазы с данной плазмиды согласно стандартной методике. Число копий mini-Mu элементов в хромосоме полученных штаммов было определено методом ДНК-гибридизации по Саузерну. Результаты экспериментов суммированы в таблице 7.
Таблица 7. Зависимость увеличения числа итегрированных копий mini-Mu после повторной транспозиции с использованием плазмиды pMH10 от присутствия в составе mini-Mu вектора гена-репрессора cts62 и сайта ias, активирующего транспозицию в cis-положении.
| Вектор mini-Mu | Наличие в mini-Mu гена cts62 и сайта ias | Увеличение числа копий mini-Mu, интегрированного в хромосому | ||
| Интеграция | Амплификация | |||
| Первая | Вторая | |||
| Mcts-thrA*BC-CmR | cts62 ias | 1 | 2 | 3 |
| Mcts-PR-thrA*BC-CmR | 1 | 2 | 3 | |
| Mcts-PR-leuA*BCD-CmR | 1 | 2 | 3 | |
| M-thrA*BC-CmR | - | 4 | 7 | 12 |
| M-PR-thrA*BC-CmR | 4 | 7 | 10 | |
| M-PR-leuA*BCD-CmR | 4 | 7 | 10 | |
Из данных таблицы 7 видно, что амплификация с использованием транспозазной плазмиды привела к увеличению числа копий mini-Mu в хромосоме бактерий, причем увеличение наблюдалось в случаях двух видов векторов (рМ и pM-cts-IAS). При использовании интегративного вектора без репрессорного гена процесс амплификации происходил более эффективно, число интегрированных копий mini-Mu было увеличено с 4 до 7. Следует заметить, что процесс амплификации векторов группы pM-cts-IAS был мало эффективен. Число интегрированных в хромосому копий mini-Mu увеличилось с единицы до двух, причем амплификация наблюдалась только в менее 5% проверенных клонов, в остальных же число копий оставалось на исходном уровне.
Далее полученные таким образом штаммы были проверены на возможность применения второго цикла амплификации. Результаты проведенных экспериментов представлены в таблице 7. Из приведенных данных видно, что повторная амплификация также привела к увеличению исходного числа копий mini-Mu вектора в хромосоме реципиентных штаммов. Как и в первом цикле, эффективная амплификация наблюдалась у векторов, которые имеют только attL- и attR-сайты фага Mu (pM-thrA*BC-CmR, pM-PR-thrA*BC-CmR, pM-PR-leuA*BCD-CmR); копийность элементов возросла до 10-12 единиц. Следует отметить, что интегрированные после первого и второго этапа копии mini-Mu кассет сохранялись, локализация сайтов интеграции генов thrA*BC и leuA*BCD также не менялась; наблюдалось образование новых копий, что согласуется с репликативной моделью транспозиции фага Mu. Амплификация векторов группы pM-cts-IAS была также мало эффективна. Увеличение числа копий с 2 до 3 наблюдалось в менее чем 5% изученных клонов. На основании полученных в ходе проведенных экспериментов данных нами был сделан вывод о том, что более эффективный процесс интеграции и амплификации наблюдался при использовании векторов mini-Mu, содержащих только attL- и attR-сайты фага Mu (вектор рМ).
Следует отметить, что при создании штаммов-продуцентов увеличение числа копий определенных генов может быть нежелательно. В таких случаях можно рекомендовать использовать вектор pM-cts-IAS, обеспечивающий низкое число копий интегрированных генов.
3.4 Стабильность штаммов, содержащих в хромосоме интегрированные mini-Mu кассеты.
Важной характеристикой полученных штаммов-продуцентов является стабильность продукции. Проведенная оценка стабильности штаммов-продуцентов треонина и лейцина, полученных посредством интеграции и амплификации соответствующих оперонов биосинтеза (thrA*BC и leuA*BCD), после инкубации при повышенной температуре 37°С и семи последовательных пересевов в течение месяца показала отсутствие различий в продуктивности штаммов. Полученные штаммы поддерживали продуктивность на прежнем уровне, которая составляла 98-100% по отношению к продуктивности исходного штамма.
3.5 Зависимость утраты плазмид mini-Mu вектора и модуля транспозазы от наличия гена-репрессора Mu в составе
интегративного вектора.
Проведение работы с использованием двухплазмидной системы показало, что немаловажным критерием оценки эффективности применения системы является утрата плазмид после этапа интеграции, так как для дальнейшего анализа и работы отбираются только те клоны, в которых наблюдается утрата обеих плазмид. Была проведена робота по оценке утраты векторов mini-Mu и транспозазной плазмиды при проведении экспериментов по интеграции треонинового и лейцинового оперонов в хромосомы реципиентных штаммов. Полученные в результате проведенных экспериментов данные свидетельствуют о том, что удаление гена-репрессора Mu cts62 из состава интегративного вектора приводит к увеличению эффективности утраты обеих плазмид (mini-Mu вектора и pMH10) в 20-50 раз. Таким образом, при использовании векторов группы рМ, содержащих только attL- и attR-сайты фага Mu, эффективность утраты обоих плазмид разработанной системы стала практически 100%.
В результате проведенной работы по оценке эффективности интеграции и амплификации 2 групп векторов рМ и рМ-cts-IAS, стабильности полученных штаммов-продуцентов и на основании данных по эффективности утраты плазмид, был сделан вывод об эффективности использования данной системы для задач конструирования бесплазмидных штаммов-продуцентов.
4. Конструирование малокопийных интегративных векторов mini-Mu, не содержащих антибиотический маркер.
В настоящее время предъявляются повышенные требования к промышленным штамма-продуцентам, одним из которых является отсутствие антибиотических маркеров в хромосоме штаммов. Проведенные эксперименты показали, что разработанная mini-Mu система поддерживает эффективную интеграцию и амплификацию интегрированных генов в хромосому E. coli в составе векторов, содержащих антибиотический маркер внутри mini-Mu. Нами было сделано предположение, что полученные результаты свидетельствуют о возможности использования разработанной системы для интеграции генов в хромосому E. coli в отсутствие антибиотического маркера в составе mini-Mu вектора. С другой стороны, для обеспечения стабильности интегративных mini-Mu векторов, содержащих в своем составе гены, находящиеся под контролем сильного PR-промотора фага, необходимо использовать векторы с меньшей копийностью. Таким образом, возникла необходимость создания новой линии малокопийных интегративных mini-Mu векторов, в которых предполагалось отсутствие антибиотического маркера внутри mini-Mu. Данная задача была выполнена в несколько этапов. Оценку наличия интеграции в полученных в результате проведенных экспериментов штаммах предполагалось проводить несколькими методами: ДНК-гибридизацией по Саузерну, ПЦР, а также по уровню продукции аминокислоты.
4.1. Конструирование интегративных mini-Mu векторов pM16 и pM17.
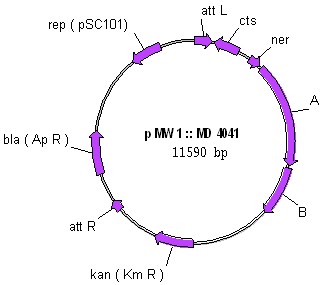
При конструировании новой линии интегративных mini-Mu векторов в качестве малокопийного репликона была использована производная плазмиды pMW119 – pMW1. Данная плазмида была получена из плазмиды pMW119 (репликон pSC101) путем удаления lac-области и полилинкера. Далее была осуществлена интеграция in vivo элемента mini-Mu MD4041 из бактериальной хромосомы штамма LE::MD4041 в вектор pMW1. В результате проведенной работы была получена рекомбинантная плазмида pMW1::MD4041 (рис.4), далее на основе которой были сконструированы интегративные векторы.
Было проведено удаление внутренней последовательности между att-сайтами фага Mu и встраивание двух тендемных копий терминатора транскрипции фага fd, полилинкера для клонирования генов, а также РR-промотора фага (вектор pM17). В результате проведенной работы было получено два вектора pM16 и pM17 (рис.5) для клонирования генов под собственной регуляцией, а также под контролем сильного РR-промотора фага (соответственно).
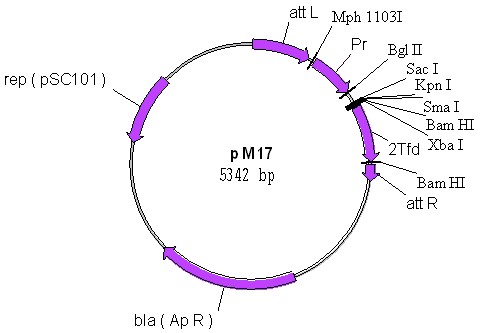

4.2. Определение структуры интегративного вектора рМ17.
Поскольку вектор pMW1::MD4041 был получен путем клонирования in vivo, необходимо было определить точное место встраивания mini-Mu на векторе рMW1. С этой целью было проведено определение нуклеотидной последовательности вектора pM17 с использованием в качестве праймеров олигонуклеотидов, комплементарных последовательности attL- и attR-сайтов фага Mu, а также векторной части молекулы. Проведенный анализ результатов определения последовательности нуклеотидов показал, что транспозиция mini-Mu с плазмиды pMud4041 в вектор рMW1 прошла в районе par-сайта и сопровождалась дупликацией последовательности из 5 п.н. (ggggt). Данная транспозиция является классической встройкой Mu в вектор на основании данных описанных в литературе (Casadaban M. et al., 1991). Дупликация 5 п.н. сайта-мишени подтверждает, что акт встраивания mini-Mu в вектор pMW1 является истинным транспозиционным событием. В векторе mini-Mu расположен следующим образом: attL-сайт фага Mu находится перед геном repA на расстоянии 490 п.н., attR-сайт на расстоянии 470 п.н. от начала гена ApR. Эти результаты соответствуют данным, полученным ранее, на основании рестрикционного анализа. В результате секвенирования вектора pMW1 показано, что инверсии и делеции в векторной части молекулы отсутствуют.
5. Эффективность разработанной mini-Mu системы
в неселективных условиях.
В данном разделе суммированы результаты экспериментов по оценке эффективности интеграции как многокопийных, так и малокопийных mini-Mu векторов, не содержащих антибиотический маркер. Как было сказано ранее, оценку наличия интеграции при использовании безмаркерных интегративных векторов mini-Mu предполагалось проводить несколькими методами: ДНК- гибридизацией по Саузерну, ПЦР, а также по уровню продукции аминокислоты.
5.1. Изучение эффективности интеграции генов биосинтеза аминокислот.
В многокопийном интегративном векторе pM было осуществлено клонирование оперонов биосинтеза различных аминокислот: треонина, изолейцина, валина и лейцина. Были сконструированы интегративные векторы pMРR-thrA*BC, pMРR-ilvG*MEDA*YC, pMРR-ilG*MEDА, pMРR-leuA*BCD и проведена интеграция данных конструкций в хромосому штамма E. coli C600. Полученные в результате экспериментов клоны после этапа излечивания от плазмид были проверены на наличие интеграции методом ДНК-гибридизации по Саузерну. В каждом случае было проверено по 20 клонов. Результаты оценки эффективности интеграции в проведенных экспериментах суммированы в таблице 8.
Таблица 8. Эффективность mini-Mu интеграции различных генов в хромосому штамма E. coli С600.
| Гены, клонированные в mini-Mu векторах | Эффективность интеграции, в % |
| PR-thrA*BC | 95 - 100 |
| PR-ilvG*MEDA*YC | 95 |
| PR-ilvG*MEDА | 85 |
| PR-leuA*BCD | 95 |
Из приведенных в таблице 8 данных видно, что во всех случаях наблюдался высокий процент интеграции от 85 до 100%. Полученные данные показывают эффективность использования разработанной системы в целом и интегративных векторов mini-Mu группы рМ, несодержащих антибиотический маркер, в частности.
5.2. Влияние терминации транскрипции внутри mini-Mu вектора
на эффективность интеграции.
Наши исследования также показали важность наличия эффективного терминатора транскрипции внутри mini-Mu вектора для инеграции генов в бактериальную хромосому E. coli. Результаты, подтверждающие данное влияние, были получены на основании экспериментов по интеграции валинового, треонинового оперонов в составе многокопийных и малокопийных интегративных векторов, содержащих и несодержащих эффективные терминаторы транскрипции, в качестве которых были выбраны двойной терминатор фага fd и терминатор изолейцин-валинового оперона Tilv. Были сконструированы интегративные векторы: pMPR-ilvG*MED, pMPR-ilvG*MED-2Tfd, pMPR-ilvG*MED-Tilv (репликон рМВ1); pM-att-thrA*BC, рM-att-thrA*BC-2Tfd (репликон рSC101). Интеграция данных mini-Mu векторов в хромосому штамма E. coli С600 была осуществлена по стандартной методике. Полученные клоны были проверены на наличие интеграции методом ДНК- гибридизации по Саузерну и ПЦР методом. В каждом случае было проверено по 20 клонов. Результаты экспериментов суммированы в таблице 9.
Таблица 9. Влияние присутствия эффективного терминатора транскрипции внутри mini-Mu вектора на интеграцию генов в хромосому E. coli.
| Гены, клонированные в mini-Mu векторах | Эффективность интеграции, в % |
| PR-ilvG*MED | 2 |
| PR-ilvG*MED-2Tfd | 95 |
| PR-ilvG*MED-Tilv | 90 |
| -att-thrA*BC | 3 |
| -att-thrA*BC-2Tfd | 80 |
Как видно из таблицы 9, в отсутствие эффективного терминатора транскрипции эффективность интеграции валинового, треонинового оперонов низкая. Введение в данные конструкции двойного терминатора транскрипции фага fd или терминатора транскрипции изолейцин-валинового оперона Тilv повысило эффективность процесса интеграции до 80-95%.
Мы считаем, что причина данного повышения эффективности интеграции заключается в пространственном разрешении транспозиционного комплекса, являющегося обязательным промежуточным соединением в процессе транспозиции. В отсутствие эффективной терминации РНК-полимераза может вызывать пространственные ограничения при образовании транспозосомного комплекса, блокируя связывание транспозазы фага Mu с att-сайтами.
5.3. Эффективность интеграции в процессе первичной транспозиции.
Другой важной характеристикой эффективности процесса интеграции является количество копий интеграционной кассеты, встроившихся в бактериальную хромосому в течение одного цикла. С учетом данного критерия была проведена оценка эффективности интеграции следующей группы генов: треонинового оперона thrA*BC, валинового оперона ilvG*MEDА и лейцинового оперона leuA*BCD. Была осуществлена интеграция многокопийных mini-Mu векторов рМPR-thrA*BC, pMPR-ilvG*MEDА, pMРR-leuA*BCD в хромосому штамма E. coli C600. Полученные в результате экспериментов бесплазмидные клоны были проверены методом ДНК-гибридизации по Саузерну на наличие интеграции. Для каждого оперона было проверено по 100 независимо полученных бесплазмидных клонов. Результаты экспериментов суммированы в таблице 10.
Таблица 10. Эффективность интеграции mini-Mu векторов в хромосому E. coli.
| Гены, клонированные в mini-Mu векторах | Доля штаммов с различным числом копий интегрированных генов, в % от общего числа исследуемых штаммов | ||||
| 1 копия | 2 копии | 3 копии | 4 копии | 5 копий | |
| PR-thrA*BC | 17 | 23 | 35 | 15 | 10 |
| PR-ilvG*MEDА | 15 | 25 | 40 | 15 | 5 |
| PR-leuA*BCD | 20 | 25 | 33 | 15 | 7 |
Из приведенных в таблице 10 данных видно, что наиболее эффективно происходила интеграция 3 копий исследуемых интеграционных конструкций, что составило от 33 до 40% от общего числа проверяемых клонов. В 25% проверяемых клонов наблюдалось по две копии интегрированных генов. Эффективность встраивания одной копии составила от 15 до 20%. Интеграция более чем 3х копий наблюдалось с убывающей эффективностью: для четырех составило 15% и для пяти копий - от 5 до 10%. Хорошим показателем эффективности разработанной безмаркерной системы является то, что более 80% проверенных клонов содержит более одной копии интегрированных mini-Mu кассет.
5.4. Амплификация mini-Mu кассет, интегрированных
в хромосому бактерии.
Важным свойством разработанной системы является возможность дополнительной амплификации ранее интегрированных в бактериальную хромосому генов при помощи транспозазной плазмиды pMH10. С этой целью в реципиентные штаммы, в которые ранее были интегрированы гены треонинового оперона thrA*BC, валинового оперона ilvG*MED-2Tfd и гены PTS системы транспорта сахарозы scrKYABR, была введена плазмида pMH10 и осуществлена амплификация по стандартной методике. Оценка полученных штаммов на наличие амплификации проводилась методом ДНК-гибридизации по Саузерну. В данном исследовании было проведено два последовательных этапа амплификации и на каждом определялось число копий интеграционных mini-Mu кассет в хромосомах штаммов. Данные по эффективности амплификации генов приведены в таблице 11.
Таблица 11. Двухэтапная амплификация генов, интегрированных в хромосому E. coli, с использованием транспозазной плазмиды pMH10.
| Гены, клонированные в mini-Mu векторах | Амплификация генов, интегрированных в хромосому, с использованием плазмиды pMH10 | ||
| Интеграция | Первая амплификация | Вторая амплификация | |
| PR-thrA*BC | 4 | 7 | 10 |
| PR-ilvG*MED-2Tfd | 4 | 7 | 10 |
| scrKYABR | 1 | 3 | 5 |
Как видно из результатов, представленных в таблице 11, в хромосоме изучаемых штаммов исходное количество копий генов треонинового и валинового оперонов составляло 4 единицы. После проведения первого этапа амплификации копийность равнялась 7 в обоих случаях. Проведенная повторная амплификация позволила увеличить число интегрированных копий до 10. В случае генов PTS системы транспорта сахарозы после проведения первого цикла амплификации число копий равнялось 3. Проведенный затем второй этап амплификации позволил увеличить копийность до 5 единиц.
Значение присутствия в составе интегративного вектора эффективного терминатора транскрипции для процесса интеграции было уже показано ранее. Полученные данные позволяют сделать предположение о том, что его наличие также важно для процесса амплификации.
5.5. Эффективность интеграции малокопийных интегративных mini-Mu векторов.
Была проведена оценка эффективности интеграции безмаркерных малокопийных интегративных mini-Mu векторов. Результаты проведенных экспериментов представлены в данном разделе. В малокопийных интегративных векторах pM16, pM17 (рис.5) было осуществлено клонирование ряда генов гликолитического пути: pfkA (фосфофруктокиназа), pgi (фосфоглюкоизомераза), glk (глюкокиназа), eno (енолаза); генов oбщего метаболизма: ppc (фосфоенолпируваткарбоксилаза), ppc*, pntAB (трансгидрогеназа), aspA (аспартаза), aspC (аспартатаминотрансфераза), а также генов биосинтеза треонина thrA*B и гена asd (аспартат--полуальдегиддегидрогеназа). Полученные mini-Mu векторы были интегрированы в хромосому штамма E. coli MG1655 по стандартной методике. Затем была проведена оценка эффективности интеграции методом ПЦР среди полученных бесплазмидных клонов с использованием в качестве праймеров соответствующих пар олигонуклеотидов, комплементарных attL- или attR-сайтам фага Mu и определенной последовательности исследуемого гена. В каждом опыте была осуществлена проверка 20 клонов. Результаты экспериментов суммированы в таблице 12.
Таблица 12. Эффективность интеграции в хромосому E. coli генов, клонированных в малокопийных интегративных векторах.
| Гены, клонированные в mini-Mu векторах | Эффективность интеграции, в % |
| PR -pfkA | 90 - 100 |
| PR -pgi-pfkA | 85 |
| PR -glk | 75 |
| PR -eno | 90 - 100 |
| PR -ppc* | 75 |
| PR -ppc | 75 - 90 |
| pntAB | 80 - 90 |
| PR -asd | 75 |
| PR -aspC-asd | 95 - 100 |
| PR -ppc-aspA-pntAB | 80 - 100 |
| ppc-aspA-pntAB-att-thrA*B | 80 |
Из данных, приведенных в таблице 12 видно, что во всех случаях наблюдалась высокая эффективность интеграции - от 75 до 100% (данные получены на основании нескольких экспериментов). Таким образом, результаты проведенных экспериментов показывают, что разработанная mini-Mu интеграционная система обеспечивает эффективную интеграцию генетического материала в хромосому E. coli в отсутствие селективного маркера и последующую его амплификацию.
6. Использование разработанной интегративной mini-Mu системы для конструирования бесплазмидного штамма-продуцента валина,
не содержащего маркер антибиотической устойчивости.
При конструировании штамма-продуцента валина в качестве реципиента был использован штамм V-01. Данный штамм был получен на основе штамма дикого типа E. coli MG1655 путем последовательного внесения мутаций ilvG5 и ileS17 посредством Р1-трансдукции.
Штамм-продуцент валина V-4 был получен на основе штамма V-01 путем интеграции генов валиного оперона, находящихся под регуляцией PR-промотора фага, из состава плазмиды pMPR-ilvG*MED-2T fd в бактериальную хромосому штамма V-01 и последующими несколькими этапами амплификации данного оперона при помощи транспозазной плазмиды pMH10.
На первом этапе конструирования была осуществлена интеграция mini-Mu вектора pMPR-ilvG*MED-2Tfd в хромосому реципиентного штамма V-01. Среди полученной группы штаммов был отобран лучший V-2 на основании результатов ферментации в пробирках (рис. 6). Было проведено определение числа копий mini-Mu кассет в хромосоме данного штамма методом ДНК-гибридизации по Саузерну. Результаты гибридизации показали, что в хромосоме штамма V-2, полученного после первого этапа интеграции, содержалось 4 копии валинового оперона (рис.7). Количество интегрированных копий mini-Mu определяли по числу полос на радиоавтогафе и их интенсивности.
Далее при использовании транспозазной плазмиды рМН10 было проведено два последовательных этапа амплификации mini-Mu кассет pMPR-ilvG*MED-2Tfd в хромосоме данного штамма V-2. На основании данных по продуктивности полученных штаммов в условиях пробирочной ферментации были отобраны штаммы V-3 и V-4, обладающие повышенным уровнем синтеза валина (рис. 6). В полученных штаммах было проведено определение числа копий валинового оперона методом ДНК-гибридизации по Саузерну. Как показали полученные результаты, в хромосоме штамма V-3 содержалось 7 копий валинового оперона, а в хромосоме штамма V-4 - 10 копий валинового оперона (рис. 7).

Этапы 0 1 2 3
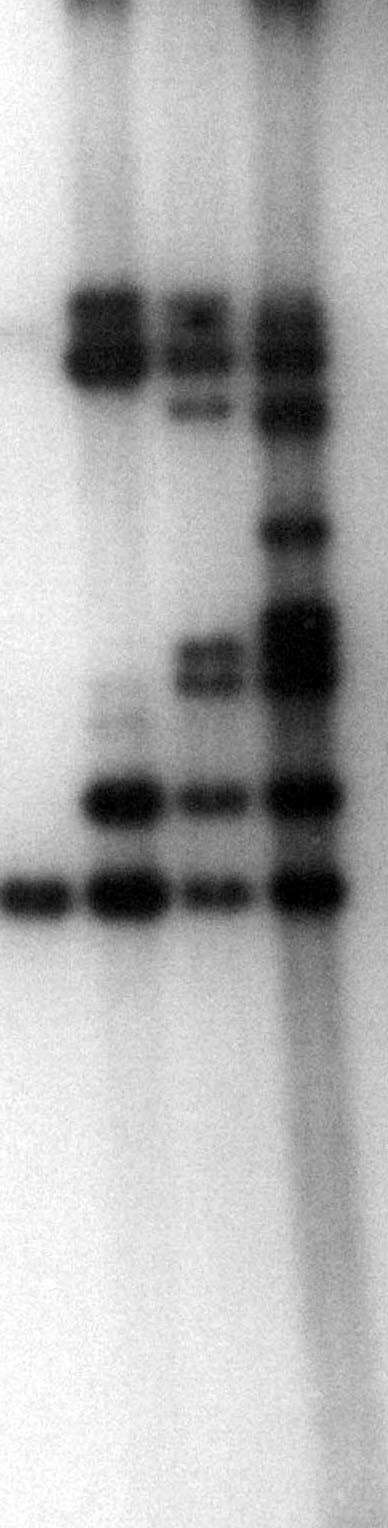
Число копий 1 4 7 10
Таким образом, проведенный повторный цикл амплификации привел к последующему увеличению числа копий валинового оперона с 7 до 10 в хромосоме исходного штамма V-3. Проведенный эффективный процесс амплификации валинового оперона сопровождался поэтапным увеличением продуктивности штаммов. Конструирование штамма-продуцента валина является примером эффективного применения способа увеличения числа копий интегративной кассеты путем последовательной амплификации с использованием только транспозазной плазмиды рМН10. В результате проведенной работы был получен бесплазмидный безмаркерный штамм-продуцент валина, в хромосоме которого содержится 10 интегрированных копий валинового оперона.
ВЫВОДЫ
1. Проведена оценка эффективности транспозиции группы транспозонов: Tn5, mini-Tn10, mini-Mu (MD4041), MD4041-thrA*BC. Показана высокая эффективность транспозиции mini-Mu транспозонов группы MD. Сконструированы штаммы-продуценты треонина с использованием интегративных векторов группы MD4041-thrA*BC. Показана нестабильность полученных штаммов, что явилось результатом высокой активности транспозазы, гены которой входят в состав данного транспозона.
2
. Проведено разделение интегративного и транспозазного доменов mini-Mu вектора MD4041, и разработана двухплазмидная система. Плазмида-помощник pMH10 кодирует транспозазу A фага Mu, транспозиционный кофактор - белок B, термочувствительный репрессор cts62, репрессор ner и attL-сайт. Интегративный вектор содержит сайты необходимые для интеграции (attL- и attR-сайты фага Mu) и маркер антибиотической устойчивости.
3. Проведено сравнительное изучение эффективности интеграции векторов pM-cts-IAS и pM, в которые были клонированы гены треонинового и лейцинового оперонов. Эффективность интеграции составила: 98-100% для векторов группы pM, что было в 30-50 раз более эффективно, чем для векторов группы pM-cts-IAS (2-3%). Проведена оценка эффективности амплификации векторов двух видов. При проведении нескольких последовательных этапов амплификации с использованием вектора pM число копий mini-Mu кассет было увеличено с 4 до 7, а затем до 10. Амплификация векторов группы pM-cts-IAS происходила с такой же низкой эффективностью, как и интеграция, и число копий mini-Mu кассет было увеличено с 1 до 2, а затем до 3 при проведении второго этапа амплификации.
4. Проведена оценка эффективности интеграции и амплификации многокопийных и малокопийных интегративных векторов, не содержащих антибиотический маркер. Наиболее эффективные интегративные векторы включают только attL- и attR-сайты фага Mu: pM, pM16, pM17. Во всех случаях наблюдался высокий процент интеграции: 85-100% (репликон рМВ1), 75-100% (репликон pSC101).
5
. Безмаркерные интегративные векторы были успешно использованы при конструировании генетически стабильного высокопродуктивного бесплазмидного штамма-продуцента валина, который содержал 10 копий mini-Mu кассет PR-ilvG*MED-2Tfd.
Список работ, опубликованных по теме диссертации:
1. Саврасова Е.А. // «Разработка интеграционной mini-Mu системы для обеспечения высокоэффективной интеграции и амплификации генетического материала в хромосому бактерии E. coli», Материалы международной школы-конференции «Генетика микроорганизмов и биотехнология», Москва, 28 ноября - 1 декабря, 2006 г, стр. 77-78.
2. Саврасова Е.А. // «Интеграционная mini-Mu система применимая для конструирования бесплазмидных штаммов-продуцентов аминокислот на основе E. сoli», Материалы четвертого московского международного конгресса «Биотехнология: состояние и перспективы развития», Москва, 12-16 марта, 2007, том 2, стр. 96.
3. Ахвердян В.З., Саврасова Е.А., Каплан А.М., Лобанов А.О., Вавилова Е.Ю., Козлов Ю.И. // «Разработка mini-Mu системы, обеспечивающей эффективную интеграцию генетического материала в хромосому бактерии Escherichia coli и его амплификацию». Биотехнология №3, 2007, стр.3-20.
4. Саврасова Е.А., Ахвердян В.З, Лобанов А.О., Каплан А.М., Вавилова Е.Ю., Козлов Ю.И. // «Создание mini-Mu системы, лишенной селективных маркеров, для интеграции генов в хромосому бактерии Escherichia coli».
Биотехнология №4, 2007, стр.3-17.
5. Ахвердян В.З., Саврасова Е.А., Каплан А.М., Лобанов А.О., Козлов Ю.И. «Способ получения L-аминокислот, штамм Escherichia coli – продуцент L-аминокислоты». Патент РФ №2229513.
6. Ахвердян В.З., Саврасова Е.А., Каплан А.М., Лобанов А.О., Козлов Ю.И. «Способ получения L-треонина, штамм Escherichia coli – продуцент треонина». Патент РФ №2244007.
7. Ахвердян В.З., Саврасова Е.А. «Бактерия, принадлежащая к роду Escherichia – продуцент треонина и способ получения L-треонина». Патент РФ №2288264.

