Поиск, идентификация и изучение экспрессии генов-кандидатов псориатического процесса
На правах рукописи
Брускин Сергей Александрович
ПоисК, идентификация и изучение экспрессии генов-кандидатов псориатического процесса
03.00.03 – молекулярная биология
АВТОРЕФЕРАТ ДИССЕРТАЦИИ НА СОИСКАНИЕ УЧЕНОЙ СТЕПЕНИ
КАНДИДАТА БИОЛОГИЧЕСКИХ НАУК
Москва – 2008
Работа выполнена в лаборатории функциональной геномики Института общей генетики им. Н.И. Вавилова РАН
| НАУЧНЫЙ РУКОВОДИТЕЛЬ: Доктор биологических наук, профессор | Пирузян Элеонора Суреновна |
| ОФИЦИАЛЬНЫЕ ОППОНЕНТЫ: Доктор биологических наук, профессор | Сулимова Галина Ефимовна |
| Институт общей генетики им. Н.И. Вавилова РАН | |
| Доктор биологических наук, профессор | Вейко Владимир Петрович |
| ФГУП «Государственный научно-исследовательский институт генетики и селекции промышленных микроорганизмов» | |
ВЕДУЩАЯ ОРГАНИЗАЦИЯ:
Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова
Защита состоится « » __________2008 г. в 1400 часов на заседании Диссертационного совета Д 217.013.01 при ФГУП «Государственный научно-исследовательский институт генетики и селекции промышленных микроорганизмов» по адресу: 117545, г. Москва, 1-й Дорожный проезд, д. 1.
С диссертацией можно ознакомиться в библиотеке ФГУП «Государственный научно-исследовательский институт генетики и селекции промышленных микроорганизмов».
Автореферат разослан «___» ___________ 2008 г.
Ученый секретарь
Диссертационного совета,
кандидат биологических наук Заиграева
Галина Григорьевна
Общая характеристика работы
Актуальность проблемы. Псориаз – заболевание кожи, является сложной генетически обусловленной патологией, в проявлении которой задействованы большие группы (сети) взаимодействующих генов/белков. При этой патологии запуск патологического процесса происходит внешними триггерами окружающей среды (психо - эмоциональные стрессы, инфекции и пр.). Патология на данный момент неизлечима, а лечение направлено на увеличение периодов ремиссии и на снижение тяжести болезни. В среднем псориазом страдает 3% населения мира, причем имеется четкая регионально-этническая дифференциация распространенности заболевания. Псориаз редко приводит к летальному исходу, однако существенно влияет на качество жизни пациентов и часто приводит к инвалидности. В последнее время псориазом болеет все больше молодежи, что впоследствии скажется на потере трудоспособности части взрослого населения, поэтому необходимо уже сейчас начинать разработку эффективных терапий и ранней диагностики псориаза.
Развитие любого многофакторного заболевания обусловлено двумя основными детерминантами - генетической предрасположенностью и запускающими заболевание триггерами. Локусы, связанные с псориазом, локализованы, по крайней мере, на 8 различных хромосомах и обозначаются как PSORS (Psoriasis Susceptibility) PSORS1 – PSORS9.
В патогенезе многофакторных заболеваний важным является вопрос, касающийся роли триггеров внешней среды. Некоторые из данных триггеров (например, инфекции) могут приводить к различному уровню экспрессии цитокинов у различных индивидуумов. Другие могут влиять на эпигенетические модификации (например, возможно опосредованные RUNX). Псориаз может быть спровоцирован стимулами внешней среды, такими как инфицирование стрептококком, повреждение (феномен Кебнера), стресс (нейропептиды), курение и алкоголь.
Характер питания и лекарственные препараты также могут провоцировать многофакторные заболевания. Среди токсинов N-нитросоединения являются основными кандидатами на роль триггеров многофакторных заболеваний. Поэтому является важным изучение полиморфизма генов системы биотрансформации ксенобиотиков.
Так как псориаз обусловлен разрегулированной работой генетического аппарата, то эффективным методом в разработке подходов для диагностики, лечения и создания лекарственных препаратов является поиск критических звеньев патологического процесса, а именно, генов-кандидатов и соответствующих белковых продуктов. Если генетические исследования многофакторных заболеваний продвинулись в достаточной степени как в России, так и за рубежом, то применение постгеномных технологий с целью выявления биомаркеров и исследования патогенеза данной патологии остаются задачей ближайшего будущего. К настоящему моменту, по существу, не опубликовано работ по комплексному использованию транскриптомики и протеомики для изучения псориаза. Благодаря стремительному развитию геномных и постгеномных технологий, пользуясь литературными источниками и базами данных, можно выделить известные ассоциированные с данными патологиями гены, на основании компьютерных исследований составить карты и сети, содержащие гены-кандидаты, и выделить подпроцессы, которые могут являться критическими в развитии патологий. Далее необходимо полученные результаты экспериментально проверить с помощью стандартных молекулярно-биологических методов.
Цель и задачи исследования. Основной целью исследования являлось проведение поиска, выявления и изучения экспрессии генов-кандидатов псориатического процесса.
В рамках работы были поставлены следующие задачи:
- Изучить возможную ассоциацию ферментов систем деградации ксенобиотиков у больных псориазом, на примере гена NAT2.
- Изучить изменение экспрессии генов BAX, BCL-2, CASP3 и TP53 при псориазе.
- С использованием методов информационной биологии определить круг генов-кандидатов патогенеза при псориазе.
- Проанализировать уровни экспрессии генов, кодирующих компоненты транскрипционного фактора AP1, в пораженной псориазом коже.
- Идентифицировать белки, участвующие в развитии очага поражения у больных псориазом.
Научная новизна работы. Впервые на основе анализа информационного материала при помощи программы «MetaCore®» компании GENEGO Inc. (США) определены гены-маркеры патологического процесса при псориазе, белки которых могут рассматриваться как потенциальные мишени для подбора индивидуализированной лекарственной терапии.
Впервые изучена возможная ассоциация полиморфизма гена системы биотрансформации ксенобиотиков (NAT2) и псориаза.
Впервые методом двумерного электрофореза проведено сравнение белковых профилей в пораженной и непораженной псориазом коже.
Практическая значимость работы. Данные, полученные при анализе экспрессии генов-кандидатов патогенеза при псориазе, могут способствовать разработке новых диагностикумов и идентификации новых мишеней лекарственных препаратов для лечения данного заболевания.
Апробация результатов работы. Основные положения и результаты работы были представлены на научно-практических конференциях «Молекулярная генетика, геномика и биотехнология» (Минск, 2004); «Новые информационные технологии в медицине, биологии, фармакологии и экологии» (Гурзуф, 2005); «Генетика в XXI веке: современное состояние и перспективы развития» (Москва, 2004); на 4-ом съезде Европейской ассоциации дерматовенерологов в 2006г. в Финляндии; на межлабораторном семинаре Института общей генетики им. Н.И. Вавилова РАН (Москва, 2007); на межлабораторном семинаре Государственного научно-исследовательского института генетики и селекции промышленных микроорганизмов (Москва, 2007);
Структура и объем диссертации. Диссертационная работа состоит из введения, обзора литературы, материалов и методов исследования, результатов и обсуждения, заключения, а также выводов и списка цитируемой литературы. Работа изложена на _153 страницах машинописного текста, включая _16_ таблиц, _41_ рисунок и __3_ фотографии. Список цитируемых литературных источников включает _137 наименований.
Основное содержание работы
Глава 1. Псориаз: характеристика заболевания и генетика патологии
В данной главе приведена клиническая характеристика заболевания и эпидемиология псориаза, обсуждается характер наследования заболевания. Особое внимание уделяется вопросу о роли триггеров внешней среды в патогенезе данного заболевания. В главе рассматриваются локусы, связанные с псориазом, локализованные, по крайней мере, на восьми хромосомах человека. Глава завершается обсуждением рабочей модели иммунопатогенеза псориаза. Особое внимание уделено процессам, происходящим в коже человека при развитии псориаза - в бессимптомной коже (предпсориатическая или визуально непораженная кожа больного), в которой уже возник ряд молекулярных изменений, и при появлении хронических поражений (псориатических бляшек).
Глава 2. N-ацетилтрансферазы человека
В главе обсуждается фенотип ацетилирования у человека и полиморфизм гена NAT2. Приведен список аллелей NAT2 у человека. Обсуждается ассоциация фенотипа ацетилирования с рядом многофакторных заболеваний, в числе которых ряд онкологических заболеваний, астма, диабет 1 типа, системная красная волчанка.
Глава 3. Транскрипционный фактор АР-1
В главе обсуждаются компоненты транскрипционного фактора AP-1, участие их в ответе клеток на действие ряда сигнальных молекул, их участие в процессах развития кожи, а также механизмы регуляции экспрессии генов, кодирующих компоненты транскрипционного фактора AP-1.
Глава 4. Материалы и методы
В главе приведен перечень бактериальных штаммов и сред для выращивания E.coli, составы использованных буферов.
Приведены методы выделения ДНК и РНК, определения фенотипа ацетилирования, генотипа ацетилирования на микрочипах, мультиплексной полимеразной цепной реакции, обратной транскрипции, полуколичественной полимеразной цепной реакции и полимеразной цепной реакции в реальном времени.
Приведены методы определения активности каспазы–3 в образцах кожи колориметрическим методом, определения содержания белка р53 в образцах кожи методом Вестерн-блот гибридизации. Приведен метод двумерного электрофореза.
Статистическая обработка данных проводилась с использованием программы STATISTICA 6.0.
Глава 5. Результаты и обсуждение
5.1. Сравнительное изучение фенотипа ацетилирования и полиморфизма гена NAT2
Для того чтобы провести сравнительный анализ результатов по полиморфизму N-ацетилирования, получаемых с использованием метода определения ацетилирующей способности индивидуума (фенотип ацетилирования) и метода аллель-специфичной гибридизации на микрочипе (генотип ацетилирования), были проведены следующие исследования.
Фенотип ацетилирования был определен в группе волонтеров методом тестирования скорости ацетилирования сульфадимезина. Генотип NAT2 в популяционной выборке волонтеров определяли методом гибридизации ДНК на биочипе и на основании полученных результатов рассчитывали предполагаемые фенотипы ацетилирования. Как видно из представленных данных, частота медленных ацетиляторов в популяционной выборке составляет 45% (рисунок 1) и достоверно не отличается (p>0.01) от результатов, полученных при определении фенотипа ацетилирования методом тестирования скорости ацетилирования (47%).
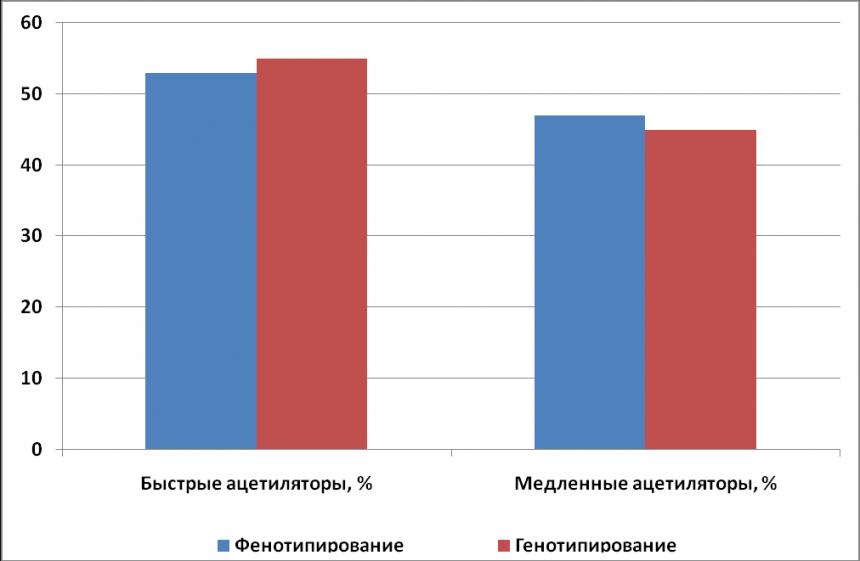
Рисунок 1. Частота фенотипов быстрых и медленных ацетиляторов по локусу NAT2 в московской выборке волонтеров, рассчитаная согласно данным фенотипирования и генотипирования
Сравнительные характеристики и предполагаемые области применения двух подходов (количественное определение скорости ацетилирования и качественное определение генотипа ацетилирования) для определения статуса ацетилирования у индивидуумов представлены в таблице 1.
Таблица 1. Сравнительные характеристики и области применения методов определения фенотипа и генотипа ацетилирования
| Фенотипирование | Генотипирование | |
| Возможности | Точное количественное определение фенотипа ацетилирования. За счет одного измерения суммируются все возможные полиморфизмы в кодирующей области гена NAT2 и промоторной области. | Точное качественное определение фенотипа ацетилирования (быстрый или медленный). За счет одного измерения определяются известные полиморфизмы в кодирующей области гена NAT2. |
| Область применения | Предсказание риска токсичности или положительного эффекта от применения лекарственных препаратов. Выявление предрасположенности к заболеваниям в зависимости от скорости ацетилирования | Проведение популяционных исследований по генетическому полиморфизму ацетилированию. Выявление предрасположенности к заболеваниям в зависимости от генотипа гена NAT2. |
На основании полученных данных и сравнительного анализа можно сделать следующие заключения. Метод определения ацетилирующей способности индивидуума для выявления фенотипа ацетилирования за одно измерение позволяет суммировать все известные полиморфизмы и количественно определить уровень ацетилирования у индивидуума. На основании этого можно предложить этот метод для количественной оценки скорости ацетилирования у индивидуума и более точного предсказания риска токсичности или, наоборот, положительного эффекта от применения лекарственных препаратов. Метод гибридизации ДНК на олигонуклеотидной матрице (биочипе) позволяет достаточно точно определить генотипы и аллели, а также распределение частот аллелей и генотипов в популяционных выборках индивидуумов. На основании этого можно предположить, что созданный гелевый микрочип даст возможность проводить популяционные исследования по генетическому полиморфизму ацетилирования индивидуумов без фенотипирования, в том числе и с целью установления корреляции между генотипом ацетилирования и предрасположенностью данного индивидуума к заболеваниям.
5.2. Полиморфизм гена NAT2 и его ассоциация с псориазом
На основании литературных данных, свидетельствующих о том, что полиморфизм гена NAT2 строго ассоциируется с рядом онкологических заболеваний, а также в связи с имеющимися литературными данными о взаимосвязи фенотипа ацетилирования с другим системным воспалительным аутоиммунным барьерным заболеванием – системной красной волчанкой (SLE), нами было высказано предположение о возможной взаимосвязи фенотипа ацетилирования и псориаза.
Основываясь на результатах по взаимосвязи между фенотипом и генотипом ацетилирования и на возможности использования биологических микрочипов для определения генотипа NAT2, нами было проведено исследование группы больных псориазом (180 человек) и здоровых волонтеров (99 человек).
В таблице 2 показано распределение частоты встречаемости шести однонуклеотидных замен в позициях 282, 341, 481, 590, 803 и 857 гена NAT2 у больных псориазом и здоровых индивидуумов. Это основные, наиболее часто встречающиеся замены в московской выборке, вносящие вклад в изменение фенотипа ацетилирования. Частота встречаемости ни одной из замен достоверно не различаются (p>0.01) в выборке здоровых волонтеров и больных псориазом. Это указывает на отсутствие роли ряда ксенобиотиков, а также продуктов их биотрансформации за счет ацетилирования N-ацетилтрансферазой, в запуске или развитии патогенеза псориаза.
Также не выявлено достоверного отличия (p>0.01) между скоростью ацетилирования у больных псориазом и здоровых индивидуумов.
Таблица 2. Сравнение распределения частот встречаемости однонуклеотидных замен в позициях 282, 341, 481, 590, 803 и 857 гена NAT2 у больных псориазом (слева) и здоровых индивидуумов (справа) в г. Москве
| 282 | 341 | 481 | ||||
| AA* | 0,50 | 0,59 | 0,33 | 0,28 | 0,42 | 0,35 |
| Aa | 0,42 | 0,37 | 0,46 | 0,57 | 0,49 | 0,58 |
| aa | 0,08 | 0,04 | 0,21 | 0,15 | 0,09 | 0,07 |
| 590 | 803 | 857 | ||||
| AA | 0,43 | 0,55 | 0,35 | 0,30 | 0,95 | 0,92 |
| Aa | 0,48 | 0,40 | 0,52 | 0,56 | 0,05 | 0,07 |
| aa | 0,09 | 0,05 | 0,13 | 0,14 | 0,00 | 0,01 |
A – аллель дикого типа, а – аллель мутантного типа
Следует, однако, подчеркнуть, что у больных псориазом выявлена достоверная ассоциация (p<0.01) с полиморфным сочетанием 282C/T 341C/C 481C/T 590G/A 803A/G 857A/A в гене NAT2.
5.3. Изменение некоторых апоптических медиаторов и эффекторов в ко же у больных псориазом
В нормальном эпидермисе кератиноциты поддерживают точное и тонко сбалансированное соотношение между клеточной пролиферацией и клеточной дифференцировкой. При созревании кератиноцитов в псориатических бляшках нарушены клеточная дифференциация и клеточная пролиферация. Если нормальный цикл созревания кератиноцитов составляет 28-30 дней, то при псориазе наблюдается его ускорение в восемь раз и сокращение цикла созревания кератиноцитов до 3-4 дней [Bowcock, Cookson, 2004]. Кроме того, в псориатической коже отмечаются изменения в процессе апоптоза, что приводит к утолщению рогового слоя кожи.
Нами было изучено изменение соотношения продуктов генов BAX и BCL-2 в пораженной и непораженной коже больных псориазом и его изменение после лечения методом полуколичественной ПЦР, сопряженной с обратной транскрипцией. Лечение пациентов проводилось препаратом Глутоксим®. Эффективность лечения оценивалась по изменению индекса PASI.
На рисунке 2 показано влияние успешного лечения препаратом «Глутоксим®» на соотношение мРНК генов Bax/Bcl-2. Соотношение Bax/Bcl-2 изменилось достоверно (p<0.01).
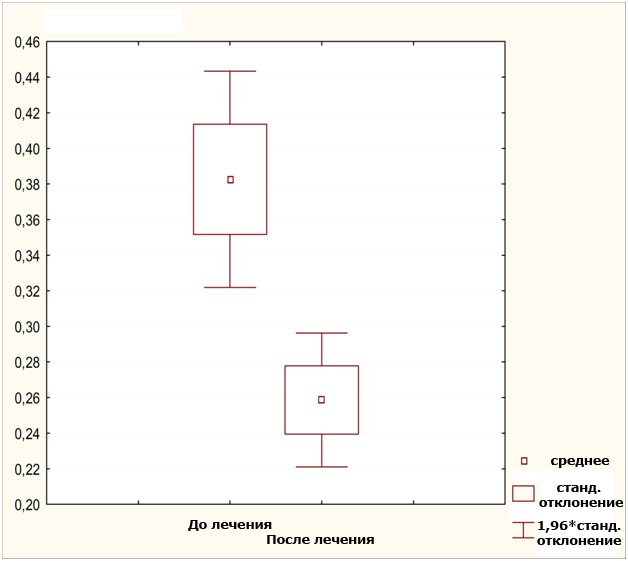
Рисунок 2. Изменение соотношения мРНК генов в коже больных псориазом до и после лечения препаратом «Глутоксим®».
Независимо от пути развития сигнала на апоптоз ключевая роль в процессе отводится каспазам, ферментам, осуществляющим деградацию белков и нуклеиновых кислот в клетке. Вследствие того, что каспаза-3 является, если не ключевой, то одной из самых важных эффекторных каспаз, мы определяли изменение ее активности в пораженной коже больных псориазом, а также изучили влияние лечения пациентов на изменение активности каспазы в коже больного.
Однако здесь мы не получили достоверного отличия активности фермента (рисунок 3) в группе больных до и после лечения (p>0.01).
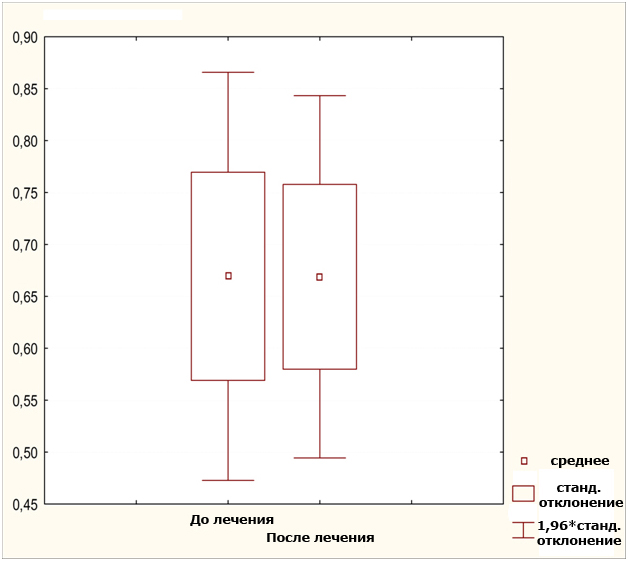
Рисунок 3. Изменение активности белка каспазы-3 в коже больных псориазом до и после лечения препаратом «Глутоксим®».
5.4. Компоненты транскрипционного фактора AP-1 как гены - кандидаты при псориазе.
Нашей задачей было произвести поиск генов-кандидатов на развитие псориатического процесса. Классический генетический подход в поиске генов-кандидатов заключается в семейном анализе и установлении генетических ассоциаций между проявлением болезни и сцепленными с этим проявлением локусами. На данный момент высокоинформативным инструментом изучения экспрессии больших групп генов являются результаты экспериментов, в которых экспрессия генов оценивается количественно с помощью биологических микрочипов. В своих биоинформационных исследованиях мы использовали базу данных GEO DataSets (http://www.ncbi.nlm.nih.gov/geo/), в которой в виде электронных таблиц собраны результаты экспериментов оценки уровня экспрессии генов на микрочипах. Для дальнейшего анализа нами была отобрана запись GDS1391, в которой представлена информация об уровне экспрессии генов в коже трех здоровых волонтеров, а также в пораженной и непораженной коже четырех больных псориазом.
На данный момент в рамках стремительного развития постгеномных технологий появляются программные продукты, позволяющие концентрировать и систематизировать большие объемы генетической информации, выстраивать гипотезы генных сетевых взаимодействий. Одной из таких программ является программный продукт MetaCore® компании GENEGO Inc (США). В результате информационного анализа экспрессии около 12000 генов на биологических микрочипах с помощью программы MetaCore нами было установлено, что число генов, изменивших свою экспрессию более чем в 1,5 раза при псориазе, составляет 7563.
На первом этапе мы сравнили уровни экспрессии генов (транскриптом) в пораженной коже больных псориазом и в коже здоровых волонтеров. Для всех генов был установлен порог изменения уровней экспрессии равный 2, то есть программа будет работать только с теми генами, уровень экспрессии которых изменен (увеличен или уменьшен) более чем в 2 раза в пораженной коже, по сравнению с уровнем экспрессии тех же генов в коже здоровых волонтеров.
Анализ транскриптомных данных показал, что при псориазе преимущественно наблюдается увеличение транскрипции множества генов. Обилие генов, существенно увеличивших свою экспрессию при псориазе в ключевых процессах клеточного метаболизма, свидетельствует в пользу того, что патологический процесс в пораженной коже в целом обусловлен именно увеличением транскрипционной активности генов в клетках кожи, что совпадает с литературными данными о гиперактивности пролиферативной способности кератиноцитов кожи и ускоренных процессах дифференцировки клеток кожи [Liu Y et al., 2007].
Если представить распределение генов, изменивших свою транскрипцию в пораженной коже больных псориазом по сравнению с кожей здоровых волонтеров, по их участию в различных молекулярно-генетических процессах, то основными измененными процессами в коже при псориазе являются иммунный ответ, клеточный цикл, воспаление, пролиферация и др. (рисунок 4).
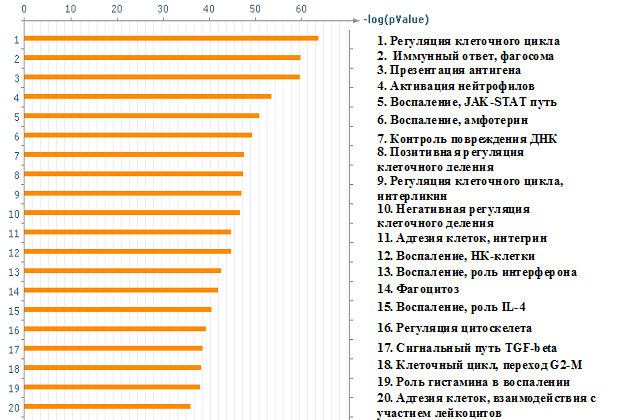
Рисунок 4. Основные процессы, измененные в коже больных псориазом, по сравнению с кожей здоровых волонтеров
Большой интерес для нас представляло сравнение уровней экспрессии генов в пораженной части кожи больных псориазом по отношению к визуально непораженной части кожи, находящейся на расстоянии не более 3 см от пораженной псориазом кожи одного и того же больного. Такое сравнение позволяет максимально исключить влияние побочных факторов на чистоту эксперимента. Для всех генов был установлен порог изменения уровней экспрессии равный 2. Мы сравнивали данные от 4-х пациентов.
На рисунке 5 показаны первые 20 наиболее измененных процессов в пораженной коже больных в сравнении с непораженной кожей. Как видно, этими процессами являются развитие эпидермиса, кератинизация, дифференциация кератиноцитов, метаболизм липидов и другие.

Рисунок 5. Первые 20 наиболее измененных процессов в пораженной коже в сравнении с непораженной кожей больных псориазом.
Далее мы выдвинули гипотезу, что для изменения экспрессии больших групп координировано работающих генов, что мы можем наблюдать при псориазе, задействованных в тех или иных процессах в клетке (множество разрегулированных процессов при псориазе), необходимо, чтобы, прежде всего, изменили свою экспрессию ключевые транскрипционные факторы, инициирующие каскадные процессы.
Нами проанализированы измененные при псориазе клеточные процессы с целью их детального описания. При этом для дальнейшего анализа мы выбрали 10 процессов с самым высоким значением величины p-value. Для визуализации генетических процессов на уровне генных сетевых взаимодействий мы использовали карты сетевых взаимодействий генов, наложив на них изменения в уровнях экспрессии генов. При этом выбирали карты взаимодействий генов, описывающие основные измененные процессы в клетке. Карты сетевых взаимодействий генов отличаются от генных сетей тем, что в них информация о генных взаимодействиях систематизирована и выстроена в соответствии с современными представлениями о конкретном молекулярно-генетическом процессе, описанном с помощью данной карты. На рисунке 6 приведены условные обозначения, используемые на картах сетевых взаимодействий генов.
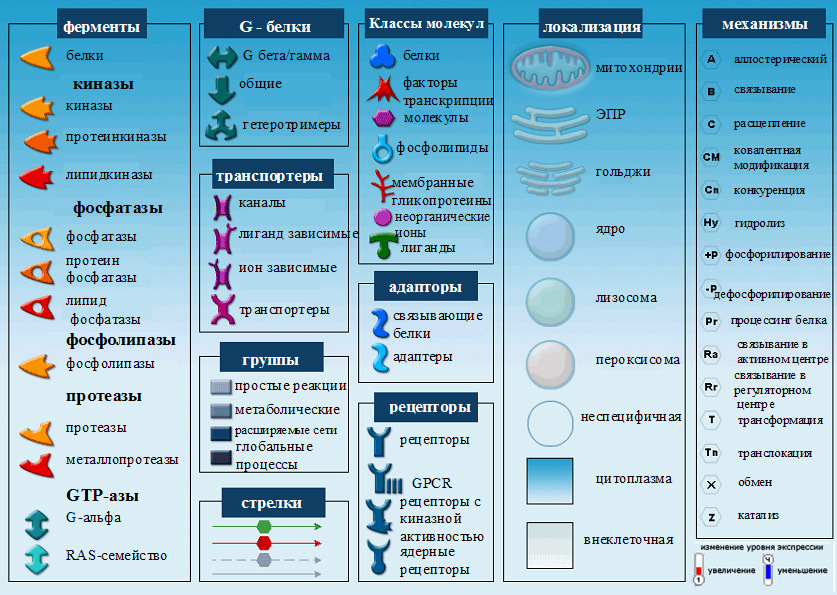
Рисунок 6. Условные обозначения, используемые на картах сетевых взаимодействий генов.
На рисунке 7 приведена карта сетевых взаимодействий генов при передаче сигнала от EGF рецептора в клетку и изменение экспрессии ее компонентов в пораженной коже больных псориазом по сравнению с кожей здоровых волонтеров. Видно, что, хотя уровень экспрессии рецептора не изменен значительно, существенно изменен уровень экспрессии всех его лигандов (от 2 раз для EGF до более чем в 30 раз для ERBB2). Также обращает на себя внимание и то, что изменена экспрессия генов, которые активируются различными путями после связывания рецептора с лигандом.
Рисунок 7. Карта сетевых взаимодействий генов при передаче сигнала от EGF рецептора в клетку и изменение экспрессии генов, участвующих в данном пути, в пораженной коже, в сравнении с кожей здоровых волонтеров.
На рисунке 8 показано сетевое взаимодействие генов при передаче сигнала от EGF рецептора (EGFR) в клетку и изменение экспрессии генов, участвующих в данном пути, в пораженной коже, в сравнении с непораженной. Как видно, в пораженной коже значительно изменена экспрессия только транскрипционных факторов (c-Fos, c-Myc и STAT3, примерно в 2,5-3 раза). Если сравнить данные, представленные на рисунке 8, с данными, представленными на рисунке 7, то мы увидим, что ни медиаторы передачи сигнала, такие как GRB2, Shc, SOS, h-Ras, c-RAF, MEK1/2 и др., ни лиганды, ни рецептор не изменили свою экспрессию, а активированными в пораженной коже в сравнении с непораженной остались только c-Fos, c-Myc и STAT3. Однако необходимо отметить, что, если в сравнении со здоровыми, c-Myc и c-Jun увеличивали экспрессию почти в 7 раз, то в сравнении с непораженной кожей c-Jun не изменил экспрессию, а c-Myc увеличил всего в 3 раза, c-Fos и STAT3 увеличивали экспрессию в 13 и 11 раз, соответственно, в сравнении со здоровыми и всего в 2,7-3 раза в сравнении с непораженной кожей. Все это свидетельствует в пользу того, что изменения процессов метаболизма происходят не только в пораженной, но и в непораженной коже, причем непораженная кожа больных псориазом, в смысле измененных метаболических процессов, занимает промежуточное положение между кожей здоровых людей и пораженной кожей [Nickoloff and Nestle, 2004].
Мы проанализировали вышеобозначенные карты генных взаимодействий при псориазе и пришли к выводу, что во всех исследуемых процессах в качестве основных транскрипционных факторов, изменивших свою экспрессию при псориазе, присутствуют только компоненты транскрипционного фактора АР-1 и транскрипционный фактор NF-kB. Фактор NF-kB, как известно, активируется при иммунных ответах и не является специфичным для псориаза, поэтому мы его исключили из генов-кандидатов.
Напротив, компоненты транскрипционного комплекса AP-1 могут являться генами-кандидатами при псориазе по следующим причинам. Известно, что транскрипционный фактор AP-1 представляет собой группу парных комплексов, образованных ДНК-связывающими белками, входящими в семейства Jun, Fos и ATF. Фактор AP-1 обеспечивает ответ клеток на действие ростовых факторов, цитокинов, нейротрансмиттеров и других межклеточных сигнальных молекул. В регуляции активности AP-1 участвуют G-белки, адаптерные белки, MAP-киназы и другие компоненты внутриклеточных регуляторных систем. Зависимые от AP-1 гены играют важную роль в регуляции пролиферации, морфогенеза, апоптоза и дифференцировки клеток. Транскрипционный фактор АР-1 участвует в поддержании базального уровня экспрессии многих генов. Он является одной из главных мишеней для соединений, вызывающих клеточную пролиферацию или дифференцировку.
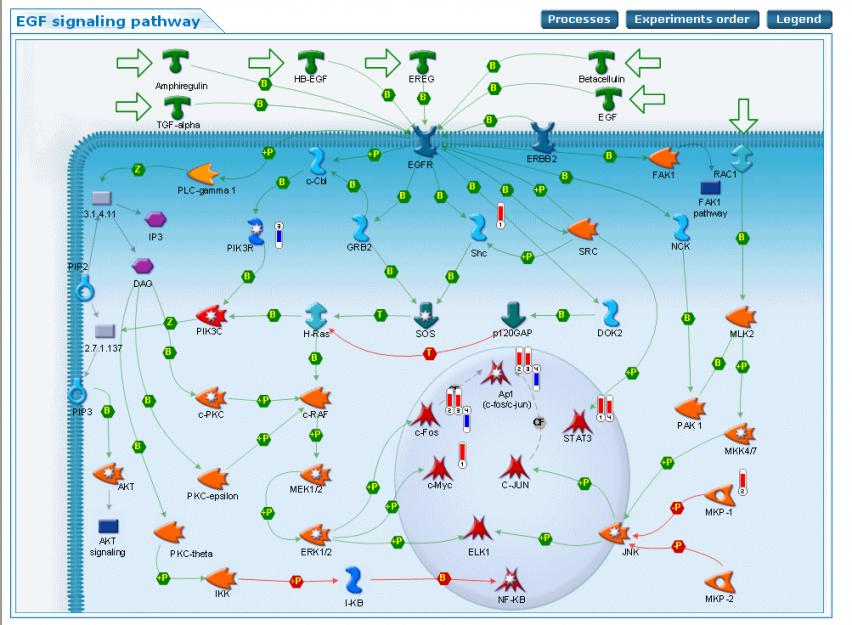
Рисунок 8. Карта сетевых взаимодействий генов при передаче сигнала от EGF рецептора в клетку и изменение экспрессии генов, участвующих в данном пути, в пораженной коже, в сравнении с непораженной у больных псориазом.
Известно, что AP-1 обеспечивает ответ клеток на действие различных сигнальных молекул: цитокинов, пептидных гормонов, нейротрансмиттеров, ростовых и паракринных факторов. Активация AP-1 также происходит в экстремальных для клеток условиях: при тепловом шоке, гипоксии, в присутствии ксенобиотиков и токсинов, под действием УФ-облучения и ионизирующей радиации, а также при изменении осмотического давления и динамическом воздействии на плазматические мембраны.
Все это обусловливает возможность участия генов AP-1 системы в патогенезе воспалительных барьерных заболеваний. Действительно, при анализе данных экспрессионных микрочипов нами выявлено, что экспрессия генов c-Fos, c-Jun и JunB увеличена в 10-20 раз при псориазе.
5.5. Анализ уровней экспрессии генов, кодирующих компоненты транскрипционного фактора AP1
На основании биоинформационного анализа мы выдвинули предположение о возможной ключевой роли белков компонентов транскрипционного фактора AP1 в развитии поражения и сравнили экспрессию генов JUNB, JUND и ATF4 в пораженной псориазом коже по сравнению с непораженной.
Для анализа уровня экспрессии мы использовали метод полимеразной цепной реакции в реальном времени. Обработку результатов полимеразной цепной реакции проводили методом 2-CT согласно [Livak and Schmittgen, 2001].
На рисунке 9 показано изменение уровня экспрессии генов JUNB, JUND и ATF4 в пораженной псориазом коже в сравнении с непораженной кожей этих же больных (№№1-4).
Видно, что экспрессия гена JUNB в пораженной коже увеличена по сравнению с непораженной в 2,5 раза (у больного №2) и до 7 раз (у больного №1). Экспрессия гена JUND увеличена у больных №1 и №3 в 2,5 и 4,5 раза, а гена ATF4 уменьшена в 1,5 и 5 раз, соответственно. У больного №2 экспрессия генов JUND и ATF4 практически не изменилась. Так же на рисунке 9 показано изменение уровня экспрессии генов JUNB, JUND и ATF4 в пораженной псориазом коже в сравнении с непораженной кожей у больного №4. У этого больного экспрессия всех изучаемых генов снижена (JUNB уменьшена в 1,3 раза, JUND в 2,6 раза, ATF4 в 1,7 раза).
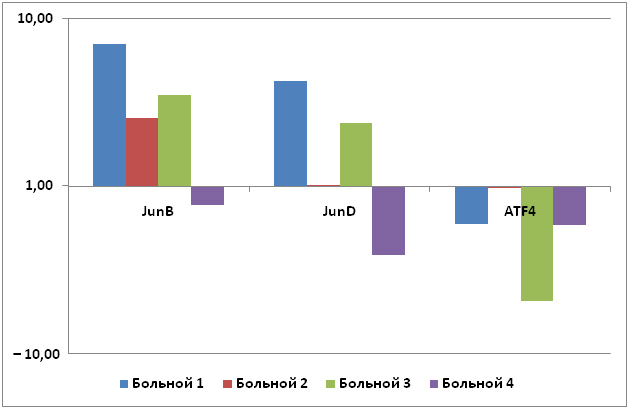
Рисунок 9. Изменение уровня экспрессии генов JUNB, JUND и ATF4 у больных псориазом в пораженной коже по сравнению с непораженной.
5.6. Идентификация новых белков, участвующих в развитии очага поражения у больных псориазом
(на базе Института биомедицинской химии РАМН)
В данном исследовании мы использовали биопсии пораженной и непораженной кожи от трех пациентов больных псориазом Типа I.
После электрофореза и окрашивания гелей серебром мы идентифицировали 10 новых пятен, которые не встречались (или их интенсивность была существенно ниже) в непораженной коже и которые проявили себя в очаге поражения.
На рисунках 10 и 11 приведены электрофореграммы разделения белков в двух направлениях в пораженной и непораженной коже от одного пациента. Красной рамкой показаны пятна, которые изменены в пораженной коже по сравнению с непораженной.
 |  |
| Рисунок 10. 2D-электрофорез белков кожи, пораженной псориазом. | Рисунок 11. 2D-электрофорез белков непораженной псориазом кожи. |
Пятна были вырезаны из геля (~ 3 мм2) и белки из них были идентифицированы. Белки из пятен № 1, 2, 3, 4 были идентифицированы методом MALDI-TOF масс-спектрометрии, а белки из пятен 5-10 были идентифицированы методом nanoLC-MS/MS масс-спектрометрии.
Результаты идентификации белков приведены в таблице 3.
Таблица 3. Идентифицированные белки, различающиеся в пораженной и непораженной псориазом коже.
| Пятно, номер | Название белка | %Vol | |
| Пораженная кожа | Непораженная кожа | ||
| 1 | Кератин 17 | 1,97±0,92 | 0,18±0,06 |
| Кератин 14 | |||
| Кератин 16 | |||
| 2 | SCCA2/SCCA1 | 0,28±0,09 | 0,066±0,02 |
| 3 | Антиген чешуйчатой клеточной карциномы; SCC antigen | 0,35±0,18 | 0,03±0,01 |
| 4 | Енолаза 1 | 0,87±0,22 | 0,40±0,14 |
| 5 | Супероксиддисмутаза [Mn] | 0,22±0,03 | 0,11±0,02 |
| 6 | Галлектин 7; Gal-7 | 1,14±0,41 | 0,19±0,01 |
| 7 | Белок S100-A9 | 0,54±0,03 | 0 |
| 8 | Белок S100-A9 | 0,15±0,07 | 0 |
| 9 | Белок S100-A7 (Псориазин, Psoriasin) | 0,51±0,16 | 0 |
| 10 | Белок S100-A7 (Псориазин, Psoriasin) | 1,36±0,37 | 0,02±0,03 |
Заключение
В этом разделе представлены полученные в работе результаты, а также приводятся новые литературные данные, свидетельствующие о возможных новых механизмах регуляции патогенетического процесса при псориазе.
Выводы
- Проведенный биоинформационный анализ сетевых взаимодействий генов позволил отобрать гены, кодирующие белки- компоненты транскрипционного фактора АР-1, как возможные гены, влияющие на развитие патологического процесса при псориазе.
- Показано, что в отличие от корреляции скорости ацетилирования с предрасположенностью к другому многофакторному заболеванию системной красной волчанке, нами не показана ассоциация между псориазом и скоростью ацетилирования. Тем не менее, полиморфное сочетание 282C/T 341C/C 481C/T 590G/A 803A/G 857A/A показало ассоциацию с заболеванием.
- Определение соотношения транскриптов генов BAX/BCL2 до и после успешного лечения у больных псориазом дает основание считать, что это соотношение может быть маркером степени тяжести псориатического процесса.
- Проведено количественное измерение экспрессии генов JUNB, JUND и ATF-4 с помощью полимеразной цепной реакции в реальном времени, в результате чего было экспериментально показано изменение экспрессии данных генов в пораженной псориазом коже.
- С помощью протеомного анализа образцов псориатической кожи установлены 10 маркерных белков, присутствующих только в пораженной коже. Данные белки могут рассматриваться как потенциальные мишени действия фармакологических препаратов при лечении псориаза.
Список работ, опубликованных по теме диссертации
- С.А. Брускин, М.К. Саркисова, Ан.Л. Пирузян. Метаболическая и генетическая паспортизация человека для ранней диагностики и индивидуальной фармакотерапии. Материалы Международной научной конференции «Молекулярная генетика, геномика и биотехнология». Минск. С. 219-221. 2004.
- И.В. Голденкова, Ан.Л. Пирузян, М.К. Саркисова, С.А. Брускин, Р.М. Абдеев, А. Махулаева, И.М. Корсунская. Метаболическая и генетическая паспортизация человека для ранней диагностики и индивидуальной фармакотерапии кожных заболеваний на примере витилиго и псориаза, Материалы III Съезда генетиков и селекционеров России. «Генетика в XXI веке: современное состояние и перспективы развития», Т.I. С. 63., Москва., 2004
- С.А. Брускин, А.С. Глотов, Т.В. Наседкина, Л.А. Радкевич, И.В. Голденкова. Разработка микрочипа быстрого скрининга генотипа и установления фенотипа ацетилирования для метаболической и генетической паспортизации человека с целью ранней диагностики и индивидуальной фармакотерапии, IT+M&Ec'2005, С. 201-204. Гурзуф, Украина, 2005
- Кожекбаева Ж.М., Глотов А.С., Брускин С.А., Голденкова И.В., Пирузян Э.С., Заседателев А.С., Наседкина Т.В. Разработка биочипа для определения аллельных вариантов NAT2 гена. VI Международная конференция «Молекулярная генетика соматических клеток», С. 76, Звенигород, 2005
- С.А. Брускин, А.В. Марахонов, И.В. Голденкова-Павлова, Э.С. Пирузян. Термостабильные ферменты для наработки новых терапевтических и профилактических препаратов и диагностических систем, Сборник научных трудов «Факторы экспериментальной эволюции организмов», С. 537-542., Алушта, 2006
- И.М. Корсунская, Л.В. Егоренкова, Э.С. Пирузян, С.А. Брускин, Р.М. Абдеев, И.В. Голденкова-Павлова, Л.Т. Тогоева, С.С. Олейник, Ан.Л. Пирузян. Роль системы апоптоза в патогенезе псориаза. Клиническая дерматология и венерология. №6, C.13-17, 2006.
- И.В. Голденкова-Павлова, С.А. Брускин, Р.М. Абдеев, Е.В. Маркарова, С. Г. Бигвава, Л.А. Радкевич, Х.А. Курданов, Ж.М. Кожекбаева, А.С. Глотов, О.А. Гра, А.С. Заседателев, Т.В. Наседкина, Э.С. Пирузян. Сравнительный анализ результатов фенотипирования и генотипирования по полиморфизму N-ацетилирования у человека. Генетика. Т. 42. № 8. с. 1443-1450, 2006.
- С.А. Брускин, Ж.М. Кожекбаева, Т.В. Наседкина, И.В. Голденкова-Павлова. Сравнительный анализ результатов фенотипирования и генотипирования по полиморфизму N-ацетилирования у человека, Материалы Международной конференции «Генетика в России и мире», С. 21, Москва, 2006
- Z. M. Kozhekbaeva, O. A. Gra, A. S. Glotov, I. V. Goldenkova-Pavlova, S.A. Bruskin, E. V. Markarova, E. S. Piruzyan, T. V. Nasedkina. N-acetyltransferase 2 (NAT2) gene polymorphisms in psoriasis and colon cancer patients from the Moscow population// Supplementary of Eur. J. Hum. Genet. Nice. France, June 16-19. 2007 Ж. М. Кожекбаева, А. С. Глотов, О. А. Гра, И. В. Голденкова-Павлова, С. А. Брускин, Е. Е. Агафонова, Е. В. Маркарова, Р. М. Абдеев, И. М. Корсунская, Ан. Л. Пирузян, В. Е. Барский, А. С. Заседателев, Т. В. Наседкина. Определение точечных мутаций гена NAT2 с помощью биологических микрочипов// Молекулярная биология. №41, стр.725-733, 2007
- Э.С.Пирузян, Т.А. Никольская, Р. М. Абдеев, С. А. Брускин. АР-1 система транскрипционных факторов как гены-кандидаты при псориазе// Молекулярная биология. т.41, C.1069-1080, 2007
- Брускин С.А., Абдеев Р.М., Пирузян Э.С. Изучение изменения соотношения мРНК генов BAX/BCL-2 в коже больных псориазом. Приложение к журналу "Открытое образование" Материалы XV Международной конференции и дискуссионного научного клуба "Новые информационные технологии в медицине, биологии, фармакологии и экологии" IT+M&Ec'2007 Украина, Крым, Ялта-Гурзуф. С. 47-49, 2007
- R.M. Abdeev, S.A. Brouskin, T.A. Nikolskaya, E.S. Piruzian. Survey of psoriasis candidate genes by using bioinfirmatics. In Abstract Book of Four International Symposium on Computational Methods in Toxicology and Pharmacology Integrating Internet Resources. Russia, Moscow, p. 71, 2007
- S.A. Brouskin, R.M. Abdeev, T.A. Nikolskaya, E.S. Piruzian. Comparison of psoriasis and Crohn’s disease pathological processes at the level of gene network interactions by bioinformatics methods. In Abstract Book of Four International Symposium on Computational Methods in Toxicology and Pharmacology Integrating Internet Resources. Russia, Moscow, p. 86, 2007
- S.A. Bruskin, R.M.Abdeev, S.A.Moshkovsky, I.M.Korsunskaya, E. S. Piruzyan. Study of protein profiles in psoriatic plaques and healthy skin//Abstr.book 6th Annual Cytokines and Inflammation Conf., 28-29 January, Orlando, USA. 2008
- С.А. Брускин, И.В. Голденкова-Павлова, И.М. Корсунская, Ан.Л. Пирузян. Патент №2311643 от 06/04/2006 «Способ оценки состояния апоптической системы в коже у больных псориазом»
- Корсунская И.М., Брускин С.А., Ан.Л. Пирузян, Абдеев Р.М. Патент по заявке 049747 от 21 декабря 2006 г. «Способ оценки состояния апоптической системы в коже у больных псориазом»

