Экспрессия генов гуанилспецифичных рибонуклеаз бацилл в условиях фосфатного голодания
На правах рукописи
УЛЬЯНОВА Вера Владимировна
ЭКСПРЕССИЯ ГЕНОВ ГУАНИЛСПЕЦИФИЧНЫХ РИБОНУКЛЕАЗ БАЦИЛЛ В УСЛОВИЯХ ФОСФАТНОГО ГОЛОДАНИЯ
03.00.07 – микробиология
Автореферат
диссертации на соискание ученой степени
кандидата биологических наук
Казань – 2009
Работа выполнена на кафедре микробиологии Казанского государственного университета им. В. И. Ульянова-Ленина
| Научный руководитель: | кандидат биологических наук, доцент Вершинина Валентина Ивановна |
| Официальные оппоненты: | доктор биологических наук, старший научный сотрудник Коксин Владимир Петрович (РЦПБ СПИД и ИЗ МЗ РТ, г. Казань) кандидат биологических наук, старший научный сотрудник Морозова Ольга Владимировна (Институт проблем экологии и недропользования АН РТ, г. Казань) |
| Ведущая организация: | Казанский институт биохимии и биофизики КНЦ РАН, г. Казань |
Защита диссертации состоится «26» ноября 2009 г. в __ часов на заседании диссертационного совета Д 212.081.08 при Казанском государственном университете по адресу: 420008, г. Казань, ул. Кремлевская, д. 18, главное здание, ауд. 211.
С диссертацией можно ознакомиться в научной библиотеке им. Н. И. Лобачевского при Казанском государственном университете.
Автореферат разослан «21» октября 2009 г.
Ученый секретарь
диссертационного совета,
доктор биологических наук З. И. Абрамова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Ферменты нуклеинового обмена в течение многих лет привлекают к себе внимание исследователей в связи с их исключительной ролью в жизни организмов и практической значимостью для человека. Рибонуклеазы выполняют важные функции в метаболизме бактериальных клеток: они не только необходимы для извлечения рибонуклеотидов из окружающей среды и элиминации ненужных внутриклеточных РНК, но и участвуют в контроле экспрессии генов путем изменения стабильности различных видов РНК. Кроме того, секретируемые рибонуклеазы могут являться для их продуцентов эффективным средством в конкурентной борьбе с другими микроорганизмами за экологическую нишу.
Рибонуклеазы применяются в генной инженерии, молекулярной биологии и биотехнологии для удаления РНК из биологического материала, структурно-функциональных исследований нуклеиновых кислот и их комплексов с белками, разработке векторов для позитивной селекции рекомбинантов, получения стерильных трансгенных растений. Перспективным прикладным аспектом использования микробных РНКаз является медицинский. Области их возможного применения связаны с лечением опухолей и вирусных инфекций.
Внеклеточные гуанилспецифичные рибонуклеазы обнаружены у многих видов бацилл, в том числе у Bacillus amyloliquefaciens, B.circulans (барназоподобные РНКазы), В.intermedius, В.pumilus, B.thuringiensis (биназоподобные РНКазы). Ферменты сходны по первичной структуре, близки по физико-химическим и каталитическим свойствам. Однако исследование биосинтеза рибонуклеаз выявило значительные различия в условиях, при которых происходит их накопление в среде, что оставляет открытым вопрос о назначении этих ферментов.
Клонирование и секвенирование генов гуанилспецифичных РНКаз открыло возможность для изучения регуляции их синтеза на уровне транскрипции. Выявление регуляторных механизмов, отвечающих за экспрессию генов в тех или иных условиях, является одной из глобальных проблем молекулярной биологии. Бактерии способны активировать синтез определенных продуктов только в специфической экологической обстановке, либо репрессировать его, если образуемые белки препятствуют другим процессам, протекающим в данный момент в клетке. Регуляция экспрессии генов может также осуществляться как часть процесса дифференцировки и развития клеточной популяции. Информация о путях контроля экспрессии гена важна не только для установления функции кодируемого им белка, но и необходима для осуществления направленного воздействия на геном микроорганизма с целью увеличения выхода желаемого продукта.
Таким образом, знание молекулярных механизмов регуляции синтеза рибонуклеаз позволит создать фундамент для их эффективного использования в прикладных сферах и будет способствовать решению ряда общебиологических проблем, связанных с ролью этих ферментов в основных физиологических процессах клетки.
Целью настоящего исследования явилось выяснение механизмов регуляции экспрессии генов гуанилспецифичных рибонуклеаз бацилл в условиях фосфатного голодания.
В работе решались следующие задачи:
1. Провести поиск у различных видов бацилл ортологов phoP, spo0A и resD генов B.subtilis, продукты которых контролируют специфический ответ на фосфатное голодание.
2. Исследовать взаимодействие фактора транскрипции PhoP B.subtilis с регуляторными областями генов гуанилспецифичных рибонуклеаз бацилл.
3. Определить потенциальные сайты связывания Spo0A и ResD белков в промоторах генов бациллярных рибонуклеаз.
4. Изучить экспрессию генов гуанилспецифичных рибонуклеаз в нативных и дефектных по регуляторным белкам Pho регулона штаммах B.subtilis.
Положения, выносимые на защиту:
- Регулятор транскрипции PhoP B.subtilis - типичный представитель семейства гомологичных белков, контролирующих Pho ответ у различных видов бацилл, может быть использован в качестве модельного белка для изучения связывания с промоторами генов гуанилспецифичных рибонуклеаз.
- Специфическое взаимодействие белка PhoP с промоторами генов рибонуклеаз В.intermedius, В.pumilus, B.thuringiensis позволяет отнести их к новым членам Pho регулона, функционирующего у бацилл в условиях фосфатного голодания.
- Наличие в промоторах генов гуанилспецифичных рибонуклеаз бацилл потенциальных сайтов связывания регуляторных белков ResD и Spo0A и изменение уровня ферментативной активности в соответствующих мутантных штаммах свидетельствует о роли этих белков в экспрессии генов исследуемых РНКаз.
Научная новизна работы. Анализ распространенности среди бацилл двухкомпонентных систем трансдукции сигнала PhoP-PhoR, ResD-ResE и многокомпонентной системы Spo0A-фосфопередачи, контролирующих Pho ответ B.subtilis, выявил высокую консервативность регуляторов ответа и видовые особенности, присущие гистидин киназам. Впервые показано непосредственное связывание основного регулятора Pho ответа бацилл – белка PhoP с промоторами генов рибонуклеаз В.intermedius, В.pumilus, B.thuringiensis, что на молекулярном уровне подтверждает его участие в контроле транскрипции их генов. Кроме того, в регуляторных областях генов рибонуклеаз охарактеризованы потенциальные сайты связывания для Spo0A и ResD белков и получены приоритетные данные об участии данных факторов транскрипции в регуляции экспрессии генов гуанилспецифичных РНКаз.
Практическая ценность работы. Полученные в работе данные о механизмах контроля синтеза внеклеточных рибонуклеаз бацилл могут быть использованы при конструировании экспрессионных систем с целью получения высокоэффективных промышленных штаммов-продуцентов целевых белков. Подобные системы должны включать ген целевого белка под контролем промотора биназоподобной рибонуклеазы и бациллярный штамм-хозяина для его экспрессии, дефектный по негативному регулятору Spo0A. В частности этот подход позволил нам получить суперпродуцент рибонуклеазы В.intermedius, обладающей противоопухолевой и противовирусной активностью. Кроме того, выявленные в работе закономерности важны для общего понимания механизмов функционирования регуляторных систем бациллярной клетки и могут быть использованы в учебном процессе в соответствующих курсах лекций и семинарах для студентов-биологов.
Связь работы с научными программами. Исследования проводились в соответствии с планом НИР КГУ (№ гос. регистрации 01.2.006.09683 «Механизмы функциональной активности клетки») и были выполнены при финансовой поддержке ФЦНТП "Исследования и разработки по приоритетным направлениям развития науки и техники" (Госконтракты 02.434.11.3020, 02.512.11.2050 и 02.512.12.2014), гранта РФФИ 05-04-48182, гранта Правительства Республики Татарстан (2008 г.), программы Международного союза микробиологических сообществ «UNESCO-IUMS-SGM Fellowship».
Апробация работы. Основные положения диссертации представлены на XIII Международной научной конференции «Ферменты микроорганизмов: структура, функции, применение» (Казань, 2005); V Республиканской научно-практической конференции молодых ученых и специалистов «Наука. Инновации. Бизнес» (Казань, 2005); Всероссийской молодежной школе-конференции «Актуальные аспекты современной микробиологии» (Москва, 2005); 10-ой Пущинской школе-конференции молодых ученых, посвященной 50-летию Пущинского научного центра РАН, «Биология – наука XXI века» (Пущино, 2006); I Международной научно-практической конференции «Микробная биотехнология – новые подходы и решения» (Казань, 2007); XIV Международной конференции студентов, аспирантов и молодых ученых «Ломоносов» (Москва, 2007); I Всероссийском, с международным участием, конгрессе студентов и аспирантов биологов «Симбиоз Россия 2008» (Казань, 2008); Первой межуниверситетской конференции по современной биологии «Bionews» (Kazan, 2008); XIV Международной конференции, посвященной 20-летию партнерства между Казанским государственным университетом и Гиссенским университетом им. Ю. Либиха, «Microbial enzymes in biotechnology and medicine» (Kazan, 2009).
Публикации. По материалам диссертации опубликовано 11 работ.
Благодарности. Автор выражает глубокую признательность профессору Колину Харвуду (Университет Ньюкасла, Великобритания) за предоставленную возможность проведения на базе его лаборатории экспериментов по изучению взаимодействия PhoP белка B.subtilis с регуляторными областями генов гуанилспецифичных рибонуклеаз бацилл; профессору Мичико Накано (Университет здоровья и науки Орегона, США) за предоставленные для работы resD-resE мутантные штаммы, а также сердечно благодарит научного руководителя к.б.н., доцента Вершинину Валентину Ивановну за внимательное отношение к работе и всех коллег НИЛ биосинтеза и биоинженерии ферментов кафедры микробиологии КГУ.
Структура и объем диссертации. Диссертация состоит из введения, обзора литературы, описания материалов и методов исследования, изложения результатов исследования, обсуждения результатов, выводов, списка литературы, включающего 218 источника, из них 186 зарубежных, и приложений. Работа изложена на 138 страницах машинописного текста, содержит 9 таблиц и 27 рисунков.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Штаммы бактерий. Escherichia coli BL21 DE3 (F– ompT gal dcm lon hsdSB (rB- mB-) DE3 (lacI lacUV5-T7 ind1 sam7 nin5)), предоставленный проф. К. Харвудом (Университет Ньюкасла, Великобритания) был использован для продукции PhoP и PhoR белков B.subtilis; B.amyloliquefaciens Н2 (проф. Р. Хартли, Национальные институты здоровья, США), B.circulans BCF247 и B.thuringiensis var. subtoxicus В388 (Центр “Биоинженерия” РАН), B.intermedius 7P (Всероссийская коллекция промышленных организмов), B.pumilus KMM62 (ТИБОХ ДВО РАН) - для получения промоторных областей генов гуанилспецифичных рибонуклеаз. Роль регуляторных белков в контроле экспрессии генов РНКаз изучали в штаммах B.subtilis: JH642 (pheAl trpC2), JH646 (pheA1 trpC2 spo0A12), JH647 (pheA1 trpC2 spo0E11) и R15-13 (pheA1 trpC2 abrB23 spo0A12), полученных из Бациллярного генетического стокового центра (Государственный университет Охайо, США); LAB2506 (trpC2 pheA1 resD::cat) и LAB2234 (trpC2 pheA1 resE::spc), предоставленных проф. М. Накано (Университет здоровья и науки Орегона, США).
Плазмиды pET-PhoP и pET-PhoR231 предназначены для получения белка PhoP и цитоплазматического фрагмента белка PhoR B.subtilis в клетках E.coli (проф. К. Харвуд, Университет Ньюкасла, Великобритания); pMZ55, pMZ56, pMZ58, pMZ59 и pMT420 - для экспрессии генов гуанилспецифичных рибонуклеаз B.intermedius (биназа, РНКаза Bi), B.pumilus (РНКаза Bpu), B.thuringiensis (РНКаза Bth), B.circulans (РНКаза Bci) и B.amyloliquefaciens (барназа, РНКаза Ba) соответственно в штаммах B.subtilis (коллекция НИЛ биосинтеза и биоинженерии ферментов КГУ).
Бактерии культивировали на L-бульоне либо бесфосфорной синтетической среде (содержание Фн - 4 мкг/мл) при 37°С с аэрацией. Контроль роста культуры производили путем измерения оптической плотности суспензии при длине волны 590 нм. При необходимости в среды добавляли соответствующие антибиотики: канамицин (10 мкг/мл), спектиномицин (75 мкг/мл), хлорамфеникол (5 мкг/мл – для штамма B.subtilis LAB2506 и 10 мкг/мл – для штаммов, несущих плазмиду pMT420), ампициллин (100 мкг/мл), а для ауксотрофных штаммов - фенилаланин и триптофан (50 мкг/мл).
Выделение хромосомной ДНК из клеток В.subtilis осуществляли с помощью набора реактивов «DNeasy Blood & Tissue Kit» («Qiagen»). Выделение плазмидной ДНК из клеток E.coli и В.subtilis, рестрикцию плазмид, электрофорез ДНК в агарозном геле, а также трансформацию плазмидами компетентных клеток E.coli и B.subtilis проводили стандартными методами [Sambrook and Russell, 2001].
Промоторные области генов рибонуклеаз бацилл и гена ykoL B.subtilis (позитивный контроль для EMSA анализа) амплифицировали в программируемом термостате «Techne TC-512» в реакционной смеси с Platinum Pfx-полимеразой («Invitrogen»), хромосомной ДНК соответствующих видов бацилл и праймерами, представленными в таблице. Состав реакции и условия проведения ПЦР, оптимальные для каждой пары праймер-матрица, подобраны в данной работе. Очистку ПЦР-продуктов проводили с помощью китов «QIAquick PCR Purification Kit» или «QIAquick Gel Extraction Kit» («Qiаgen»).
Таблица
Праймеры для амплификации регуляторных областей генов гуанилспецифичных рибонуклеаз бацилл и гена ykoL B.subtilis
| Праймеры | Промоторы генов для амплификации | Последовательность |
| FBaR | РНКаз Ba и Bci | 5’-GAAAACGTCACATTGC-3’ |
| RBaR | 5’-TCATCATGTGAAGCTG-3’ | |
| FBpR | РНКаз Bi, Bpu Bth | 5’-TTAATCGGAAAAGACG-3’ |
| RBpR | 5’-GAAGCTGTCCTCTTG-3’ | |
| YkoL-FOR | ykoL | 5’- TGAAATGCTGGAGACGTTTATG-3’ |
| YkoL-REV | 5’-TTTTCTAAAGCGGATTTCAATA-3’ |
Белки PhoP-His6 и PhoR-His6 B.subtilis выделяли из цитоплазмы рекомбинантного штамма E.coli, выращенного при 30°С на L-бульоне с добавлением в середине логарифмической фазы роста индуктора ИПТГ (0.5 мМ). Клетки разрушали ультразвуком. Осветленный дезинтеграт клеток наносили на колонку с никель-сефарозой, уравновешенную фосфатным буфером (рН 8.0). Элюцию связавшегося белка проводили в градиенте 20-500 мМ имидазола. Полученный препарат подвергали гель-фильтрации на
сефадексе G-100. Степень чистоты и молекулярный вес белков оценивали с помощью Ds-Na-ПААГ-электрофореза, используя 4%-ый концентрирующий (рН 6.8) и 10%-ый разделяющий (рН 8.8) гели на основе трис-глицинового буфера [Laemmli, 1970].
Масс-спектрометрический анализ очищенных PhoP и PhoR белков проведен на MALDI-TOF масс-спектрометре «Voyager DE-RP» доктором Дж. Греем (лаборатория «Pinnacle», Университет Ньюкасла, Великобритания). Результаты проанализированы с помощью программы «Mascot PMF» (http://www.matrixscience.com).
О ДНК-связывающей активности PhoP белка в отношении промоторов генов гуанилспецифичных рибонуклеаз бацилл судили по изменению электрофоретической подвижности комплекса ДНК–белок – метод EMSA [Allenby et al., 2006].
Способность трансформантов к синтезу РНКазы проверяли по методу Джеффриса. Активность рибонуклеазы РНКазы в культуральной жидкости определяли модифицированным методом Анфинсена по кослоторастворимым продуктам гидролиза РНК [Лещинская с соавт., 1980]. Специфическую активность рассчитывали как отношение общей рибонуклеазной активности к величине биомассы.
Информация о геномах бацилл, нуклеотидных и аминокислотных последовательностях рибонуклеаз и регуляторных белков извлечена из баз данных Виртуального института микробного стресса и выживания «MicrobesOnline» (http://www.microbesonline.org) и Национального центра биотехнологической информации (NCBI, http://www.ncbi.nlm.nih.gov/genomes/lproks.cgi).
Поиск ортологов регуляторных белков B.subtilis проводили с помощью средств сайта «MicrobesOnline». Филогенетические древа были построены методом ближайшего связывания (neighbour-joining) на основе выровненных с помощью программы «MUSCLE» (http://www.drive5.com/muscle) и отредактированных с помощью программы «GBlocks» (http://molerol.cmima.csic.es/castresana/gblocks_server.html) аминокислотных последовательностей.
Потенциальные сайты для взаимодействия регуляторных белков с промоторами генов рибонуклеаз выявляли с помощью программы «Virtual Footprint» (http://www.prodoric.de/vfp/vfp_promoter.php) и визуально, используя их логотипы, представленные в базах «Prodoric» (http://www.prodoric.de) и «DBTBS» (http://dbtbs.hgc.jp ).
Статистическую обработку результатов проводили с использованием пакета программ «Excel 2003». Рассчитывали среднеквадратичное отклонение (), результаты считали достоверными при 10%. При расчете достоверности получаемых разностей использовали t-критерий Стьюдента, принимая Р 0.05 за достоверный уровень значимости.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
1. Ортологи phoP, spo0A и resD генов Bacillus subtilis в секвенированных геномах бацилл.
Известно, что функционирование Pho регулона в условиях дефицита в среде неорганического фосфата контролируется у B.subtilis тремя взаимосвязанными системами [Birkey et al., 1998] - PhoP-PhoR (основная роль в регуляции метаболизма фосфора), ResD-ResE (отвечает за модуляцию процессов аэробного и анаэробного дыхания) и многокомпонентной системой Spo0A-фосфопередачи (инициирует спорообразование). Для того чтобы оценить их роль в регуляции экспрессии генов гуанилспецифичных рибонуклеаз бацилл, на первом этапе работы было необходимо установить, присутствуют ли подобные системы у других представителей рода и насколько они могут быть функционально сходны. Для этого в секвенированных геномах бацилл мы провели поиск ортологов указанных регуляторных систем. Так как у прокариот многие гены являются ксенологами [Lerat et al., 2005; Kunin et al., 2005], было важно оценить вероятность происхождения исследуемых белков в результате горизонтального транспорта генов. Поэтому мы также сравнивали генетический контекст генов [Korbel et al., 2004; Wu et al., 2005] и сопоставляли филогенетические древа бациллярных видов, построенные на основе аминокислотных последовательностей регуляторных белков и гена 16S-рРНК [Price et al., 2007].
Потенциальные ортологи phoP-phoR, resD-resE и spo0A генов B.subtilis были обнаружены у всех бацилл. Генетический контекст phoP-phoR генов бацилл оказался весьма сходным (рис. 1А), в то время как resD-resE и spo0A гены расположены в более вариабельных локусах. Аминокислотные последовательности PhoP белков бацилл были идентичны таковым B.subtilis на 69-88%, PhoR – на 40-71%, ResD - на 73-95%, ResE – на 52-91%, Spo0A - на 75-97%. По степени идентичности аминокислотных последовательностей и сходству организации генетических локусов виды бацилл можно разделить на отдельные группы, преимущественно отражающие филогенетическое родство, что характерно только для истинных ортологов.
В совокупности полученные данные позволяют утверждать, что у различных видов бацилл имеются структурно и функционально сходные PhoP, Spo0A и ResD белки, что позволило нам использовать B.subtilis в качестве модельного организма для изучения регуляции экспрессии генов гуанилспецифичных рибонуклеаз бацилл.
2. Взаимодействие PhoP белка Bacillus subtilis с промоторами генов гуанилспецифичных рибонуклеаз бацилл.
В промоторах генов гуанилспецифичных рибонуклеаз В.intermedius, В.pumilus, B.thuringiensis ранее были обнаружены потенциальные последовательности для связывания PhoP белка B.subtilis и установлено, что
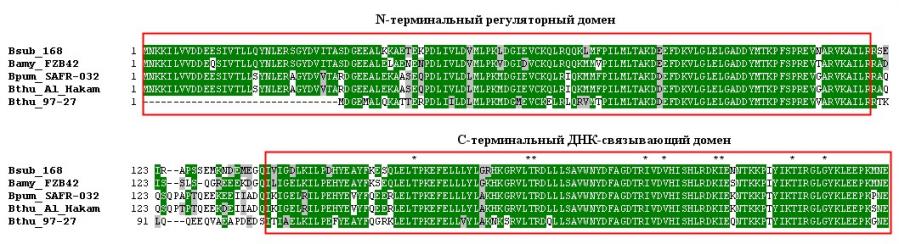
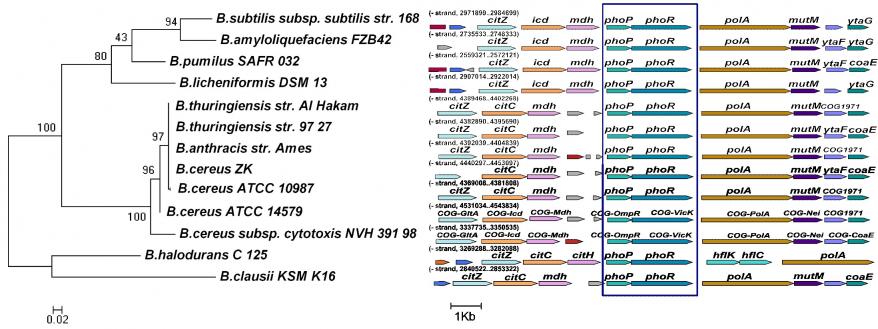
Рисунок 1. Ортологи PhoP белков B.subtilis у различных видов бацилл.
А) Филогенетическое древо, построенное на основе аминокислотных последовательностей PhoP белков бацилл, и генетический контекст кодирующих их генов. Гены phoP-phoR выделены рамкой.
Б) Сравнительный анализ аминокислотных последовательностей PhoP белков бацилл. Функционально значимые аминокислоты ДНК-связывающего домена отмечены звездочкой.
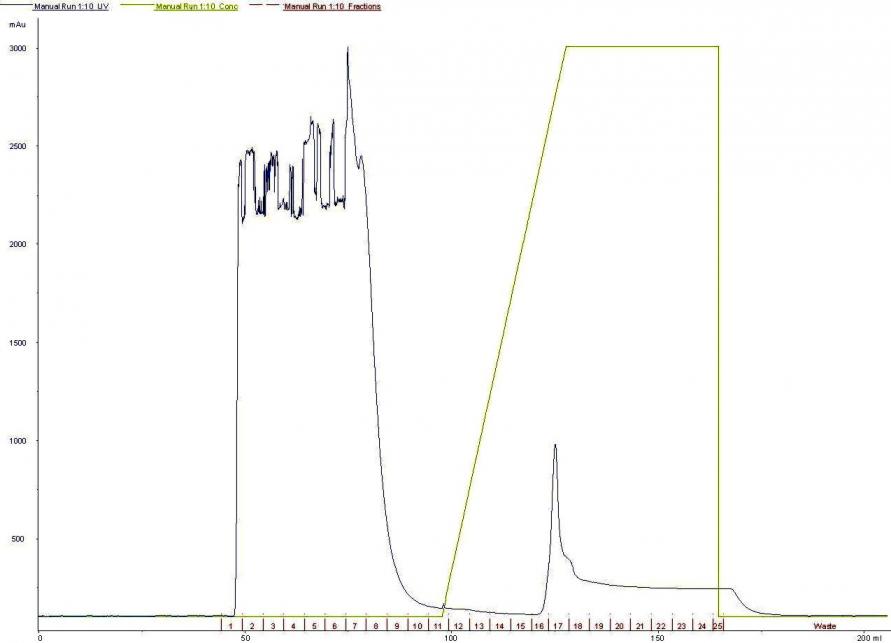

Рисунок 2. Аффинная хроматография осветленного дезинтеграта клеток E.coli, экспрессировавших PhoP-His6 белок B.subtilis, (А) и DS-Na-ПААГ-электрофорез белковых фракций (Б).
экспрессия их генов в рекомбинантных штаммах B.subtilis является PhoP-PhoR-зависимой [Знаменская с cоавт., 1999, Морозова с соавт., 2001], в то время как синтез рибонуклеазы B.circulans хотя и зависел от содержания фосфора в окружающей среде, но не подчинялся контролю со стороны PhoP-PhoR системы. Чтобы сделать окончательный вывод о непосредственном участии PhoP белка в транскрипции генов рибонуклеаз бацилл, было необходимо экспериментально оценить его способность связываться с их промоторными областями.
Проведенный нами сравнительный анализ первичной структуры PhoP белков B.subtilis, B.amyloliquefaciens, B.pumilus и B.thuringiensis показал, что основные различия сосредоточены в линкерной области, соединяющей N- и С-домены белков, в то время как функционально значимые аминокислотные остатки ДНК-связывающих доменов консервативны (рис. 1Б). Это свидетельствует об универсальности взаимодействия этих регуляторов ответа с ДНК-мишенями, поэтому мы использовали PhoP белок B.subtilis для изучения связывания с промоторами генов гуанилспецифичных рибонуклеаз бацилл методом EMSA.
Получение PhoP и PhoR регуляторных белков B.subtilis. Белки PhoP и PhoR B.subtilis были экспрессированы в индуцибельной Т7-системе, включающей конструкцию на основе pET вектора и штамм-реципиент E.coli BL21(DE3). Для оптимизации синтеза рекомбинантных белков была проведена серия экспериментов, в которой варьировали температуру выращивания продуцента, концентрацию вносимого индуктора и время индукции. Эффективным оказалось выращивание бактерий при температуре 30°С и индукция синтеза целевых белков с помощью 0.5 мМ ИПТГ в течение 3 часов. Эти условия были применены для препаративного выделения белков. В результате очистки с помощью металл-хелатной аффинной хроматографии (рис. 2) и последующей гель-фильтрации были получены электрофоретически гомогенные белки (рис. 3). Проведенный масс-спектрометрический анализ препаратов подтвердил, что они являются именно PhoR и PhoP белками B.subtilis.

Рисунок 3. PhoP и PhoR белки B.subtilis, выделенные из рекомбинантных штаммов E.coli.
Условные обозначения: 1 – неиндуцированная культура; 2-3 – растворимые клеточные фракции, содержащие соответственно PhoR и PhoP белки; 4 – PhoR, 5 - PhoP.
ПЦР-амплификация промоторов генов гуанилспецифичных рибонуклеаз. Для получения регуляторных областей генов РНКаз бацилл была выделена их хромосомная ДНК и проведена амплификация необходимых участков с помощью ПЦР. Принимая во внимание сходство промоторных областей генов рибонуклеаз, для их амплификации были использованы две пары праймеров – одна для биназоподобных РНКаз, а другая - для барназоподобных РНКаз (см. табл.). Так как праймеры не были строго специфичными, потребовалась оптимизация условий проведения ПЦР. Для каждого промотора были подобраны концентрации ДНК-матрицы и ионов магния, а также температура отжига праймеров. Полученные фрагменты были очищены и определена концентрация ДНК в препаратах (рис. 4).
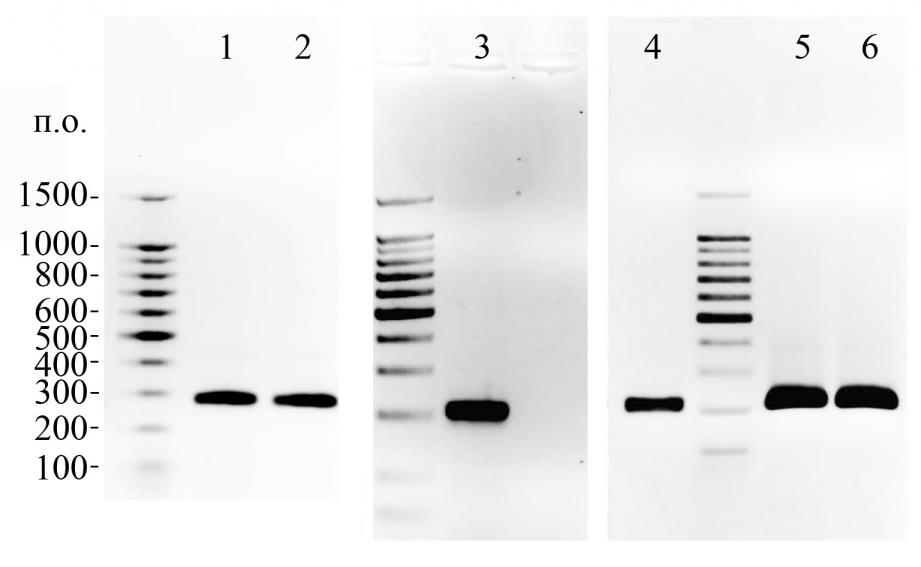
Рисунок 4. Промоторные области генов гуанилспецифичных рибонуклеаз бацилл и гена ykoL B.subtilis, амплифицированные с помощью ПЦР.
Условные обозначения: 1 – B.amyloliquefaciens H2, 2 – B.circulans BCF247, 3 - B.subtilis subsp. subtilis str. 168, 4 – B.intermedius 7P, 5 – B.pumilus KMM62, 6 – B.thuringiensis var. subtoxicus В388.
Анализ изменения электрофоретической подвижности в геле комплекса ДНК–белок. Чтобы доказать непосредственное связывание белка PhoP с промоторами генов рибонуклеаз бацилл, был проведен EMSA-анализ, в котором использовали PhoP белок в активной (фосфорилированной с помощью родственной киназы PhoR) и неактивной формах. Было показано, что регулятор транскрипции PhoP эффективно связывается с промоторами генов РНКаз Вi, Bpu и Bth (рис. 5А), степень взаимодействия зависит от концентрации белка. Фосфорилирование регулятора ответа белком PhoR оказывает незначительное влияние, что объясняется возможным фосфорилированием PhoP с помощью киназ E.coli [Yamamoto et al., 2005; Baek and Lee, 2007]. Промоторы генов РНКаз Ba и Bci не обладали способностью образовывать комплекс с PhoP белком (рис. 5Б).
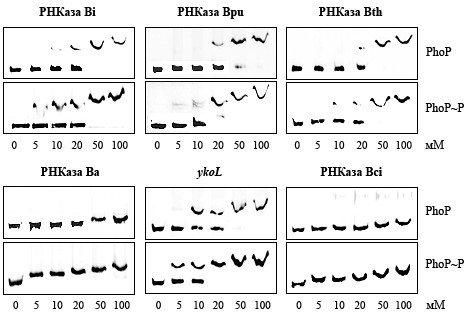
Рисунок 5. Изменение электрофоретической подвижности комплекса белка PhoP с регуляторными областями генов рибонуклеаз бацилл.
А) Промоторы генов рибонуклеаз B.intermedius, B.pumilus и B.thuringiensis.
Б) Промоторы генов рибонуклеазы B.amyloliquefaciens, ykoL B.subtilis (позитивный контроль) и рибонуклеазы B.circulans.
Таким образом, полученные данные о взаимодействии PhoP белка с промоторами генов биназоподобных рибонуклеаз in vitro в совокупности с более ранними результатами по изучению экспрессии их генов в phoP-phoR мутантных штаммах B.subtilis позволяют отнести внеклеточные рибонуклеазы В.intermedius, B.pumilus и B.thuringiensis к новым членам Pho регулона бацилл. Вместе с тем открытым остался вопрос о механизмах регуляции экспрессии генов других гуанилспецифичных рибонуклеаз – РНКаз B.circulans и B.amyloliquefaciens, промоторы которых не способны взаимодействовать с PhoP белком.
3. Сайты связывания регуляторных белков Pho регулона в промоторах генов рибонуклеаз бацилл.
Для обнаружения нуклеотидных последовательностей, определяющих регуляторные механизмы экспрессии генов гуанилспецифичных рибонуклеаз, был проведен сравнительный анализ их промоторных областей на наличие сайтов взаимодействия с регуляторными белками Spo0A и ResD B.subtilis. В промоторных областях генов РНКаз Ва и Вci было выявлено несколько

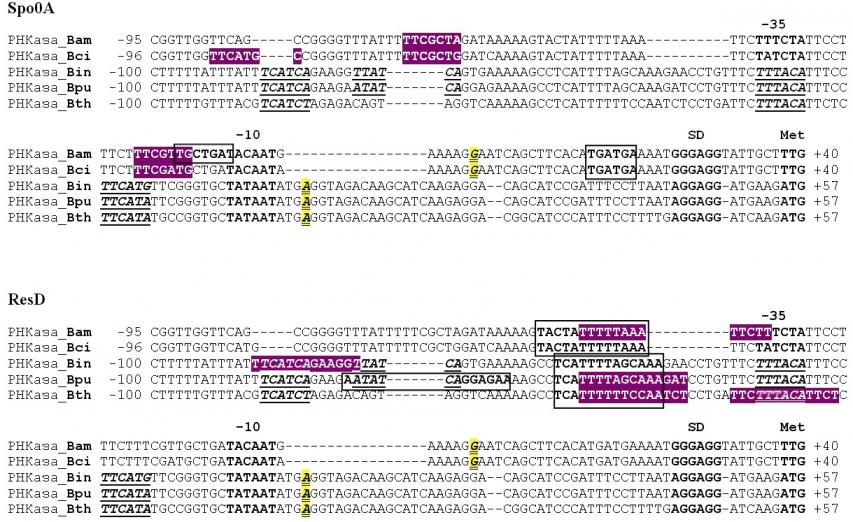
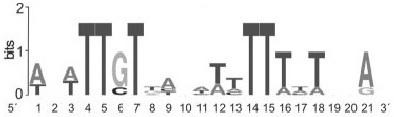
Рисунок 6. Потенциальные сайты связывания регуляторных белков Pho регулона в промоторах генов гуанилспецифичных рибонуклеаз бацилл.
А) Spo0A-последовательности. Б) ResD-последовательности.
Условные обозначения: сайты связывания регуляторных белков на «плюс» цепи выделены рамкой, на «минус» цепи – серым цветом; предполагаемые Pho-боксы подчеркнуты одной линией, точка начала транскрипции – дважды; сверху приведены логотипы Spo0А- и ResD-боксов B.subtilis.
нуклеотидных последовательностей, гомологичных 0A-боксу B.subtilis (рис. 6А). Они отличались от консенсусной 1-3 нуклеотидами. Расположение большинства потенциальных 0А-боксов в промоторах генов РНКаз Ba и Bci практически совпадало, хотя в них были отмечены и небольшие различия. В промоторах генов гуанилспецифичных рибонуклеаз В.intermedius, B.pumilus и B.thuringiensis 0А-подобных сайтов B.subtilis, обнаружено не было. Сайты, гомологичные ResD-связывающим последовательностям B.subtilis, были найдены в промоторах генов всех исследуемых РНКаз, однако количество сайтов и их расположение было различно (рис. 6Б). Таким образом, наличие в промоторах генов гуанилспецифичных рибонуклеаз бацилл потенциальных сайтов для связывания регуляторных белков, указывает на возможную роль данных факторов в регуляции транскрипции генов РНКаз.
4. Экспрессия генов гуанилспецифичных рибонуклеаз в нативных и дефектных по регуляторным белкам Pho регулона штаммах Bacillus subtilis.
Влияние ResD-ResE белков на экспрессию генов рибонуклеаз бацилл в клетках B.subtilis. Чтобы установить, участвуют ли регуляторные белки в контроле экспрессии генов рибонуклеаз, был исследован эффект мутаций в кодирующих их генах на активность РНКаз. Известно, что дефекты в ResD-ResE системе оказывают влияние на экспрессию генов Pho регулона в условиях фосфатного голодания [Sun et al., 1996а]. В наших исследованиях показано, что resD мутация негативно сказывается на уровне продукции биназоподобных рибонуклеаз. Специфическая активность рибонуклеаз Bi, Bpu и Bth в штаммах, дефектных по ResD белку, снижается по сравнению с уровнем РНКазной активности в штамме с полноценной регуляторной системой соответственно на 89, 87 и 94% (рис. 7). Полученные результаты согласуются с данными литературы о специфической активности щелочной фосфатазы, типичного представителя Pho регулона, в resD мутанте, которая также снижается на 80-90% от уровня активности в штамме дикого типа [Hulett, 1996]. Это позволяет сделать вывод о том, что белок ResD задействован в контроле экспрессии генов биназоподобных рибонуклеаз так же, как и других членов Pho регулона, т.е. является позитивным регулятором [Birkey et al., 1998; Schau et al., 2004].
Показано, что делеция гена киназы resE не приводит к утрате ферментативной активности рекомбинантными штаммами B.subtilis, несущими плазмиды с генами биназоподобных рибонуклеаз (рис. 7). Это объясняется тем, что ResD белок может быть фосфорилирован другими сенсорными киназами либо низкомолекулярными донорами фосфата, такими как ацетилфосфат [Laub and Goulian, 2007].
Отсутствие белков двухкомпонентной системы ResD-ResE не оказывает влияния на экспрессию гена РНКазы B.amyloliquefaciens и B.circulans в условиях фосфатного голодания. Однако наличие потенциальных сайтов
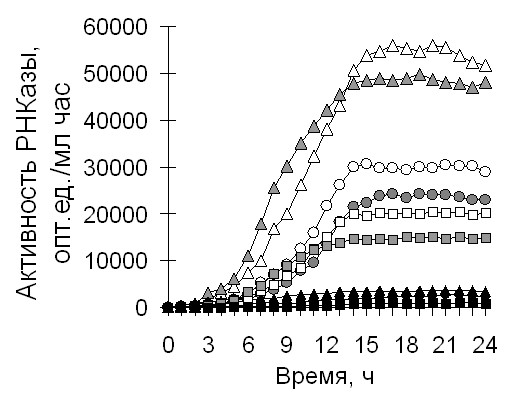
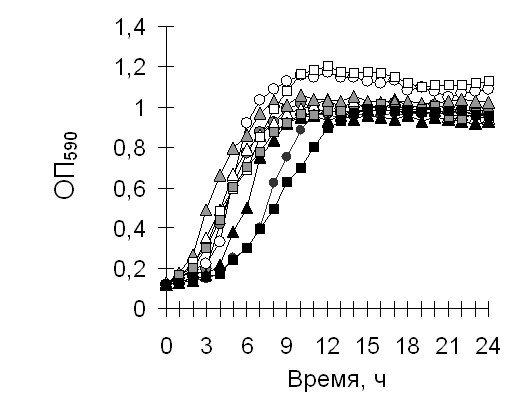
Рисунок 7. Экспрессия генов биназоподобных рибонуклеаз в дефектных по ResD и ResE белкам рекомбинантных штаммах B.subtilis.
А) Рост рекомбинантных штаммов. Б) рибонуклеазная активность.
Условные обозначения: штамм B.subtilis JH642 изображен белым цветом, B.subtilis LAB2234 (resE) – серым, B.subtilis LAB2506 (resD—) – черным; РНКаза Bi кружками, РНКаза Bpu – треугольниками, РНКаза Bth - квадратами.
связывания для белка ResD в промоторах всех гуанилспецифичных рибонуклеаз бацилл, свидетельствует о том, что данный фактор все же может регулировать экспрессию их генов, но, по-видимому, в других условиях.
Роль Spo0A белка в регуляции экспрессии генов рибонуклеаз бацилл в клетках B.subtilis. Исследование влияния Spo0A белка на экспрессию генов гуанилспецифичных рибонуклеаз бацилл проводили в штаммах, несущих мутации в самом гене spo0A (образование функционального регулятора ответа практически невозможно), гене его фосфатазы spo0E (гиперактивная фосфатаза делает Spo0A регулятор неактивным), а также в двойном spo0A/abrB мутанте (возможность проследить AbrB-опосредованный путь функционирования Spo0A белка).
Установлено, что мутация в гене spo0A негативно сказывается на продукции РНКазы Ba. Рибонуклеазная активность как в одиночном, так и в двойном spo0A/abrB мутанте практически отсутствовала (рис. 8). Полученный результат свидетельствует о том, что белок Spo0A является позитивным регулятором экспрессии гена рибонуклеазы B.amyloliquefaciens, и действует независимо от AbrB белка.
Специфическая активность барназы в spo0E мутантном штамме, в котором основная часть Spo0A белка присутствует в неактивной форме, соответствовала контролю (рис. 8). Этот результат в сравнении с тем, что получен с одиночным spo0A мутантом, позволяет полагать, что ген РНКазы Ва, по-видимому, активируется небольшими количествами фосфорилированного Spo0A
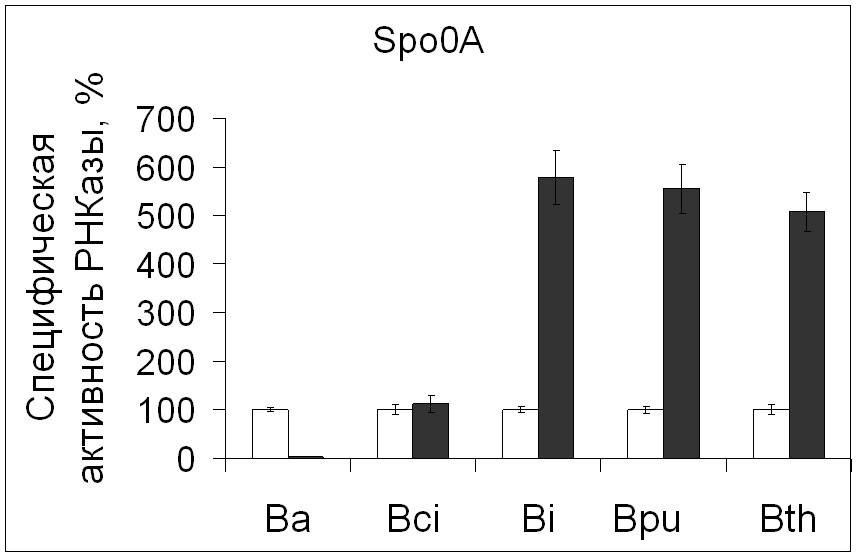
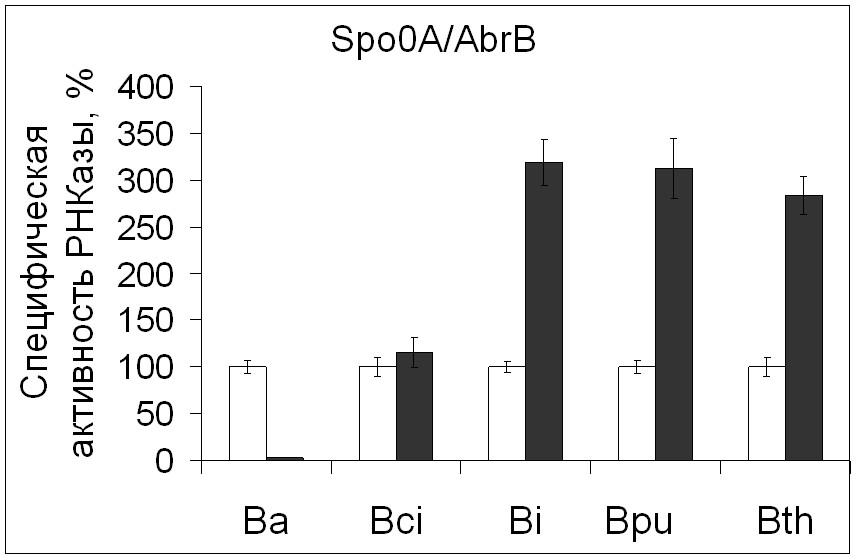
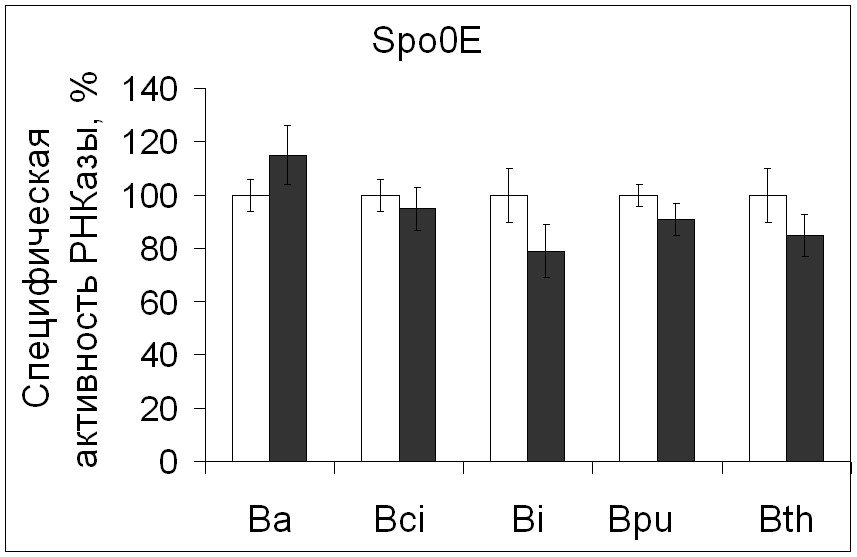
Рисунок 8. Экспрессия генов рибонуклеаз бацилл в рекомбинантных штаммах В.subtilis, дефектных по Spo0A, AbrB и Spo0E белкам.
Условные обозначения: уровень активности фермента в рекомбинантном штамме B.subtilis с полноценными регуляторными белками - белые столбики, активность РНКазы в мутантных штаммах – черные столбики.
регулятора. Присутствуя в клетках в стадии замедления роста в малых количествах, активный Spo0A регулятор выполняет важные функции. Он не только способствует высвобождению вторичных метаболитов, в том числе и гидролитических ферментов и антимикробных веществ, но и принимает участие в регуляции таких важных для популяции бактерий процессов, как бактериальный «апоптоз» и формирование колоний сложного типа - биопленок [Gonzalez-Pastor et al., 2003; Verhamme et al., 2009].
Активность рибонуклеазы Bci в исследуемых мутантных штаммах B.subtilis не отличалась от контроля (рис. 8). Следовательно, ее биосинтез не подвержен действию Spo0A белка. Отсутствие регуляции со стороны основных белков фосфатного регулона, а также альтернативного сигма В фактора [Морозова, 2000], который контролирует у B.subtilis неспецифический ответ на фосфатное голодание [Allenby et al., 2005], свидетельствует о том, что ген фосфат-зависимой рибонуклеазы B.circulans относится к группе малоизученных генов фосфатного стимулона, неспецифически индуцируемых при истощении фосфора в окружающей среде.
Несмотря на то, что в промоторах генов гуанилспецифичных рибонуклеаз В.intermedius, B.pumilus и B.thuringiensis сайтов, подобных 0А-боксам B.subtilis, выявлено не было (рис. 6), не исключена вероятность участия регулятора ответа Spo0A в контроле экспрессии генов этих РНКаз, так как известно, что данный белок контролирует множество процессов в клетке косвенно, влияя на транскрипцию других регуляторных белков, в частности AbrB [Molle et al., 2003].
В наших экспериментах было показано, что Spo0A белок является негативным регулятором экспрессии генов биназоподобных РНКаз, на что указывает значительное повышение РНКазной активности (в 5-6 раз) в Spo0A-дефектных штаммах (рис. 8). В двойных spo0A/abrB мутантах уровень РНКазной активности превышает контрольные значения лишь в 3 раза (рис. 8), что свидетельствует о том, что белок AbrB является позитивным регулятором. Результаты о влиянии Spo0A белка на экспрессию генов биназоподобных РНКаз согласуются с данными литературы для гена щелочной фосфатазы [Hulett, 1996] и подтверждают его AbrB-опосредованный эффект.
Эксперименты с мутантными штаммами не только подтвердили справедливость отнесения генов гуанилспецифичных рибонуклеаз к новым членам Pho регулона, но и способствовали решению практической задачи, нацеленной на получение суперпродуцентов этих важных с практической точки зрения ферментов.
Получение суперпродуцентов бациллярных рибонуклеаз. Существуют различные методы для получения микроорганизмов, характеризующихся способностью к повышенному синтезу целевого белка, которые успешно были применены в отношении бацилл-продуцентов гуанилспецифичных рибонуклеаз. В частности, использование принципов генной инженерии и мутагенеза позволило добиться 5 и 10-кратного увеличения активности биназы по сравнению с природным продуцентом [Балабан с соавт., 1992; Знаменская с соавт., 1999]. В настоящей работе мы предлагаем иной подход, основанный на устранении негативного регулятора синтеза целевого белка. Клонировав мультикопийную плазмиду с геном биназы в Spo0A-дефектный штамм B.subtilis, нам удалось увеличить выход фермента в 30 раз по отношению к природному штамму B.intermedius 7Р. К тому же использование для получения внеклеточных целевых белков spo0A-мутантного штамма-хозяина, имеет ряд неоспоримых преимуществ, в частности нарушения в синтезе протеолитических ферментов у таких бактерий способствуют продукции полноразмерных секретируемых белков [Kodama et al., 2007]. Более того, предложенный подход может быть положен в основу конструирования систем для экспрессии других важных белковых продуктов. Подобные системы должны включать ген целевого белка под контролем промотора биназоподобной рибонуклеазы и Spo0A-дефектный штамм-хозяина.
ВЫВОДЫ
1. Анализ секвенированных геномов бактерий рода Bacillus показал, что ортологи phoP, spo0A и resD генов B.subtilis, продукты которых контролируют специфический Pho ответ, представлены у всех бацилл, что позволило нам использовать B.subtilis в качестве модельного организма для изучения регуляции экспрессии генов гуанилспецифичных рибонуклеаз.
2. Основной регулятор Pho ответа – фактор транскрипции PhoP B.subtilis образует специфический комплекс с промоторами генов рибонуклеаз B.intermedius, B.pumilus и B.thuringiensis и не взаимодействует с промоторами РНКаз B.circulans и B.amyloliquefaciens.
3. В регуляторных областях генов гуанилспецифичных рибонуклеаз выявлены нуклеотидные последовательности, гомологичные сайтам связывания других регуляторных белков Pho регулона: ResD сайты – у всех исследуемых РНКаз, а Spo0А боксы – только у рибонуклеаз B.circulans и B.amyloliquefaciens.
4. В условиях фосфатного голодания экспрессия генов рибонуклеаз B.intermedius, B.pumilus и B.thuringiensis в рекомбинантных штаммах B.subtilis позитивно регулируется белком ResD, и негативно - белком Spo0A. Синтез рибонуклеазы B.circulans не зависит от этих регуляторов, в то время как экспрессия гена РНКазы B.amyloliquefaciens находится под позитивным контролем белка Spo0A.
5. Полученные результаты дают основание считать внеклеточные рибонуклеазы B.intermedius, B.pumilus и B.thuringiensis новыми членами фосфатного регулона, а рибонуклеазу B.circulans, в отличие от близкого структурного гомолога – фосфат-независимой РНКазы B.amyloliquefaciens, следует отнести к участникам неспецифического Pho ответа.
Публикации по теме диссертации
- Ульянова, В. В. Роль Spo0A и AbrB белков в регуляции экспрессии гена рибонуклеазы Bacillus pumilus в рекомбинантных штаммах Bacillus subtilis / В. В. Ульянова, В. И. Вершинина, М. Р. Шарипова // Ферменты микроорганизмов: структура, функции, применение: материалы XIII Международной научной конференции, Казань, 4-8 апр. 2005. - Казань: Казан. гос. ун-т. – С. 86-87.
- Ульянова, В. В. Роль белков системы Spo0A-фосфопереноса в регуляции экспрессии гена биназы в клетках Bacillus subtilis / В. В. Ульянова, В. И. Вершинина // Наука. Инновации. Бизнес: материалы V Республиканской научно-практической конференции молодых ученых и специалистов, Казань, 9 июн. 2005. – Казань: Экоцентр, 2005. – С. 64-65.
- Ульянова, В. В. Роль белков системы Spo0A-фосфопереноса в регуляции экспрессии гена рибонуклеазы Bacillus intermedius в клетках Bacillus subtilis / В. В. Ульянова, В. И. Вершинина // Актуальные аспекты современной микробиологии: тезисы Всероссийской молодежной школы-конференции, Москва, 1-3 нояб. 2005. – С. 81.
- Ульянова, В. В. Экспрессия гена рибонуклеазы B.thuringiensis позитивно регулируется двухкомпонентной системой ResD-ResE B.subtilis / В. В. Ульянова, М. А. Золотова, В. И. Вершинина // Биология – наука XXI века: сб. тез. 10-ой Пущинской школы-конференции молодых ученых, посвященной 50-летию Пущинского научного центра РАН, Пущино, 17-21 апр. 2006. - С. 56.
- Ульянова, В. В. Влияние Spo0A и AbrB белков на экспрессию генов гуанилспецифичных рибонуклеаз Bacillus intermedius и Bacillus pumilus в рекомбинантных штаммах Bacillus subtilis / В. В. Ульянова, В. И. Вершинина, М. А. Харитонова, М. Р. Шарипова // Микробиология. – 2007. – Т. 76, № 5. – C. 639-644.
- Ульянова, В. В. Регуляция экспрессии генов рибонуклеаз Bacillus thuringiensis и Bacillus circulans / В. В. Ульянова, М. А. Золотова, В. И. Вершинина // Материалы докладов XIV Международной конференции студентов, аспирантов и молодых ученых «Ломоносов», Москва, 11-14 апр. 2007. - М.: Издательский центр Факультета журналистики МГУ им. М.В. Ломоносова, 2007. - С. 29-30.
- Ульянова, В. В. Двухкомпонентная система ResD-ResE позитивно регулирует экспрессию генов гуанилспецифичных рибонуклеаз бацилл / В. В. Ульянова, М. А. Золотова, М. А. Харитонова, О. Н. Ильинская, В. И. Вершинина // Молекулярная генетика, микробиология и вирусология. – 2008. - №3. – C. 23-28.
- Ульянова, В. В. Системы, контролирующие специфический ответ бацилл на фосфатное голодание / В.В. Ульянова, В.И. Вершинина // Ученые записки Казанского государственного университета. Серия Естественные науки. – 2008. – Т. 150, кн. 2. – C. 231-244.
- Ульянова, В. В. Участие гуанилспецифичных рибонуклеаз Bacillus thuringiensis и Bacillus circulans в ответе клеток на фосфатное голодание / В. В. Ульянова, В. И. Вершинина // Биология: традиции и инновации в 21 веке: Сб. науч. тр. по материалам I Всероссийского, с международным участием, конгресса студентов и аспирантов биологов «Симбиоз Россия 2008», Казань, 6-10 июл. 2008. – Казань: Изд-во КГУ, 2008. - С. 35-36.
- Ulyanova, V. V. Role of sigma B factor in regulation of binase gene expression in Bacillus subtilis cells / V. V. Ulyanova, E. G. Glazunova, V. I. Vershinina // Building the Future in Biology “Bionews”: Proceedings of the First Interuniversity Conference on Modern Biology, Kazan, 24 Nov. 2008. – Kazan: Kazan State University, 2008. – P. 47.
- Ulyanova, V. V. Interaction of Bacillus subtilis PhoP regulator with promoter regions of guanyl-specific ribonuclease genes / V. V. Ulyanova // Microbial enzymes in biotechnology and medicine: XIV International conference devoted to the 20lh anniversary of partnership between Kazan State University and Justus-Liebig Giessen University, Kazan, 5-7 June 2009. – Kazan: Kazan State University, 2009. - P. 118-119.

