Полимор фны е маркер ы ряда генов системы гемостаза и генетическ ая предрасположенность к неблагоприятному течению ишемической болезни сердца у больных, перенесших острый коронарный синдром.
На правах рукописи

ПУШКОВ АЛЕКСАНДР АЛЕКСЕЕВИЧ
полиморфные маркеры РЯДА генов СИСТЕМЫ ГЕМОСТАЗА и ГЕНЕТИЧЕСКая ПРЕДРАСПОЛОЖЕННОСТь К НЕБЛАГОПРИЯТНОМУ ТЕЧЕНИЮ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА У БОЛЬНЫХ, ПЕРЕНЕСШИХ ОСТРЫЙ КОРОНАРНЫЙ СИНДРОМ.
03.01.03 – молекулярная биология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата биологических наук
Москва – 2011
Работа выполнена в лаборатории молекулярной диагностики и геномной дактилоскопии ФГУП «Государственный научно-исследовательский институт генетики и селекции промышленных микроорганизмов» (ФГУП «ГосНИИ генетика»).
| Научный руководитель: | |
| доктор биологических наук, профессор ФГУП «ГосНИИ генетика», г. Москва | Носиков Валерий Вячеславович |
| Официальные оппоненты: | |
| Доктор биологических наук, профессор Институт молекулярной генетики РАН, г. Москва | Сломинский Петр Андреевич |
| Доктор медицинских наук, ФГУ НИИ физико-химической медицины ФМБА, г. Москва | Явелов Игорь Семенович |
| Ведущая организация | Институт молекулярной биологии им. В.А. Энгельгардта РАН, г.Москва |
Защита состоится « » декабря 2011 г. в 14 часов на заседании Диссертационного совета Д.217.013.01 при ФГУП «Государственный научно-исследовательский институт генетики и селекции промышленных микроорганизмов» по адресу: 117545, Москва, 1-й Дорожный проезд, д. 1.
С диссертацией можно ознакомиться в библиотеке ФГУП «ГосНИИ генетика».
Реферат разослан « » ноября 2011 г.
Ученый секретарь
Диссертационного совета,
кандидат химических наук Т. Л. Воюшина
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы.
Ишемическая болезнь сердца (ИБС) — полигенное, многофакторное заболевание, являющееся наиболее частой причиной смерти среди мужчин старше 45 лет и женщин старше 65 лет во многих странах Европы, в том числе и в России. Больной, перенесший обострение ИБС, попадает в группу высокого риска повторения эпизода обострения. Предотвращение этих заболеваний представляет одну из основных задач, как практической медицины, так и медицинской науки (Оганов и соавт., 2008).
Известно, что сердечно-сосудистые патологии – многофакторные заболевания с многочисленными звеньями патогенеза. Для таких заболеваний характерен сложный механизм формирования фенотипа, в основе которого лежит взаимодействие генетических факторов с факторами внешней среды. При этом для каждого конкретного заболевания можно выделить группу, так называемых, генов-кандидатов, продукты которых могут быть прямо или косвенно вовлечены в развитие данной патологии (Goldbourt et al., 1994).
Генетическую предрасположенность к тому или иному заболеванию чаще всего изучают по принципу “случай-контроль”. Однако для многих исследований этого типа достаточно сложно бывает подобрать правильную контрольную группу, поскольку, во-первых, невозможно бывает выявить доклинические формы проявления заболевания, а во-вторых, учитывать всех умерших к моменту начала обследования. Этих недостатков лишены так называемые проспективные исследования, в которых осуществляется длительное наблюдение за большими группами лиц, входящих в группу риска, с регистрацией «конечных точек» исхода заболевания.
Поскольку нарушения функции системы гемостаза, приводящие к тромбообразованию, являются важным звеном в формировании патогенеза ишемической болезни сердца (Сидоренко и соавт., 2008), гены, кодирующие белковые компоненты этой системы, можно рассматривать как гены-кандидаты, ассоциированные с обострением ИБС, и эти гены совершенно необходимо включать в проспективные исследования.
Установление ассоциации гена с заболеванием и последующая оценка индивидуального генетического риска имеют важное значение для разработки дифференцированного подхода к профилактике и лечению данной патологии и ее осложнений в зависимости от наследственной предрасположенности конкретного пациента. Подобные исследования позволяют точнее и надежнее оценивать генетический риск развития заболевания и прогнозировать его течение (Gibbons et al., 2004).
Цель и задачи работы. Целью данной работы было изучение ассоциации полиморфных маркеров генов-кандидатов, продукты которых являются белковыми компонентами системы гемостаза, с неблагоприятным исходом у больных, перенесших острый коронарный синдром. Для достижения этой цели были поставлены следующие задачи:
- Определить аллели и генотипы полиморфных маркеров генов, кодирующих факторы свертывания крови V (F5) и VII (F7), белок С (PROC), тромбомодулин (THBD) и ингибитор активатора плазминогена типа 1 (PLANH1).
- Провести сравнительный анализ времени дожития до конечных точек у больных, перенесших острый коронарный синдром, - носителей различных генотипов полиморфных маркеров выбранных генов-кандидатов для выявления вклада генетических факторов в развитие неблагоприятных исходов.
Научная новизна работы.
- В данной работе впервые исследована ассоциация полиморфных маркеров Arg506Gln и G5393A гена F5, Arg353Gln гена F7, С(–2676)Т гена PROC, Ala455Val гена THBD и 4G(–675)5G гена PLANH1 с развитием острого коронарного синдрома.
- Обнаружена ассоциация полиморфного маркера G5393A гена F5 с повышенным риском развития неблагоприятного исхода в группе женщин, перенесших острый коронарный синдром. Установлено, что носительство генотипов GA и AA полиморфного маркера G5393A гена F5 независимо связано с наступлением таких неблагоприятных исходов как нефатальный и фатальный инфаркт миокарда (ИМ), а также нефатальный и фатальный инсульт.
- Обнаружена сочетанная ассоциация комбинации генотипов полиморфного маркера Arg353Gln гена F7 и Ala455Val гена THBD с повышенным риском развития неблагоприятного исхода в группе женщин, перенесших острый коронарный синдром.
Практическая ценность работы. Выявление ассоциации полиморфных маркеров генов с развитием острого коронарного синдрома (ОКС) открывает новые перспективы в выделении групп пациентов с высоким риском развития патологии. Полученные данные об ассоциации полиморфных маркеров G5393A гена F5, Arg353Gln гена F7 и Ala455Val гена THBD с повышенным риском развития неблагоприятного исхода в группе женщин, перенесших эпизод обострения ИБС, позволяют внедрить генетическое тестирование больных ИБС для выделения лиц, имеющих максимальную предрасположенность к развитию неблагоприятных исходов, и указывают на возможное направление разработки новых лекарственных средств.
Апробация работы. Диссертационная работа была апробирована на заседании Секции молекулярной биологии Ученого Совета ФГУП «ГосНИИ генетика» 26 октября 2011 г. Материалы работы были представлены на Х-ой ежегодной международной молодежной конференции ИБХФ РАН – ВУЗЫ «Биохимическая физика» (г. Москва, Россия, 8-10 ноября 2010 г); 79-ом съезде Европейского Атеросклеротического общества (г. Гетеборг, Швеция, 26-29 июня 2011); II-ой международной научной конференции студентов, аспирантов и молодых ученых (г. Донецк, Украина, 19-22 сентября 2011 г).
Публикации. По материалам диссертации опубликовано 6 печатных работ, включая 3 статьи, а также материалы конференций.
Структура диссертации. Диссертация состоит из следующих разделов: введение, обзор литературы, описание использованных материалов и методов, результаты и их обсуждение, выводы и список литературы. Материалы диссертации изложены на 127 страницах машинописного текста и содержат 8 таблиц и 15 рисунков. В работе процитированы 185 зарубежных и 23 отечественных литературных источника.
СОДЕРЖАНИЕ РАБОТЫ
1.1. Формирование групп больных. Характеристика и критерии включения.
В исследовании приняло участие 16 медицинских центров из семи городов России (Москва, Казань, Пермь, Челябинск, Ставрополь, Ростов-на-Дону, Санкт-Петербург), исследование проводилось с декабря 2004 г. по август 2010 г. В исследование включены больные (всего 1145 человек), поступившие в стационар в связи с развитием ОКС (Табл. 1). Больные, у которых в результате ОКС не сформировался инфаркт миокарда с зубцом Q, должны были поступить в стационар не позднее 72 ч от момента начала заболевания и иметь хотя бы один из следующих дополнительных критериев:
- депрессия сегмента ST крайней мере на 1 мм в двух соседних отведениях;
- инверсия зубца Т не менее 3 мм;
- транзиторный подъем сегмента ST;
- повышение уровня кардиоспецифических ферментов в крови (сердечная фосфокиназа креатинина, тропонины).
Идентификацию аллелей полиморфных маркеров проводили с помощью гибридизационно-флуоресцентного анализа (TaqMan® анализ)
Таблица 1.
Характеристика группы больных, перенесших острый коронарный синдром.
| Показатель | Группа больных |
| Пол (М/Ж) | 717 / 428 |
| Конечные точки | 452 |
| Возраст, лет* | 61,36 ± 11,70 |
| Курящие | 467 |
| Нестабильная стенокардия/инфаркт миокарда без зубца Q | 663 |
| Инфаркт миокарда с зубцом Q | 550 |
| Рецидив инфаркта во время госпитализации | 21 |
| Эпизоды тяжелой ишемии во время госпитализации | 158 |
| Новые ишемические изменения на электрокардиограме во время госпитализации | 46 |
| * Cредний возраст ± стандартное отклонение. |
1.2. Исследование ассоциации полиморфных маркеров ряда генов-кандидатов с острым коронарным синдромом (ОКС).
1.2.1. Исследование ассоциации полиморфного маркера Arg506Gln гена F5 с ОКС.
Фактор свертывания крови V является независимым от витамина К гликопротеином и играет ключевую роль в коагуляционном каскаде. Активация фактора V происходит за счет его специфичного расщепления тромбином с образованием фактора Vа (Mann and Kalafatis, 2003), активность которого ингибируется в свою очередь за счет ограниченного протеолиза тяжелой цепи фактора Va активированным белком С, выполняющем роль антикоагулянта (Dahlbck and Villoutreix, 2005). Протеолиз фактора Va начинается с расщепления по остатку Arg в положении 506, затем по остаткам Arg в положениях 306 и 679. Инактивация наступает после расщепления по остатку Arg в положении 306 (на этой стадии утрачивается до 90% активности), при этом белок S, выступающий в роли кофактора активированного белка С, значительно ускоряет скорость данной реакции (Norstrm et al., 2003). Таким образом, какие либо изменения в области этих участков расщепления, происходящие в том числе и на генетическом уровне, могут играть ключевую роль в регуляции процессов гемостаза.
Ген фактора V расположен на хромосоме 1q23. В настоящее время в гене фактора V обнаружен целый ряд функционально значимых полиморфных маркеров. Как было показано в ряде работ, причиной устойчивости к действию активированного белка С может быть однонуклеотидный полиморфизм G/A в положении 1691 в гене F5 (Bertina et al., 1994). Данному полиморфному маркеру, получившему название “Лейденовская мутация”, соответствует аминокислотная замена ArgGln в положении 506 полипептидной цепи. Частота данной мутации составляет от 1 до 7% в европейской популяции. Около 95% пациентов с устойчивостью к действию активированного белка С – это носители “Лейденовской мутации” (Tsongalis and Rezuke, 1997), однако, согласно недавно проведенным исследованиям, в европейкой популяции имеется достаточно большой процент людей, устойчивых к действию активированного белка С, у которых данная мутация не выявлена (Tosetto et al., 2004).
Накоплено большое количество данных по ассоциации “Лейденовской мутации” с венозными тромбозами (Tans et al., 2003). Однако работ, посвященных ассоциации данного полиморфного маркера с развитием артериальных тромбозов и других сердечно-сосудистых патологий, имеется значительно меньшее количество, а их результаты носят противоречивый характер (Ridker et al., 1995; Mannucci et al., 2010).
Кроме того, большинство работ до настоящего времени проводилось с использованием подхода «случай-контроль», который имеет определенные ограничения при формировании контрольных групп пациентов. Таким образом, основываясь на имеющихся результатах, можно сделать вывод о необходимости проведения длительного проспективного исследования для выяснения индивидуальной роли данного полиморфного маркера в патогенезе сердечно-сосудистых заболеваний.
Нами были определены частоты генотипов полиморфного маркера Arg506Gln гена F5 у всех пациентов (Табл. 2).
Таблица 2.
Частоты генотипов полиморфного маркера Arg506Gln гена F5 у больных, перенесших ОКС.
| Генотип | Число пациентов | Частота, % |
| Arg/Arg | 1069 | 93,4 |
| Arg/Gln | 76 | 6,6 |
| Gln/Gln | 0 | 0 |
| Всего | 1145 | 100 |
Частоты аллелей в изучаемой нами группе больных были близки к частотам, наблюдаемым у европейцев. Среди исследуемых пациентов нами не было обнаружено ни одного носителя «Лейденовской мутации» в гомозиготной форме. Проведенный нами анализ выживаемости пациентов показал, что риск развития неблагоприятного исхода после перенесенного острого коронарного синдрома не зависит от генотипов полиморфного маркера Arg506Gln гена F5. Эти результаты можно объяснить малым числом пациентов, носителей аллеля Gln, и отсутствием пациентов с генотипом Gln/Gln. Можно предположить, что носители данного генотипа не попали в нашу выборку по причине наступления неблагоприятного исхода еще до начала исследования. У тех же носителей «Лейденовской» мутации, которые были включены в наше исследование, развитие неблагоприятных исходов связано с другими патофизиологическими механизмами.
1.2.2. Исследование ассоциации полиморфного маркера G5393A гена F5 с ОКС.
Полиморфный маркер G5393A (rs7542281) расположен в интроне 3 гена F5. Ранее была показана ассоциация данного полиморфного маркера с неблагоприятным течением ИБС на популяции финнов (Auro et al., 2007).
Частоты генотипов полиморфного маркера G5393A гена F5 были определены нами у всех пациентов (Табл. 3). Ассоциации с развитием неблагоприятных исходов у больных, перенесших ОКС, обнаружено не было.
Таблица 3.
Частота генотипов полиморфного маркера G5393A гена F5 у больных, перенесших ОКС.
| Генотип | Число пациентов | Частота, % |
| GG | 576 | 50,4 |
| GA | 480 | 41,9 |
| AA | 89 | 7,8 |
| Всего | 1145 | 100 |
При проведении проспективных исследований с использованием «конечных точек» необходимо учитывать влияние полового диморфизма на патогенез развития заболевания (Silander et al., 2008). Так, в проведенном нами ранее проспективном исследовании, была выявлена ассоциация полиморфного маркера C(–1654)T гена PROC с неблагоприятными исходами в группе больных, перенесших острый коронарный синдром, при этом более сильная ассоциация наблюдалась в группе мужчин (Агапкина и соавт., 2010).
Принимая во внимание данные результаты, дальнейшее исследование ассоциации полиморфного маркера G5393A гена F5 с риском развития НИ проводили с разделением пациентов на группы по половому признаку.
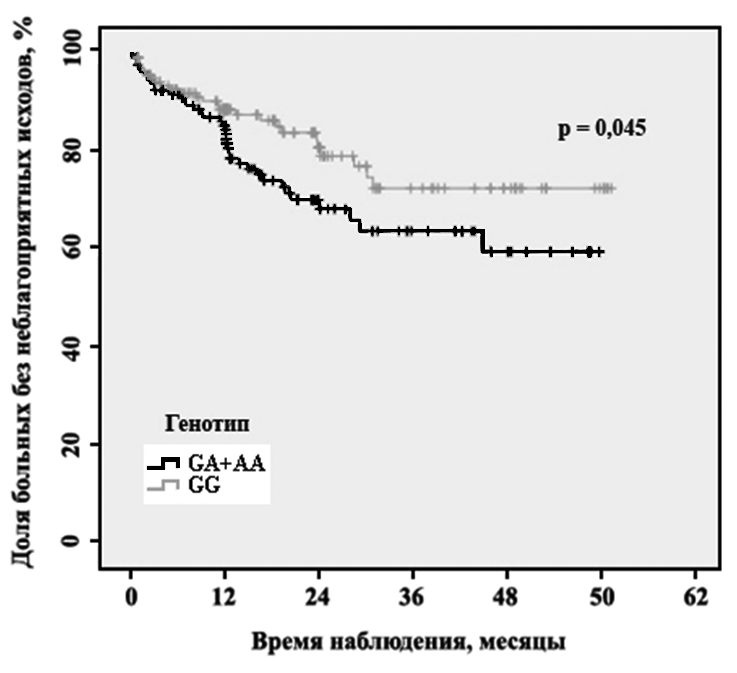
Рис. 1. График Каплана-Майера. Доля неблагоприятных исходов у женщин носителей генотипов GG и GA+AA полиморфного маркера G5393A гена F5 в зависимости от времени, прошедшего после ОКС.
Анализ времени дожития до конечной точки у носителей различных генотипов полиморфного маркера G5393A гена F5 показал, что в группе женщин носителей генотипов GA и AA за период наблюдения чаще наблюдался неблагоприятный исход (фатальный и нефатальный ИМ, фатальный и нефатальный инсульт), чем в группе гомозиготных носителей аллеля G. Время дожития до конечной точки составило 42,7 месяцев (95% CI 38,0-47,5) против 49,5 месяцев (95% CI 45,1-53,9) (2 = 4.15 р = 0.045) (Рис. 1). В группе мужчин данной ассоциации обнаружено не было, у носителей разных генотипов частоты развития неблагоприятных исходов не отличались.
Таким образом, полученные нами данные об ассоциации полиморфного маркера G5393A гена F5 с риском развития НИ в группе женщин, перенесших ОКС, согласуются с данными европейских исследований и подтверждают важную роль полового диморфизма в патогенезе развития ИБС, а также свидетельствуют в пользу необходимости внедрения генетического тестирования больных ИБС для выявления лиц, имеющих максимальную предрасположенность к развитию неблагоприятных исходов.
1.2.3. Исследование ассоциации полиморфного маркера Arg353Gln гена F7 с ОКС.
Фактор VII (проконвертин) представляет собой гликопротеин, зависимый от витамина К. Активная форма фактора VII – это сериновая протеаза, первый фермент в каскаде свёртывания крови по «внутреннему пути» (Долгов и Свирин, 2005). Активация данного пути играет ключевую роль в процессе гемостаза, в связи с чем, повышенная концентрация фактора VII может способствовать развитию тромботических событий (Зубаиров и соавт., 2000), при этом на концентрацию фактора VII в крови влияют как генетические факторы, так и приобретённые состояния.
Ген F7, кодирующий фактор свертывания VII, расположен на хромосоме 13q34. Проведены обширные исследования по выяснению роли гена F7 в патогенезе ИБС. Обнаружена ассоциация нескольких полиморфных маркеров гена F7 с уровнем фактора VII в плазме крови. Из них наиболее изучен полиморфный маркер G/A в положении 10976 (rs6046), которому соответствует аминокислотный полиморфизм Arg/Gln в положении 353 полипептидной цепи. Этот полиморфный маркер расположен в области, кодирующей каталитический домен фактора VII, и, по некоторым данным, у носителей аллеля Gln ниже риск развития неблагоприятного течения ИБС. Тем не менее, проведенные на различных популяциях исследования возможной ассоциации данного полиморфного маркера с сердечно–сосудистыми заболеваниями носят противоречивый характер. Так, Джирелли с соавт. (2000) было обнаружено, что аллель Gln ассоциирован с уменьшением риска развития ИМ. В китайской популяции при сравнении группы больных ИБС с контрольной группой ассоциация данного полиморфного маркера с ИБС не была обнаружена, в том числе и при разбиении групп по половому признаку. Частота аллеля Gln была выше в группе больных ИБС по сравнению с группой больных с ИБС и ИМ (Xu et al., 2003). Однако, при исследовании небольшой выборки пожилых пациентов с ИБС и контрольной здоровой группы было показано, что уровень фактора VII в плазме крови достоверно различался между двумя группами. При этом он был значительно ниже у носителей аллеля Gln (Lu et al., 2005). Среди 139 семей с ИБС в анамнезе, проживающих на территории Индии, пониженный уровень фактора VII в плазме крови положительно коррелировал с носительством аллеля Gln (Shanker et al., 2009) Такие же данные были получены среди новорожденных детей в нескольких популяциях, проживающих в Сингапуре (Quek et al., 2006).
Частоты генотипов полиморфного маркера Arg353Gln гена F7 были определены нами у всех пациентов (Табл. 4). Ассоциации с развитием неблагоприятных исходов у больных, перенесших ОКС, обнаружено не было. Принимая во внимание половой диморфизм подверженности ИБС, дальнейшее исследование проводили с разделением пациентов на группы по половому признаку. При этом в группе женщин нами была выявлена тенденция к увеличению числа неблагоприятных исходов у носителей генотипа Arg/Arg полиморфного маркера Arg353Gln гена F7 (р = 0,215) (Рис. 2). В группе мужчин подобной тенденции не наблюдалось, у носителей разных генотипов частоты развития неблагоприятных исходов не отличались. Эти данные подтверждают полученные ранее результаты об ассоциации аллеля Gln полиморфного маркера Arg353Gln гена F7 с пониженным риском развития неблагоприятного течения ИБС (Girelli et al., 2000; Lane et al., 1996). Возможно, у носителей аллеля Gln понижен уровень удельной активности фактора VII в плазме крови, а также имеет место некоторое снижение его секреции, что было обнаружено в ряде исследований (Ghaddar et al., 1998; Kathiresan et al., 2006).
Таблица 4.
Частота генотипов полиморфного маркера Arg353Gln гена F7 у больных, перенесших ОКС.
| Генотип | Число пациентов | Частота, % |
| Arg/Arg | 887 | 77,5 |
| Arg/Gln | 238 | 20,8 |
| Gln/Gln | 19 | 1,7 |
| Всего | 1145 | 100 |
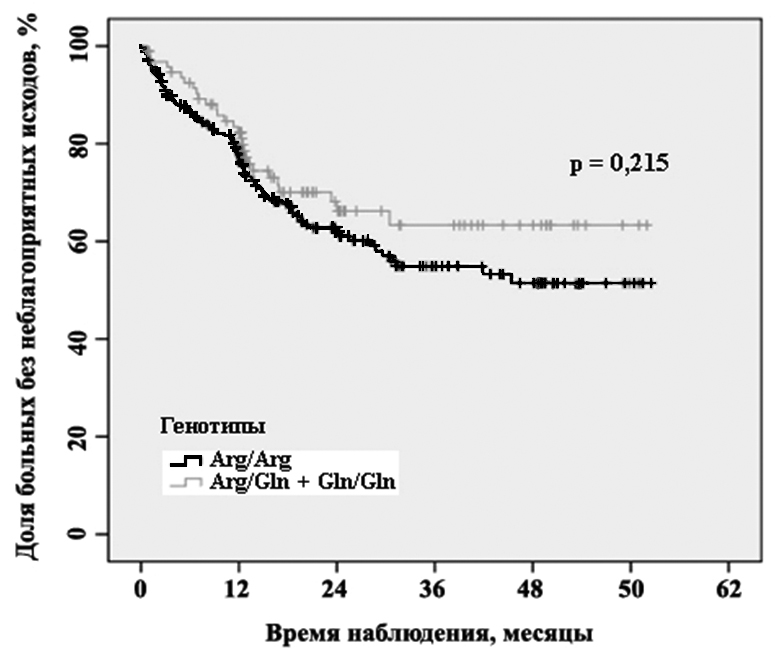
Рис. 2. График Каплана-Майера. Доля неблагоприятных исходов у женщин носителей генотипов Arg/Arg и Arg/Gln+Gln/Gln полиморфного маркера Arg353Gln гена F7 в зависимости от времени, прошедшего после ОКС.
1.2.4. Исследование ассоциации полиморфного маркера Ala455Val гена THBD с ОКС.
Тромбомодулин - интегральный гликопротеин мембран клеток, участвующий в связывании тромбина. Тромбомодулин является ключевым звеном серии реакций, регулирующих направление и скорость процессов гемостаза (Dittman and Majerus, 1990).
Ген тромбомодулина расположен на хромосоме 20р11.2. Обнаружена ассоциация нескольких полиморфных маркеров гена THBD с развитием сердечно-сосудистых заболеваний. Одним из них является полиморфный маркер С/Т в положении 1578 (rs1042579), которому соответствует аминокислотный полиморфизм Ala/Val в положении 455 полипептидной цепи. Данные об ассоциации этого полиморфного маркера с развитием ИБС, имеющиеся в настоящее время, неоднозначны (Wu et al., 2001; Сидоренко и соавт., 2006). Ряд исследований, проведенных по типу случай-контроль, выявили ассоциацию аллеля Val с ИМ, в том числе и его манифестацией в раннем возрасте, при этом генетическая составляющая вносила наибольший вклад в случае пациентов-курильщиков, а также в группе афроамериканцев (Konstantoulas et al., 2004).
Однако функциональное значение данного полиморфизма остается не до конца ясным, поскольку он не влияет на уровень тромбомодулина в плазме крови, что было показано в исследованиях в условиях in vivo (Nakabayashi et al., 1999). Возможно, наличие остатков аланина или валина в положении 455 полипептидной цепи молекулы тромбомодулина, в домене EGF-6, непосредственно связывающем тромбин, приводит к различиям в пространственной ориентации последнего на поверхности эндотелия, что в свою очередь изменяет скорость активации белка С (Aleksic et al., 2003; Yang et al., 2003).
Нами были определены частоты генотипов полиморфного маркера Ala455Val гена THBD у всех пациентов (Табл. 5).
Таблица 5.
Частоты генотипов полиморфного маркера Ala455Val гена THBD у больных, перенесших ОКС.
| Генотип | Число пациентов | Частота, % |
| Ala/Ala | 740 | 64,6 |
| Ala/Val | 365 | 31,9 |
| Val/Val | 40 | 3,5 |
| Всего | 1145 | 100 |
Проведенный анализ выживаемости пациентов показал, что риск развития неблагоприятного исхода после перенесенного острого коронарного синдрома не зависит от генотипов полиморфного маркера Ala455Val гена THBD. Кривые выживаемости больных с различными генотипами полиморфного маркера Ala455Val гена THBD существенно не различались (Рис. 3). При разделении пациентов на группы по половому признаку, в группе женщин наблюдалась слабая тенденция к увеличению числа НИ у носителей аллеля Val.
Полученные нами данные об отсутствии статистически значимой ассоциации генотипов полиморфного маркера Ala455Val гена THBD с риском развития НИ согласуются с данными, полученными в ряде европейских проспективных исследований (Auro et al., 2007). Исходя из этого, можно сделать вывод о том, что полиморфный маркер Ala455Val гена THBD не имеет индивидуального прогностического значения в оценке риска развития неблагоприятных исходов у больных, перенесших обострение ИБС. Для проведения дальнейших исследований наиболее целесообразен комплексный подход с использованием комбинации генотипов других полиморфных маркеров гена THBD.
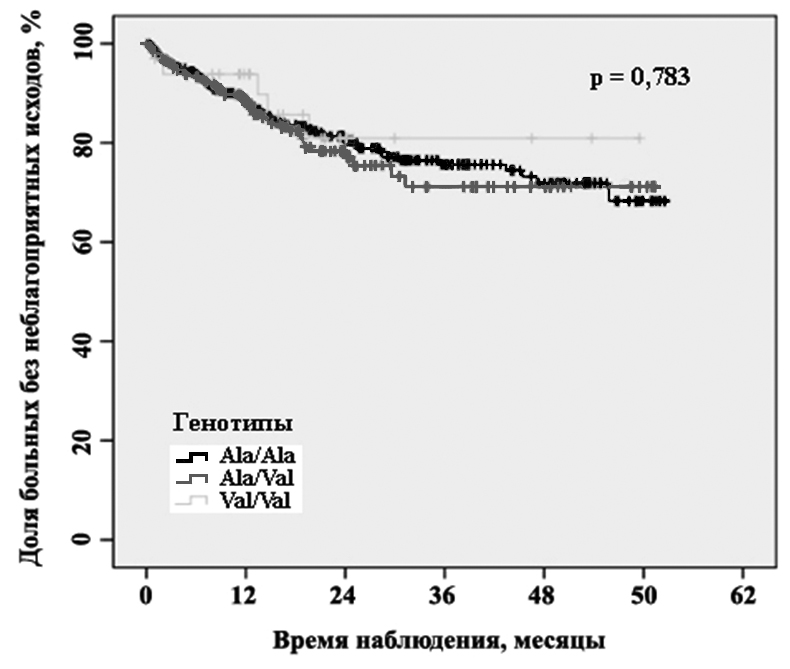
Рис.3. График Каплана-Майера. Доля неблагоприятных исходов у носителей различных генотипов полиморфного маркера Ala455Val гена THBD в зависимости от времени, прошедшего после ОКС.
1.2.5. Исследование сочетанной ассоциации полиморфного маркера Ala455Val гена THBD и полиморфного маркера Arg353Gln гена F7 с ОКС.
Важную прогностическую роль в проспективных исследованиях с использованием «конечных точек» может играть изучение совместного влияния комбинации генотипов нескольких полиморфных маркеров. Данный подход широко применяется как в современных зарубежных исследованиях (Auro et al., 2007), так и в России. Наши последние данные, полученные в результате длительного проспективного исследования на группе больных, перенесших обострение ИБС, выявили значительную сочетанную ассоциацию комбинаций генотипов полиморфных маркеров генов, продукты которых участвуют в регуляции воспаления, с развитием НИ (Благодатских и соавт., 2011).
Основываясь на этих данных, в проведенном нами многоцентровом проспективном исследовании был применен комплексный подход с использованием комбинаций генотипов исследуемых полиморфных маркеров. Поскольку тенденция к изменению числа НИ в зависимости от генотипов как полиморфного маркера Arg353Gln гена F7, так и полиморфного маркера Ala455Val гена THBD наблюдалась нами только в группе женщин, дальнейшее исследование проводили, учитывая эти результаты. Исследовалось две группы женщин. В первую были включены носители генотипов Ala/Val и Val/Val полиморфного маркера Ala455Val гена THBD и генотипа Arg/Arg полиморфного маркера Arg353Gln гена F7, во вторую группу носители генотипа Ala/Ala полиморфного маркера Ala455Val гена THBD и генотипов Arg/Gln и Gln/Gln полиморфного маркера Arg353Gln гена F7 (Табл. 6).
Таблица 6.
Характеристика групп больных, перенесших острый коронарный синдром, при исследовании совместного влияния полиморфных маркеров генов THBD и F7
(2 = 4,15, р = 0,042).
| Название группы | Генотипы полиморфных маркеров | Число пациентов | Время дожития, месяцы (95% CI) | |
| Ala455Val гена THBD | Arg353Gln гена F7 | |||
| Г1 | Ala/Val Val/Val | Arg/Arg | 95 | 40.5 (33,5-47,6) |
| Г2 | Ala/Ala | Arg/Gln Gln/Gln | 50 | 51.6 (45.0-58.1) |
В первой группе чаще наблюдался неблагоприятный исход (нефатальный и фатальный инфаркт миокарда, нефатальный и фатальный инсульт) по сравнению со второй группой. Время дожития до конечной точки в первой группе составило 40.5 месяцев (95% CI 33,5-47,6) против 51.6 месяцев (95% CI 45.0-58.1) во второй группе (2 = 4.15 р = 0.042) (Рис. 4).
Полученные нами результаты в группе женщин, перенесших обострение ИБС, подтверждают целесообразность использования такого подхода. Меньшее время дожития до конечной точки и увеличение числа неблагоприятных исходов у пациентов первой группы, возможно, связаны как с более высоким уровнем активности фактора VII у носителей генотипа Arg/Arg гена F7, так и с влиянием аллеля Val гена THBD на скорость активации белка С. Носительство аллеля Gln гена F7 и генотипа Ala/Ala гена THBD приводят, в свою очередь, к статистически достоверному уменьшению числа НИ во второй группе.
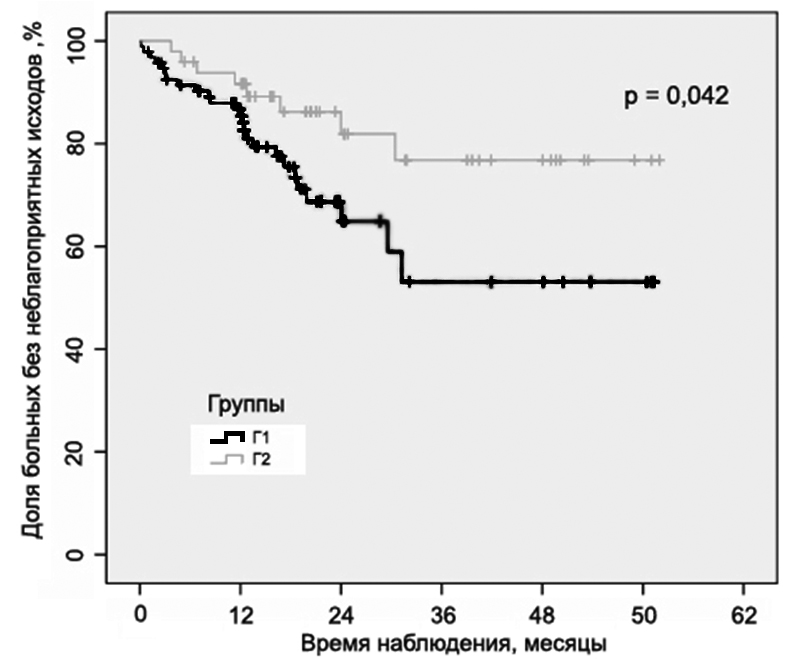
Рис. 4. График Каплана-Майера. Доля неблагоприятных исходов у женщин носителей различных генотипов полиморфных маркеров Ala455Val гена THBD и Arg353Gln гена F7, в зависимости от времени, прошедшего после ОКС.
1.2.6. Исследование ассоциации полиморфного маркера С(–2676)Т гена PROC с ОКС.
Белок C является предшественником сериновой протеиназы. Активированный белок C выполняет функции антикоагулянта. Он инактивирует факторы свертывания Va и VIIIa путем их ограниченного протеолиза и таким образом подавляет образование тромбов и воспалительные реакции. Важная роль белка С в регуляции гемостаза подтверждается множеством клинических наблюдений, свидетельствующих о том, что его наследственный дефицит ведет к развитию тромбозов различной степени тяжести уже в молодом возрасте (Folsom et al., 2002).
Также показано, что белок С вызывает увеличение концентрации тканевого активатора плазминогена, за счет нейтрализации его ингибитора. Таким образом, под действием белка С происходит сдвиг равновесия между тканевым активатором плазминогена и ингибитором активатора плазминогена типа 1 в сторону активатора, что приводит к увеличению фибринолитической активности крови (Сидоркина, 2001). Кроме того, активированный белок С участвует в регуляции воспалительного процесса, ингибируя продукцию цитокинов макрофагами, а так же оказывает цитопротективный эффект (Mosnier et al., 2007). Эти данные подтверждают исключительно важную роль белка С в регуляции гемостаза.
В промоторной области, кодирующего белок С гена PROC, расположенного на хромосоме 2q13–q14, обнаружено несколько полиморфных маркеров: C(–1654)T, A(–1641)G, A(–1476)T и C(–2676)T. Данных об ассоциации этих полиморфных маркеров гена PROC с развитием ИБС в литературе совсем немного. Впервые они были изучены Спеком и соавт. в 1995 году, при этом все исследования за последние 10 лет проводились по принципу «случай-контроль» на выборках сравнительно небольшого объема (Aiach et al., 1999; Mahmoodi et al., 2008). Минорный аллель C полиморфного маркера C(–2676)T, как было показано в недавно проведенном крупном исследовании, был ассоциирован с пониженным уровнем белка С, однако при этом не влиял на неблагоприятное течение ИБС в группе исследуемых пациентов (Reiner et al., 2008).
Принимая во внимание полученные нами ранее результаты об ассоциации полиморфного маркера C(–1654)T, расположенного в промоторной области гена PROC, с повышенным риском развития неблагоприятного исхода в группе больных, перенесших эпизод обострения ИБС (Агапкина и соавт., 2010), для изучения ассоциации гена PROC с развитием неблагоприятных исходов нами был выбран другой полиморфный маркер этого гена — C(-2676)T.
Нами были определены частоты генотипов полиморфного маркера C(-2676)T гена PROC у всех пациентов (Табл. 7).
Таблица 7.
Частоты генотипов полиморфного маркера C(-2676)T гена PROC у больных, перенесших ОКС.
| Генотип | Число пациентов | Частота, % |
| TT | 430 | 37,6 |
| TC | 517 | 45,1 |
| CC | 198 | 17,3 |
| Всего | 1145 | 100 |
Проведенный анализ выживаемости пациентов показал, что риск развития неблагоприятного исхода после перенесенного острого коронарного синдрома не зависит от генотипов полиморфного маркера C(-2676) гена PROC. Кривые выживаемости больных с различными генотипами полиморфного маркера C(-2676) гена PROC существенно не различались (рис. 5).
Эти данные свидетельствуют о том, что полиморфный маркер C(–2676)T гена PROC не ассоциирован с развитием неблагоприятного исхода у больных, перенесших ОКС.
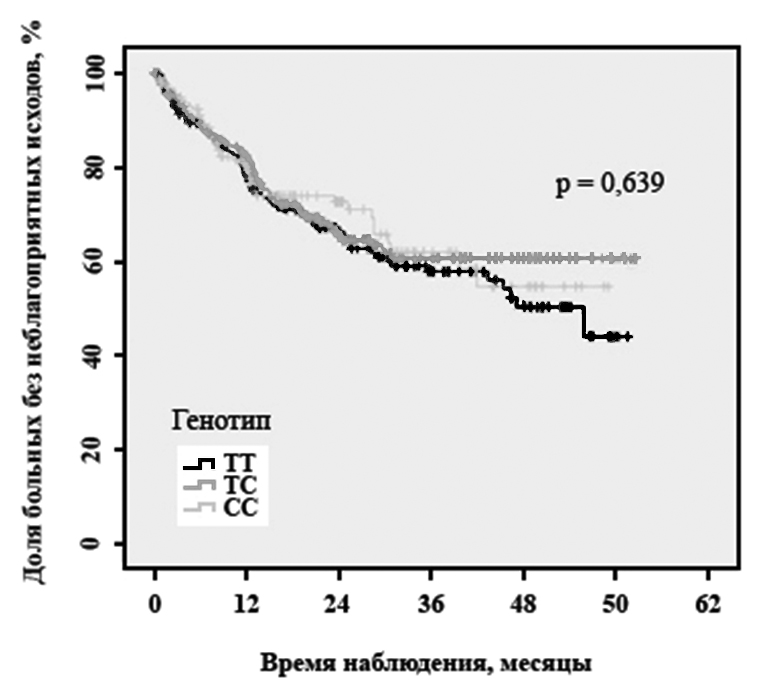
Рис.5. График Каплана-Майера. Доля неблагоприятных исходов у носителей различных генотипов полиморфного маркера C(-2676) гена PROC в зависимости от времени, прошедшего после ОКС.
1.2.7. Исследование ассоциации полиморфного маркера 4G(-675)5G гена PLANH1 с ОКС.
Ингибитор активатора плазминогена типа 1 (PAI-1) является главным физиологическим ингибитором активатора плазминогена тканевого типа (t-PA). Биологическая система активатор плазминогена/плазмин является фибринолитической системой, основная функция которой - запуск защитных механизмов, предотвращающих образование тромба. Активность этой системы зависит от уровня специфичной протеазы, плазмина, который образуется из неактивного предшественника плазминогена под действием его активаторов. Активация плазминогена, в свою очередь, регулируется посредством присутствующих в плазме крови специфичных ингибиторов активатора плазминогена. Наиболее значимым из таких ингибиторов является ингибитор активатора плазминогена типа 1 (Yamamoto et al., 2005). PAI-1 секретируется в кровь эндотелием сосудов и является ингибитором t-PA и урокиназы. Принято считать, что повышенная концентрация PAI-1 ассоциирована с неблагоприятным течением атеротромбоза (Sobel et al., 2003).
В гене PLANH1, кодирующем PAI-1, обнаружен полиморфный маркер 4G/5G в положении -675 (rs1799762). Данный полиморфный маркер расположен в промоторной области гена в районе участка связывания белка — активатора транскрипции и, по некоторым данным, у носителей аллеля 4G повышен риск развития сердечно-сосудистых заболеваний (Loew et al., 2006). К настоящему моменту проведены достаточно обширные исследования по выяснению роли гена PLANH1 в патогенезе сердечно–сосудистых заболеваний в различных популяциях. Однако, данные об ассоциации полиморфного маркера 4G(-675)5G гена PLANH1 с риском развития ИБС являются крайне противоречивыми (Затейщиков и соавт., 2002).
Частоты генотипов полиморфного маркера 4G(-675)5G гена PLANH1 были определены у всех пациентов (Табл. 8). Частоты аллелей в изучаемой нами группе больных были близки к частотам, наблюдаемым у европейцев (Rossaak et al., 2000).
Проведенный анализ выживаемости пациентов показал, что риск развития неблагоприятного исхода после перенесенного острого коронарного синдрома не зависит от генотипов полиморфного маркера 4G(-675)5G гена PLANH1 (p = 0,604) (Рис. 6). При разделении нами исследуемой выборки на мужчин и женщин ассоциация с неблагоприятными исходами также не была обнаружена.
Таблица 8.
Частоты генотипов полиморфного маркера 4G(-675)5G гена PLANH1 у больных, перенесших обострение ИБС.
| Генотип | Число пациентов | Частота, % |
| 4G4G | 378 | 33 |
| 4G5G | 550 | 48 |
| 5G5G | 217 | 19 |
| Всего | 1145 | 100 |
По данным, полученным разными исследователями, уровень PAI–1 примерно на 25% выше у носителей генотипа 4G/4G, по сравнению с носителями генотипа 5G/5G (Lane and Grant, 2000). В течение последних лет в большинстве исследований обнаружено наличие повышенного уровня PAI–1 в плазме крови у пациентов с ИБС, особенно у лиц, перенесших ИМ (Sabino et al., 2011).
Отсутствие ассоциации генотипов полиморфного маркера 4G(-675)5G гена PLANH1 с развитием неблагоприятных исходов в группе больных ИБС, перенесших острый коронарный синдром, согласуется с данными, полученными в крупномасштабных исследованиях последних лет (Koch et al., 2010) и говорит об отсутствии индивидуальной прогностической значимости данного полиморфного маркера.
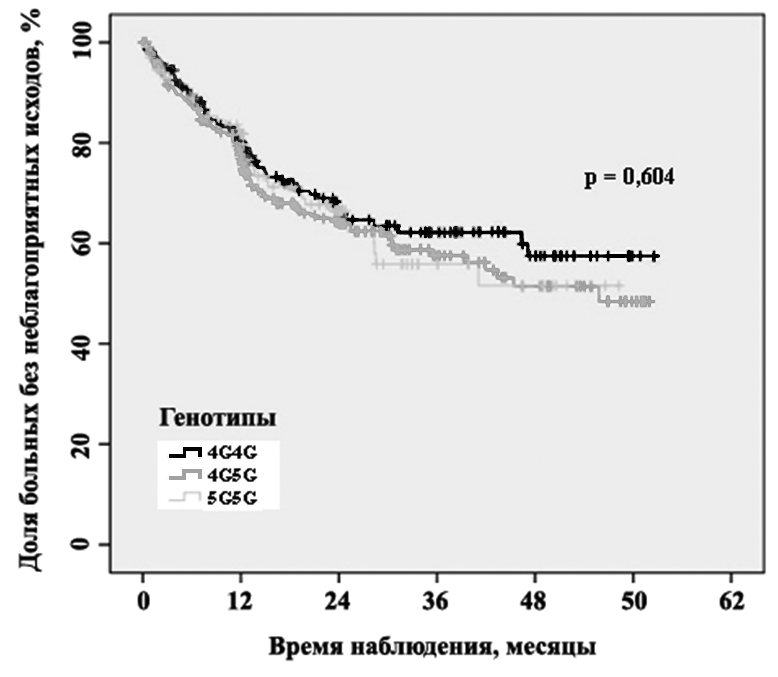
Рис. 6. График Каплана-Майера. Доля неблагоприятных исходов у носителей различных генотипов полиморфного маркера 4G(-675)5G гена PLANH1 в зависимости от времени, прошедшего после ОКС.
Работы, обнаружившие ассоциацию данного полиморфного маркера и риска развития ИМ, в основном проводились на небольших группах (Corsetti et al., 2008) и, возможно, полученные ими результаты связаны с недостаточной величиной выборки. Также, можно предположить, что аллель 4G является фактором риска развития ИМ только в молодом возрасте, в то время как средний возраст пациентов, исследуемых в нашей выборке, был старше 50 лет. Так, впервые ассоциация аллеля 4G гена PLANH1 с более высоким риском инфаркта миокарда была выявлена на шведской популяции у молодых мужчин (35 – 45 лет) (Ericsson et al., 1995), и в то же время, на больших группах пожилых пациентов ассоциация не наблюдалась. Об этом свидетельствует также достоверно более низкое число гомозиготных носителей аллеля 4G среди выживших пациентов, которые перенесли ИМ в возрасте до 35 лет (Rallidis et al., 2010). Кроме того, в нескольких более ранних работах не были обнаружены не только ассоциация данного полиморфного маркера с ИМ, но и его корреляция с уровнем PAI–1 (Doggen et al., 1999).
Таким образом, можно сделать вывод, что данный полиморфный маркер не ассоциирован с выживаемостью больных, перенесших ОКС.
ВЫВОДЫ.
- Определены частоты аллелей и генотипов полиморфных маркеров Arg506Gln и G5393A гена F5, Arg353Gln гена F7, С(–2676)Т гена PROC, Ala455Val гена THBD и 4G(–675)5G гена PLANH1 в группе больных, перенесших острый коронарный синдром.
- Для полиморфных маркеров Arg506Gln гена F5, Arg353Gln гена F7, С(–2676)Т гена PROC, Ala455Val гена THBD и 4G(–675)5G гена PLANH1 показано отсутствие ассоциации с развитием неблагоприятных исходов после эпизода ОКС.
- Обнаружена ассоциация полиморфного маркера G5393A гена F5 с повышенным риском развития неблагоприятного исхода (фатальный и нефатальный инфаркт миокарда, фатальный и нефатальный инсульт) в группе женщин, перенесших эпизод обострения ИБС.
- При изучении комбинации генотипов полиморфного маркера Arg353Gln гена F7 и Ala455Val гена THBD обнаружена их сочетанная ассоциация с повышенным риском развития неблагоприятного исхода (фатальный и нефатальный инфаркт миокарда, фатальный и нефатальный инсульт) в группе женщин, перенесших эпизод обострения ИБС.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Агапкина, Ю.В., Никитин, А.Г., Бровкин, А.Н., Пушков, А.А., Евдокимова, М.А., Кудряшова, О. Ю., Осмоловская, В.С., Минушкина, Л.О., Кочкина, М.С., Селезнева, Н.Д., Данковцева, Е.Н., Чумакова, О.С., Бакланова, Т.Н., Талызин, П.А., Резниченко, Н.Е., Донецкая, О.П., Терещенко, С.Н., Красильникова, Е.С., Джаиани, Н.А., Акатова, Е.В., Глезер, М.Г., Галявич, А.С., Закирова, В.Б., Казиолова, Н.А., Тимофеева, И.В., Ягода, А.В., Боева, О.И., Кательницкая, Л.И., Хоролец, Е.В., Шлык, С.В., Волкова, Э.Г., Маргарян, М.П., Гузь, И.О., Константинов, В.О., Тимофеева, И.В., Сидоренко, Б.А., Затейщиков, Д.А., Носиков, В.В. Полиморфные маркеры G(–455)A гена FGB и C(–1654)T гена PROC и генетическая предрасположенность к неблагоприятному течению ишемической болезни сердца у больных, перенесших острый коронарный синдром. Молекулярная биология.-2010.-Т. 44, № 4.-С. 613-619
- А.А. Пушков, К.А. Благодатских, А.Г. Никитин, Ю.В. Агапкина, А.Н. Бровкин, Д.А.Чудакова, М.А. Евдокимова, О.Ю. Асейчева, В.С. Осмоловская, Л.О. Минушкина, Т.Н. Бакланова, П.А. Талызин, О.П. Донецкая, С.Н. Терещенко, Н.А. Джаиани, Е.В. Акатова, М.Г. Глезер, А.С. Галявич, В.Б. Закирова, Н.А. Козиолова, А.В.Ягода, О.И. Боева, Е.В. Хоролец, С.В. Шлык, Э.Г. Волкова, М.П. Маргарян, И.О. Гузь, В.О. Константинов, Б.А. Сидоренко, Д.А. Затейщиков, В.В. Носиков. Полиморфные маркеры Ala455Val гена THBD и Arg353Gln гена F7 и осложнения атеросклероза у больных, перенесших острый коронарный синдром. Генетика.-2011, Т. 47, № 10, С. 101–107
- А.А. Пушков, О.В. Разуваева, К.А. Благодатских, А.М. Бурденный, А.Г. Никитин, А.Н. Бровкин, Д.А.Чудакова, М.А. Евдокимова, О.Ю. Асейчева, В.С. Осмоловская, Л.О. Минушкина, Т.Н. Бакланова, П.А. Талызин, О.П. Донецкая, С.Н. Терещенко, Н.А. Джаиани, Е.В. Акатова, М.Г. Глезер, А.С. Галявич, В.Б. Закирова, Н.А. Козиолова, А.В.Ягода, О.И. Боева, Е.В. Хоролец, С.В. Шлык, Э.Г. Волкова, М.П. Маргарян, И.О. Гузь, В.О. Константинов, Б.А. Сидоренко, Д.А. Затейщиков, В.В. Носиков. Полиморфный маркер 4G(-675)5G гена PLANH1 не ассоциирован с осложнениями атеросклероза у больных, перенесших обострение ишемической болезни сердца. Медицинская генетика.-2011.-№.11.-С.-16-21.
- A.A. Pushkov, K. A. Blagodatskikh, A. G. Nikitin, D. A. Zateyshchikov, V. V. Nosikov. Polimorphic markers of THBD and PROC genes and genetic predisposition to unfavourable outcomes in patients after acute coronary syndrome. 79 EAS Congress. Atherosclerosis Supplements.-2011.-Vol.12, №1.-P. 134-135, Gothenburg, Sweden (26-29 июня 2011 г.).
- А.А. Пушков, К. А. Благодатских, А. Г. Никитин, М. А. Евдокимова, В. С. Осмоловская, Д. А. Затейщиков, В. В. Носиков. Полиморфные маркеры Ala455Val гена THBD и C(-2676)T гена PROC и генетическая предрасположенность к неблагоприятному течению ишемической болезни сердца у больных, перенесших острый коронарный синдром. Материалы Х-ой ежегодной международной молодежной конференции ИБХФ РАН – ВУЗы «Биохимическая физика».-2011.-стр.203-204, г. Москва, Россия, (8-10 ноября 2010 г).
- А.А. Пушков, А.Г. Никитин, В.В. Носиков, Д.А. Затейщиков. Полиморфные маркеры Ala455Val гена THBD и Arg353Gln гена F7 и генетическая предрасположенность к неблагоприятному течению ишемической болезни сердца у больных, перенесших обострение ИБС. Материалы II международной научной конференции студентов, аспирантов и молодых ученых.-2011.-Стр. 232-233, г. Донецк, Украина, (19-22 сентября 2011 г).

