Разработка новых биотехнологических методов пол у чения инсулина и лечения инсулиноз а висимого сахарного диабета мелких домашних ж и вотных
На правах рукописи
АБДРАХМАНОВ ИГОРЬ КАМИЛЬЕВИЧ
РАЗРАБОТКА НОВЫХ БИОТЕХНОЛОГИЧЕСКИХ
МЕТОДОВ ПОЛУЧЕНИЯ ИНСУЛИНА И ЛЕЧЕНИЯ
ИНСУЛИНОЗАВИСИМОГО САХАРНОГО ДИАБЕТА
МЕЛКИХ ДОМАШНИХ ЖИВОТНЫХ
03.01.06 – биотехнология
(в том числе бионанотехнологии)
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора биологических наук
Ульяновск - 2011
Работа выполнена в ГНУ «Всероссийский научно-исследовательский институт экспериментальной ветеринарии им. Я.Р.Коваленко» РАСХН
| Научные консультанты: | Заслуженный деятель науки РСФСР доктор биологических наук, профессор ДЬЯКОНОВ ЛЕВ ПЕТРОВИЧ доктор биологических наук, профессор САВЧЕНКОВА ИРИНА ПЕТРОВНА |
| Официальные оппоненты: | доктор биологических наук, профессор ГЕНИНГ ТАТЬЯНА ПЕТРОВНА доктор биологических наук, профессор ГИЛЬМУТДИНОВ РУСТАМ ЯКУБОВИЧ доктор биологических наук, профессор БУКАРОВ НУРМАГОМЕД ГАДЖИКУЛИЕВИЧ |
| Ведущая организация | ФГБУ Федеральный центр токсикологической и радиационной безопасности «ФЦТРБ-ВНИВИ» |
Защита состоится «23» декабря 2011 г. в 1000 часов на заседании диссертационного совета Д 220.065.01 при ФГБОУ ВПО «Ульяновская государственная сельскохозяйственная академия» по адресу: 432063, г. Ульяновск, бульвар Новый Венец, 1, тел. 8 (8422) 44-30-58; факс 44-30-72, e-mail: [email protected]
С диссертацией можно ознакомиться в библиотеке
ФГБОУ ВПО «Ульяновская государственная сельскохозяйственная академия», а с авторефератом на сайте www.vak.ed.gov.ru
Автореферат разослан «______» _________________ 2011 года
Ученый секретарь
диссертационного совета Пыхтина Лидия Андреевна
- ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Инсулинозависимый сахарный диабет (ИЗСД) является тяжелейшим заболеванием вследствие повреждения островковой ткани поджелудочной железы (ПЖ) и сопровождается абсолютной инсулиновой недостаточностью. Сахарный диабет (СД) по распространённости занимает первое место среди эндокринологических заболеваний и третье место после сердечнососудистых и онкологических заболеваний.
Принимая во внимание угрожающие данные по статистике СД, остро встает вопрос о разработке принципиально новых подходов к его лечению, которое на сегодняшний день, как правило, является симптоматическим и не устраняет причины заболевания. Инсулинотерапия, по сути, не является лечением, это только способ отодвинуть на некоторое время наступление выраженных нарушений углеводного обмена, и, как следствие, осложнений СД. Введение больших доз инсулина не позволяет достичь желаемых результатов, т.е. полной компенсации углеводного обмена, и, тем самым, замедлить или остановить прогрессирование поздних сосудистых осложнений (Кузин М.И. с соавт., 1985; Литтман И., 1985). При этом лечение сопутствующих диабету ангиопатий эффективно только на фоне достигнутой стабилизации уровня глюкозы в крови (Дедов И.И. с соавт., 2004). Лечение СД в ветеринарии ограничивается только инсулинотерапией.
Применение экзогенного инсулина имеет ряд недостатков, связанных с постепенным развитием иммунного ответа на молекулу инсулина и потерю активности гормона. Препараты коммерческого инсулина, производимые фармкомпаниями созданы максимально приближенными к природному, однако методы генной инженерии не могут в полной мере смоделировать процессы биологического синтеза «зрелой» молекулы гормона, происходящие в -клетках ПЖ.
Другой метод лечения СД в гуманной медицине - трансплантация ПЖ или её части - связана с обязательной иммуносупрессией и обременена большим количеством этических проблем. Поэтому задача по поиску способа воздействия на причину заболевания и восстановления организмом утраченных функций остается актуальной и в медицине, и в клинической ветеринарии.
Успешное внедрение в практику экспериментальной биологии методов длительного культивирования стволовых клеток (СК) и клеток - предшественников различных тканей человека, работа с -клетками ПЖ, поиск адекватного клеточного материала, не вызывающего иммунного отторжения трансплантатов, создали предпосылки для разработки технологий заместительной клеточной и тканевой терапии. Один из таких методов - трансплантация в организм больного ИЗСД островковых клеток (ОК) ПЖ - представляется перспективным способом достижения гликемического контроля, поступления в организм эндогенного инсулина, предотвращения тяжёлых гипогликемий и сопутствующих осложнений (Скалецкий Н.Н. с соавт., 1994, Federlin K. et al., 1999).
Трансплантация -клеток ПЖ как потенциальный метод лечения диабета была внедрена в медицинскую практику более 10 лет назад, в ветеринарии этот метод не был отработан ни экспериментально, ни клинически. Однако применение этого метода будет всегда ограничиваться трудностями получения достаточного количества островков от доноров. Решением проблем тканевой трансплантации, а, следственно, лечения ИЗСД людей и животных, является разработка методов получения возобновляемых ресурсов клеток путём использования клеточных технологий.
Цель работы – разработать новые биотехнологические методы, направленные на получение инсулина in vitro, а также на лечение инсулинозависимого сахарного диабета мелких домашних животных.
Для достижения цели были поставлены следующие задачи:
- Выделить из ПЖ плодов кролика, собаки, кошки -клетки, очистить; изучить их свойства и признаки in vitro.
- Провести гибридизацию -клеток ПЖ плодов кролика с мутантной линией почки овцы, дефектной по тимидинкиназе (ПО ТК-).
- Провести сравнительный анализ клонов межвидовых гибридных культур ПО ТК- х -клетки и отобрать клоны с высокой продукцией инсулина.
- Адаптировать клоны с наиболее высокой продукцией инсулина к роллерно-суспензионному культивированию и получить суспензионные клоны гибридной культуры.
- Изучить гистологическую совместимость межвидовых гибридных культур in vitro с сыворотками крови человека.
- Разработать методы получения и культивирования примордиальных половых зародышевых клеток (ППЗК) свиньи.
- Получить in vitro инсулин-секретирующие клетки, подобные -клеткам ПЖ, путем направленной дифференцировки эмбриональных половых клеток (ЭПК) свиньи.
- Осуществить трансплантацию -клеток ПЖ плодов кролика лабораторным животным с экспериментальным СД и изучить влияние данной процедуры на течение заболевания.
- Разработать метод трансплантации -клеток ПЖ плодов кролика мелким домашним животным с диагнозом СД и изучить влияние трансплантации клеток на течение заболевания.
Научная новизна. Впервые из ПЖ собак и кошек получены культуры -клеток, изучены их свойства и признаки in vitro. Оптимизированы методики выделения -клеток ПЖ плодов кроликов, разработаны методики выделения фетальных -клеток кошек и собак.
Впервые посредством слияния получена гибридная культура почка овцы х -клетки кролика (ПО ТК- х кр), способная продуцировать инсулин in vitro.
Впервые получены и прокультивированы ППЗК свиней. Проведена направленная индукция ЭПК свиньи в инсулин-секретирующие клетки.
В опытах на лабораторных животных установлено, что ксенотрансплантация -клеток ПЖ плодов кроликов нормализует течение экспериментального СД.
Впервые проведена клиническая трансплантация -клеток ПЖ плодов кроликов мелким домашним животным, больным СД. При этом доказано, что в результате трансплантации происходит снижение уровня глюкозы в крови и моче, снижение дозы либо отказ от экзогенного инсулина, уменьшение возникновения сопутствующих диабету сосудистых осложнений.
Научно-практическая значимость работы. Разработан и запатентован способ выделения -клеток кроликов, собак и кошек из плодной ПЖ на определенных сроках гестации и очистки их культивированием, а также способ лечения СД у собак и кошек, заключающийся в трансплантации -клеток непосредственно через брюшную стенку в паренхиму левой доли печени, без применения иммуносупрессивной терапии (патент на изобретение РФ №2325921). Указанный способ успешно используется в ряде ветеринарных клиник.
Разработаны и утверждены «Методические рекомендации о порядке аттестации и поддержания перевиваемых линий клеток, используемых для культивирования вирусов и производства иммунобиологических препаратов ветеринарного назначения».
Разработаны и утверждены «Методические рекомендации по лечению инсулинозависимого сахарного диабета (СД 1) собак и кошек методом внутрипеченочной трансплантации -клеток плодов кроликов».
Полученные результаты расширяют представление о методах клеточной инженерии, направленных на получение клеточных культур, стабильно продуцирующих инсулин.
Полученные результаты открывают перспективы, позволяющие разрабатывать способы получения клеточного материала, используемого в терапии СД.
Результаты исследования могут найти применение в теоретической и экспериментальной клеточной биологии, биотехнологии, физиологии, фармакологии и клинической ветеринарии.
Личный вклад соискателя. Работа выполнена соискателем самостоятельно, участие соавторов отражено в совместно изданных научных статьях. В выполнении отдельных этапов работы принимали участие: к.б.н. Т.А. Приданцева, к.б.н. Т.В. Гальнбек, д.б.н. Н.А. Зиновьева, д.б.н. Н.Н. Скалецкий, к.б.н. М.А.Селюгин, к.с-х.н. Ю.А.Кузнецов, к.б.н. А.С.Симонова, к.б.н. Н.Б. Савенко, Л.А. Сережина, к.б.н. Т.А. Сидорова, н.с. Н.А. Шевцова за что автор приносит им свою благодарность.
Основные положения, вынесенные на защиту:
- Инсулино-продуцирующие и культурально - морфологические свойства культур -клеток из ПЖ плодов кроликов, собак, кошек не однозначны. Наиболее перспективным материалом для клеточной инженерии являются кроличьи -клетки.
- Гибридизация -клеток с постоянной линией клеток почки овцы(ПО ТК-) и последующее клонирование позволяют получить культуру клеток – продуцентов инсулина in vitro.
- Продукция инсулина в гибридных клонах зависит от длительности и метода культивирования.
- Культивирование ЭПК свиньи в индукционной среде приводит к формированию колоний инсулин–продуцирующих клеток, подобных -клеткам ПЖ.
- Предложенный метод терапии СД мелких домашних животных путем трансплантации очищенных -клеток ПЖ плодов кролика позволяет улучшить течение заболевания и сопутствующих ему осложнений.
Апробация работы. Материалы диссертационной работы доложены и обсуждены на: VIIth International Congress of Andrology «Andrology in the 21st Century» (Montreal, Canada, 2001); международном симпозиуме «Научные основы обеспечения защиты животных от экотоксикантов, радионуклидов и возбудителей опасных инфекционных заболеваний» (Казань, 2005); международной научно-практической конференции «Современное состояние и перспективы исследовании по инфекционной и протозойной патологии животных, рыб и пчел» (Москва, 2008); Всероссийской научной конференции «Современные проблемы науки и образования» Российской академии естествознания (Москва, 2008).
Публикации. По материалам диссертации опубликовано 23 печатных работы, в том числе 10 в журналах, рекомендованных ВАК РФ и 1 патент.
Структура и объем работы. Работа изложена на 300 страницах стандартного компьютерного текста и включает: введение, обзор литературы, собственные исследования с обсуждением полученных результатов, выводы, практические предложения, библиографический список использованной литературы и приложение. Материалы диссертации иллюстрированы 36 таблицами, 118 рисунками. Библиографический список литературы включает 341 источник, из которых 240 - иностранных.
- МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЙ
Работа выполнена с 2005 по 2011 гг. в отделе клеточной биотехнологии ГНУ Всероссийский научно-исследовательский институт экспериментальной ветеринарии им. Я.Р. Коваленко, согласно заданию 02.01.20. РНТП «Осуществить поддержание и развитие уникальных коллекций клеточных культур животных, вакцинных и эпизоотических штаммов вирусов, бактерий, грибов, простейших. Создать новые культуры клеток – суперпродуценты для биотехнологии методами клеточной инженерии».
Общая схема исследований представлена на Рис.1.
В качестве материала ОК использовали ПЖ плодов на сроках гестации - 26±2 сут., 38-56 сут., 42-50 сут. для кроликов, собак и кошек соответственно. Выделение ОК проводили с использованием коллагеназы (Sigma) и трипсина (ПанЭко). Культивирование проводили в СО2 инкубаторе при температуре 370С, 5% СО2. Средой для культивирования была среда 199 с добавлением 10% сыворотки плода коровы (СПК) (Hyclone).
Для гибридизации клеток в качестве партнера по слиянию использовали мутантную перевиваемую линию клеток почки овцы ПО ТК-. Эксперименты по гибридизации проводили согласно «Методическим рекомендациям по гибридизации соматических клеток сельскохозяйственных животных» (Дьяконов Л.П. с соавт., 1988).
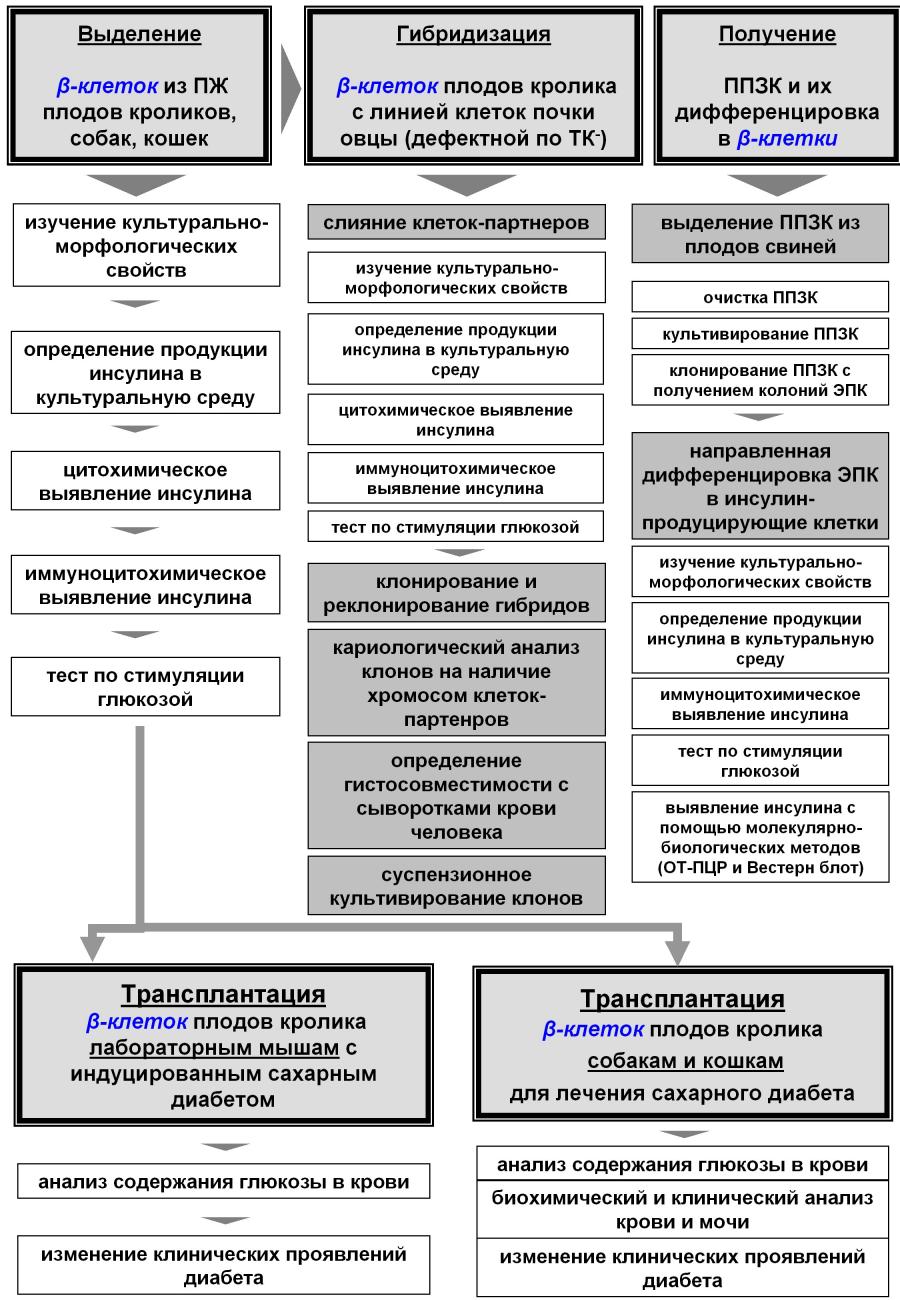
Рис. 1. Общая схема исследований.
Суспензионное культивирование гибридных клеток осуществляли на роллерной установке (Wheaton) во флаконах, обработанных силиконом.
Гистосовместимость гибридных клеток оценивали по методу микровариант комплемент - зависимой цитотоксической реакции (Абрамов В.Ю., 2005).
Наличие инсулина в экспериментальных клетках определяли с помощью цитохимического окрашивания альдегидфуксином.
Для иммуноцитохимического окрашивания экспериментальных клеток на инсулин использовали мышиные моноклональные антитела против инсулина (Sigma), специфичные для выявления инсулина кролика, собаки, кошки, свиньи. В качестве вторичных антител использовали антимышинные антитела, меченные FITC (Sigma), а также антимышинные антитела, меченные пероксидазой хрена (Медгамал).
Уровень продукции инсулина в культуральной жидкости определяли методом радиоиммунного анализа (Ronald R., 1992) в лаборатории радиоизотопного анализа НИИТиИО с помощью наборов «Insulin RIA DSL 1 600, USA».
Эксперименты по цитотоксическому действию сыворотки человека на гибридные клетки проводили в присутствии комплемента человека или кролика. Использовалась взвесь гибридных клеток ПО ТК- х кр. в концентрации 600 тыс. кл/мл. Инкубация клеток с сывороткой человека составила 30 мин, а с комплементом человека или кролика (5 мкл) - 60 мин. Каждый эксперимент выполняли дважды.
Для проведения Вестерн-блотинга белки разделяли с помощью вертикального электрофореза в полиакриламидном геле с додецилсульфатом натрия (SDS) с последующим переносом их на нитроцеллюлозную мембрану и детекцией методом иммуноблотинга. Использовали первичные мышиные моноклональные антитела против инсулина (Sigma) и вторичные антимышинные антитела, меченные пероксидазой хрена (Amersham). В дальнейшем мембраны обрабатывали ELC-реагентом с регистрацией люминесценции на фотопленку Kodak Biomax Light Film (Sigma).
Уровень экспрессии мРНК инсулина в экспериментальных клетках определяли методом ПЦР с обратной транскрипцией (ОТ ПЦР) в соответствии со стандартным протоколом. ПЦР проводилась в амплификаторе «Терцик». Продукты амплификации анализировали используя гель-электрофорез в 1,5 %-ом агарозном геле. Окраску гелей производили при помощи бромистого этидия в стандартной концентрации.
ППЗК из плодов свиней выделяли на 23, 26, 31 и 33-и сут. супоросности от естественно осемененных помесных свиноматок (крупная белая х ландрас). Культивирование ППЗК осуществляли на фидерных слоях, представленных перевиваемыми фибробластами мыши линии STO.
Фидерные STO-клетки, используемые при выделении и культивировании ППЗК, выращивали в среде DMEM, дополненной 10 %-ми СПК, 2mМ альфа-глутамина (ПанЭко) и 50 мкг/мл гентамицина (ПанЭко). Для подавления митоза клеток фидерных слоев при достижении ими монослоя использовали среду DMEM, дополненную 10 % СПК и 10 мкг/мл митомицина С (Sigma). Фидерные слои готовили по методике, описанной Савченковой И.П. (1999).
ППЗК свиней культивировали в СО2 инкубаторе при температуре 370С в контакте с газовой средой, содержащей 5 % СО2. Средой служила ДМЕМ, содержащая 15 % СПК, 2mM альфа-глутамина, 10-6 mM 2-меркаптоэтанола (Serva), 50 мкг/мл гентамицина на предварительно приготовленном фидерном слое STO-клеток.
СД у лабораторных мышей BALB/c индуцировали внутривенным введением стрептозотоцина (STZ) (Sigma) в дозе 150 мг/кг массы.
Внутрипеченочную трансплантацию клеток лабораторным мышам осуществляли интрапаренхиматозно под общей анестезией в дозе 100 тыс. кл./0,5 мл раствора на мышь.
Лабораторным собакам -клетки вводили подкожно в область холки двукратно с интервалом 19 сут. в дозе 100 тыс. клеток на 1 кг массы тела.
Собакам и котам с диагнозом СД клетки трансплантировали в паренхиму печени под эхографическим контролем в количестве 100 тыс. клеток на 1 кг массы тела непосредственно через брюшную стенку в паренхиму левой доли печени, без применения иммуносупрессивной терапии.
Уровень глюкозы в крови определяли глюкометром Accu-Chek Active (Roshe).
Оценку клинических и биохимических показателей крови и мочи после трансплантации проводили в ветеринарных лабораториях г.Москвы хозяева больных животных.
Все полученные данные подвергали биометрической обработке с определением достоверности различий между соответствующими показателями контрольных, опытных и интактных групп, с использованием общепринятых методов вариационной статистики (Лакин Г.Ф., 1990) и прикладных программ «Statistica 5.5», «Excel».
- СОБСТВЕННЫЕ ИССЛЕДОВАНИЯ
- Выделение из поджелудочных желез плодов кролика, собаки, кошки -клеток. Изучение их свойств и признаков
Работы по выделению -клеток из ПЖ животных и человека ведутся с шестидесятых годов прошлого столетия. Несмотря на то, что методы выделения ОК в большинстве случаев являются рутинными, основное направление исследований сфокусировано на получении максимально очищенного материала с высоким процентом жизнеспособных клеток.
Наиболее удобной моделью (синхронность, доступность, стоимость и пр.) для отработки методов выделения плодных -клеток, безусловно, являются ПЖ плодов кроликов. При этом в качестве диспергирующего раствора при выделении наиболее часто используется коллагеназа (Feldman J. et al., 1975) и трипсин (Misler S. et al., 1986).
В нашей стране Шумаков В.И. с соавт. (1995) для выделения -клеток из ПЖ плодов кроликов разработали модифицированный метод, использовав смесь равных долей коллагеназы и трипсина.
Получение -клеток собак и кошек представляет собой более трудоемкий процесс. Краткосрочное (24 ч) культивирование фрагментов ПЖ собак впервые описано Matas A. et al. в 1976 году. Позже Scharp D. et al. (1980) предложили два метода выделения ОК из ПЖ собак для очистки материала от протоковой, ацинарной и фиброзной тканей. В одном случае использовали коллагеназу в различных композициях, в другом – трипсин с последующим выделением клеток в градиенте Фиколла. Данный протокол был предложен как основа в отработке методов выделения -клеток из взрослой ПЖ человека для ауто- и аллотрансплантаций. В последующем работы исследователей по получению ОК из ПЖ собак были направлены на совершенствование методов выделения максимального количества островков, а также на более качественную очистку материала от сопутствующих клеток.
Более сложными в получении культуры, пригодной для трансплантации, оказались -клетки из ПЖ кошек. Maeno T. et al. (2006) описали метод выделения островково-подобных клеток из ПЖ кошек с использованием коллагеназы и последующим культивированием в течение 9 сут в бессывороточной среде. Трансплантация под капсулу почки 4-м кошкам с удаленной ПЖ очищенных таким образом клеток, позволила добиться нормогликемии на протяжении 12 сут. Zini E. et al. (2009) описали опыт получения кошачьих ОК 6-тью методами выделения с применением коллагеназы (варианты однократной и двойной обработки коллагеназой, последующее центрифугирование в градиенте Фиколла в присутствии коллагеназы или аккутазы). И хотя при использовании всех вариантов выход чистых ОК оказался одинаковым, он был чрезвычайно низок – не более 2 %.
Учитывая изложенное, представляло интерес выделить, охарактеризовать и сравнить в качестве материала для трансплантации -клетки из ПЖ плодов кролика, собаки и кошки.
Для ферментативной обработки ткани ПЖ плодов кролика мы использовали трипсин или коллагеназу. В обоих случаях на 4-е сут. культивирования отмечали клеточные колонии с характерной для ОК ПЖ морфологией. К 7 сут. культивирования колонии -клеток укрупнялись, формируя плотные многослойные конгломераты. По их краям наблюдали уплотненную зону роста фибробластов (Рис.2). Начиная с 10-12 дневного срока культивирования в культурах наблюдали инволютивные изменения, что коррелирует с данными Шумакова В.И. с соавт. (1995). Кондиционированная среда клеток плодов кроликов содержала инсулин в концентрации 38-80 мкИЕ/мл.
При окрашивании альдегид-фуксином отмечали специфическую пурпурную зернистость цитоплазмы в значительной части клеточных колоний клеток эпителиоподобной морфологии. Фибробласты при этом не прокрашивались (Рис.3). Интенсивность окрашивания существенно не менялась на протяжении всего срока культивирования клеток. Доля клеток со специфической зернистостью в колониях эпителиоподобных клеток превышала 90%.
При иммуноцитохимическом окрашивании культуры клеток, выделенной из ПЖ кролика, на инсулин с использованием флуоресцирующего красителя (FITC), выявляли специфическое желто-зеленое «свечение» прикрепившихся к стеклу колоний ОК (Рис.4); а при использовании АТ, меченных пероксидазой хрена – специфическое окрашивание секреторных клеток (Рис.5).
Таким образом, по цитологическим признакам, наличию специфической альдегид-фуксин позитивной зернистости, окрашиванию мечеными АТ против инсулина, а также феномену дегрануляции, наступающему в ответ на повышение содержания глюкозы в культуральной среде можно было заключить, что выделенные нами клетки являются -клетками островков Лангерганса ПЖ плодов кроликов.
Для выделения -клеток из ПЖ плодов собаки и кошки мы использовали методику с использованием раствора трипсин/версена. Характерной особенностью -клеток из ПЖ плодов собаки была способность при культивировании образовывать крупные колонии, от которых спонтанно отрывались клетки и плавали в суспензии, а затем снова прикреплялись, давая начало новым колониям (Рис.6). Уровень продукции инсулина во флаконах с секреторными клетками в среднем составлял 84 мкИЕ/мл. При окрашивании секреторных клеток на инсулин наблюдали специфическую пурпурную зернистость цитоплазмы (окраска ПАФ) или специфическое жёлто-зелёное свечение (ИЦХ с FITC).
Было установлено, что клетки плодов собаки по сравнению с кроличьими и кошачьими характеризовались самой низкой адгезией. В таких культурах было наибольшее количество плавающих клеток: одиночных и группами. Клетки, идентифицированные нами как -клетки, представляли собой округлые секреторные клетки с зернистой вакуолизированной цитоплазмой. Основной особенностью их было формирование крупных многослойных плавающих колоний. Пик митотической активности наблюдали на 4-5 сут. после выделения клеток, однако к 7-10 сут. культивирования клетки замедляли рост и появлялись признаки клеточной дегенерации. К 14 сут. в культуре не оставалось ни одной живой секреторной клетки.
В отличие от собак, -клетки из ПЖ плодов кошек на 3-4 сут. культивирования проявляли активный рост с преобладанием делящихся фибробластов (Рис.7). В монослое отмечали единичные эпителиоподобные клетки. После пересева с использованием трипсина клеточные культуры включали в себя только фибробласты. Без пересева клеток дегенерация монослоя происходила полностью к 10 сут. Такой характер роста клеток позволил нам заключить, что -клетки плодов кошки подвергаются вытеснению их фибробластами во время культивирования. Одной из причин этого являются, возможно, высокие адгезивные способности клеток данного вида, которые не позволяют их очистить.
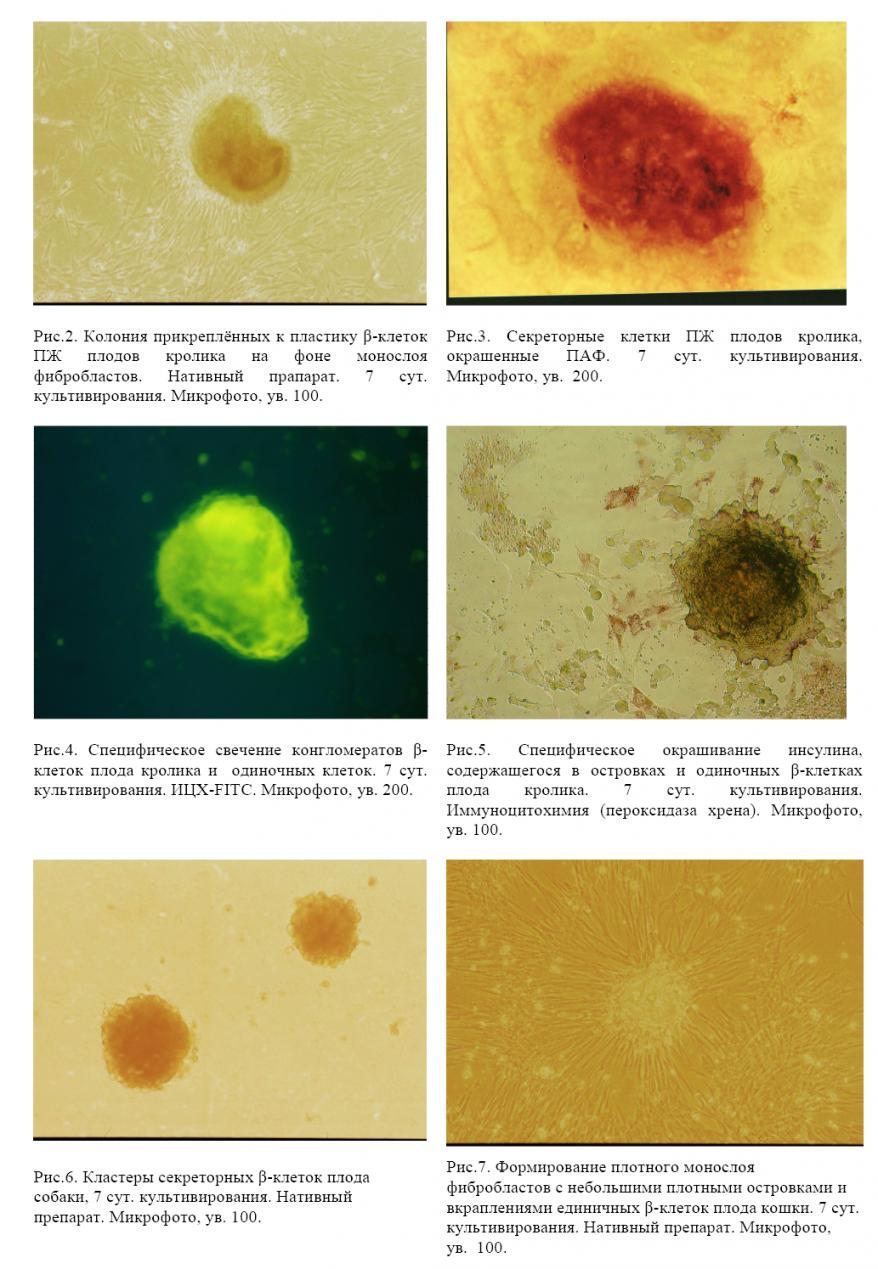
С другой стороны, можно предположить, что они подвергаются ранней дегенерации, что делает эти клетки непригодными для дальнейшего культивирования и трансплантации.
Уровень секреции инсулина на 3 сут. культивирования составлял 77 мкИЕ/мл.
Таким образом, опираясь на данные, полученные в экспериментах по выделению -клеток ПЖ плодов кроликов, собак и кошек можно заключить, что культуры клеток, полученные из ПЖ кошек заметно отличались от культур собак и кроликов высокой адгезивной способностью.
Во всех опытах мы воспроизводили низкий уровень выхода секреторных клеток. Сроки жизни кошачьих культур были заметно короче: 16-18 сут. – срок жизни -клеток плода кролика, 14 сут. – собаки, 10 сут. - кошки. Кластеров секреторных клеток в культурах -клеток ПЖ плодов кошек образовывалось гораздо меньше, адгезивная способность их была выше.
По проценту выхода секреторных клеток, сроку их жизни и степени чистоты клеточного материала для своих дальнейших исследований мы посчитали наиболее приемлемым материалом ПЖ плодов кролика. У клеток собак и кошек значительно меньше выход секреторных клеток и ниже их жизнеспособность. Кроме того, имеются определенные трудности в получении необходимого количества материала на определенных сроках гестации.
Доказательством того, что полученные и использованные нами в последующих исследованиях клетки являются именно -клетками, служат культурально-морфологические свойства, цитохимическое и иммуноцитохимическое окрашивание клеток на инсулин, а также радиоиммунный анализ продукции клетками инсулина в культуре.
- Межвидовая гибридная культура почки овцы ПО ТК- с - клетками поджелудочной железы плодов кроликов. Получение, клонирование и изучение её свойств и признаков
В задачу наших исследований входило получить культуру, способную длительно перевиваться, не обладать туморогенностью и в то же время продуцировать инсулин. Для этого необходимо было получить гибрид -клеток, не пролиферирующих in vitro, с клетками из немалигнизированных тканей.
Учитывая недостаток литературных данных по гибридизации -клеток, использовали методики, разработанные ранее в отделе клеточной биотехнологии ГНУ ВНИИ экспериментальной ветеринарии им. Я.Р.Коваленко, по получению гибридных линий на основе мутантной культуры ПО ТК-. Проведено несколько серий экспериментов по гибридизации с целью подбора оптимальных условий гибридизации, при которых расход клеток будет минимальным, а индекс слияния наибольшим:
- ПЭГ 4000 и экспозицию 1 ч в соотношении сливаемых клеток 1:10;
- ПЭГ 4000 и экспозицию 12 ч в соотношении клеток 1:10;
- ПЭГ 1000 с экспозицией 1 ч и клетки в соотношении 1:1.
Получено по 6 гибридных популяций клеток из каждой серии экспериментов (Таблица 1). Клетки гибридов первого поколения стимулировали глюкозой, чтобы по выбросу инсулина из клеток оценить их потенциал.
Таблица 1 - Продукция инсулина (мкИЕ/мл) на ранних пассажах гибридами, полученными при разных условиях гибридизации.
| Группа экспери-ментов | Название полученного гибрида | Пассаж | Стимуляция глюкозой | ||||
| 0* | 6 | 1 час | 12 часов | 24 часа | |||
| 1. | А | 13,3 | 15,8 | 15,9 | 14,3 | 12,1 | |
| Б | 14,3 | 15,5 | - | - | - | ||
| В | 12,7 | 14,7 | - | - | - | ||
| Г | 20,1 | 30,2 | 37,2 | 35,5 | 32,0 | ||
| Д | 18,0 | 28,8 | 29,6 | 24,9 | 18,8 | ||
| Е | 12,9 | 13,1 | - | - | - | ||
| 2. | 3.1.1.А | 8,0 | 12,2 | - | - | - | |
| 3.1.1.Б | 10,5 | 9,6 | - | - | - | ||
| 3.1.1.В | 6,3 | 13,1 | 13,9 | 12,4 | 10,2 | ||
| 3.1.1.Г | 14,1 | 12,7 | - | - | - | ||
| 3.1.1.Д | 7,5 | 13,3 | 13,8 | 12,9 | 11,8 | ||
| 3.1.1.Е | 7,8 | 12,5 | - | - | - | ||
| 3. | 3.1.2.А | 13,2 | 18,1 | 20,7 | 19,4 | 19,0 | |
| 3.1.2.Б | 12,1 | 22,8 | 24,2 | 21,5 | 18,1 | ||
| 3.1.2.В | 11,9 | 10,3 | - | - | - | ||
| 3.1.2.Г | 14,6 | 14,0 | - | - | - | ||
| 3.1.2.Д | 14,5 | 13,2 | - | - | - | ||
| 3.1.2.Е | 17,2 | 13,6 | - | - | - | ||
| Культуральная среда + сыворотка | 1,7 - 12,3 | ||||||
| Норма в сыворотке крови | 4-16 | ||||||
| Отрицательный контроль | 15,99 | ||||||
Примечание:
Пробы культуральной жидкости для анализа отбирали на 6 сут. культивирования
* - уровень продукции инсулина определяли в среде ГАТ на 8 сут. культивирования
Использование ПЭГ 4000 с экспозицией 1 час и 10-кратного количества секреторных клеток (1 млн. -клеток : 100 тыс. клеток ПО ТК-) (1 группа экспериментов) позволило получить гибриды с более высоким уровнем продукции инсулина (Таблица 1), по отношению к другим экспериментальным группам, в частности на 30% выше, чем в 3 группе. Использование ПЭГ 1000 и соотношением клеток 1:1 является оптимальным (100 тыс. -клеток : 100 тыс. клеток ПО ТК-) (3 группа экспериментов), т.к. позволяет расходовать -клетки в экономичном режиме и полученные гибриды обладают достаточно высоким уровнем продукции инсулина и имеют в популяции большое число клеток с морфологией, подобной -клеткам ПЖ. Причем, наблюдали зависимость между морфологией клеток, характером роста культуры и секреторной способностью клеток. В гибридах наблюдали различное соотношение округлых секреторных клеток (с морфологией -клеток, выделенных из ПЖ плодов кроликов) и эпителиоподобных клеток, обладающих высокими адгезивными свойствами. В клонах с высокой секреторной способностью наблюдали больший процент округлых клеток.
Было установлено, что уровень продукции инсулина на 6 сут культивирования на 6 пассаже в таких гибридах (с высокими продуктивными свойствами) составляет от 15,8 мкИЕ/мл до 30,2 мкИЕ/мл, что находится на верхней границе или почти в 2 раза превышает содержание инсулина в ростовой среде. Для дальнейшего клонирования мы отобрали именно эти клоны.
Гибриды клонировали на 7 пассаже методом предельных разведений. Всего при последующем отборе и реклонировании был получен 201 клон клеточной гибридной культуры.
В результате проводимого отбора методами цитохимии, иммуноцитохимии, радиоиммунного анализа на инсулин, стимуляции глюкозой оказались наиболее продуктивными клоны ГА-2, 3.2.17, 3.2.42 межвидовой гибридной культуры клеток ПО ТК- х кр. На уровне 24 пассажа имели соответствующие культурально-морфологические характеристики и высокий уровень продукции инсулина в культуральной среде. Кариологический анализ показал, что гибриды несут в своем составе хромосомы обоих партнеров по слиянию (овцы и кролика).
Однако после 32-го пассажа мы отмечали стабильное снижение уровня продукции гормона от пассажа к пассажу. Так, клетки клона ГА-2 снизили свою продукцию на 13 % от первоначальной, а клетки клонов 3.2.17 и 3.2.42 - на 28 % и 50 %, соответственно (Таблица 2).
Таблица 2 - Продукция инсулина (мкИЕ/мл) гибридными клонами при монослойном культивировании.
| Гибридный клон | № пассажа | |||
| 10 | 24 | 32 | 40 | |
| ГА-2 | 29,7 | 28,7 | 25,9 | 22,7 |
| 3.2.17. | 30,1 | 25,2 | 22,2 | 14,6 |
| 3.2.42. | 26,2 | 20,0 | 13,2 | 6,3 |
Для повышения уровня секреции инсулина была проведена серия экспериментов по получению суспензионных штаммов гибридной культуры ПО ТК- х кр. Для этого использовали клоны:
- 3.2.17 на 32 пассаже (на момент начала эксперимента продукция инсулина составила 22,2 мкИЕ/мл);
- 3.2.42 на 24 пассаже (продукция инсулина 20,0 мкИЕ/мл);
- ГА-2 на 54 пассаже (24,3 мкИЕ/мл).
В результате проведенных экспериментов было установлено, что на первых 2-3 пассажах культивирования в суспензии наблюдается увеличение продукции инсулина. Но с увеличением числа пассажей продуктивность клеток всех трех клонов заметно снизилась и к 11 пассажу наступила дегенерация клеток всех клонов (Таблица 3).
Таблица 3 - Продукция инсулина (мкИЕ/мл) гибридными клонами при суспензионном культивировании.
| Гибридный клон | № пассажа | ||||
| до опыта | 2 | 4 | 7 | 11 | |
| 3.2.17. | 22,2 | 28,7 | 16,4 | дегенерация | дегенерация |
| 3.2.42. | 20 | 26,1 | 17 | дегенерация | дегенерация |
| ГА-2 | 24,3 | 29,9 | 26 | 11,2 | дегенерация |
Примечание: нумерация пассажей ведется от начала опыта по суспензионному культивированию
Таким образом, установлена нестабильность признака секреции инсулина, присущего -клеткам ПЖ плодов кролика. Более того, при переводе гибридных клонов с максимальной продукцией инсулина в режим роллерно-суспезионного культивирования происходят изменения, которые вероятно ведут к утрате способности ими секретировать инсулин. Клеточные гибриды, полученные в результате слияния -клеток ПЖ плодов кролика и клеток почки овцы ПО ТК-, способны продуцировать инсулин в культуральную среду, однако продукция эта нестабильна и зависит от длительности культивирования.
- Определение гистологической совместимости гибридной культуры in vitro
Считается, что при пересадке островковых -клеток необходимо исключить контакт эндотелия донора с кровью реципиента, чтобы снизить вероятность гиперострого отторжения по типу гиперкоагуляции за счет продуцируемых тромбоцитами цитокинов (Badet L. et al., 2002).
Olphen A. et al. (2002) показали возможность нахождения на поверхности клеток-клонов гибридной линии человек х КРС (МДВК х 293-Puro) поверхностных антигенов любого из родителей, что доказывает неравномерное распределение хромосом родительских линий в дочерних клетках при последующих делениях. Этот факт позволил предположить отсутствие на поверхности гибрида ПО ТК- х кр. видовых антигенов вообще, что делает целесообразным проведение исследований на его гистосовместимость с другими видами животных. Представляло интерес определить степень вероятности отторжения гибридной культуры при трансплантации человеку.
Мы провели ряд тестов на гистосовместимость гибридной культуры ПО ТК- х кр. с сыворотками человека для определения возможности трансплантации инсулин-продуцирующих клонов больным СД (Таблица 4). Оценку реакции выражали в условных единицах цитотоксического теста (от 0 до 4).
Таблица 4 - Цитотоксическое действие сыворотки человека на гибридные клетки ПО ТК- х кр.
| Цитотоксический агент | № лунки | С комплементом | |
| человека | кролика | ||
| Ig лошади против лейкоцитов человека | 1 | 0 | 4 |
| Пул сывороток человека, без HLA-антител, инактивированных нагреванием 56оС 30 мин. | 2 | 0 | 4 |
| 3 | 0 | 4 | |
| 4 | 0 | 4 | |
| Сыворотка человека, АВ (IV) (потенциальные реципиенты почки, n=13) | 5 | 1 | 4 |
| 6 | 1 | 4 | |
| 7 | 4 | 4 | |
| 8 | 1 | 4 | |
| 9 | 0 | 4 | |
| 10 | 0 | 4 | |
| 11 | 0 | 4 | |
| 12 | 4 | 4 | |
| 13 | 2 | 4 | |
| 14 | 0 | 4 | |
| 15 | 3 | 4 | |
| 16 | 3 | 4 | |
| 17 | 4 | 4 | |
| Сыворотка человека (больные кардиологического отделения, мужчины, n=10) | 18 | 4 | 4 |
| 19 | 2 | 4 | |
| 20 | 0 | 4 | |
| 21 | 0 | 4 | |
| 22 | 0 | 4 | |
| 23 | 4 | 4 | |
| 24 | 4 | 4 | |
| 25 | 1 | 4 | |
| 26 | 0 | 4 | |
| 27 | 0 | 4 | |
Комплемент кролика лизировал клетки ПО ТК- х кр. во всех комбинациях, в том числе и в отсутствие сыворотки человека, что доказывает наличие видовых (кроличьих) АГ на поверхности гибридных клеток. Такой результат является положительным контролем наличия кроличьих хромосом в составе гибридной культуры.
Комплемент человека не лизировал клетки ПО ТК- х кр. в 13 случаях из 23 (лунки 5, 6, 8-10, 11, 14, 20-22, 25-27), что составляет более 50 %. Этот эффект наблюдали в присутствии иммуноглобулинов лошади, инактивированной сыворотки человека и самостоятельно (Таблица 4,Таблица 5).
Таблица 5 - Цитотоксическое действие комплемента на гибридные клетки ПО ТК- х кр.
| Цитотоксический агент | № лунки | С комплементом | |
| человека | кролика | ||
| 1. Инкубация клеток в среде 199 – 30 минут. 2. Инкубация с комплементом человека или кролика 60 минут. | 1 | 1 | 4 |
| 2 | 1 | 4 | |
| 3 | 1 | 4 | |
| 4 | 0 | 4 | |
| 5 | 0 | 4 | |
| 6 | 0 | 4 | |
Из результатов видно, что межвидовая гибридная культура ПО ТК- х кр. обладает определенной гистосовместимостью с АТ человека.
Известно, что комплекс гистосовместимости человека представляет собой несколько пар аллельных генов, которые у животных могут отличаться по числу генов, входящих в этот комплекс или вообще их наличию.
Из-за того, что невозможно было определить в наших экспериментах, какие АТ связываются с гибридными клетками, можно предположить, что отсутствие АТ в сыворотках крови человека к клеткам гибридной культуры ПО ТК- х кр. еще не свидетельствует о гистосовместимости этих двух видов. Возможно появление антител (АТ) при втором или третьем введении антигенных структур этих клеток. Нельзя исключить возможность сенсибилизации организма реципиента при однократном введении трансплантата, однако повторное введение материала может привести к анафилактической реакции, а также к отторжению трансплантата. В связи с этим, мы пришли к выводу, что вопрос о гистосовместимости гибридной культуры ПО ТК- х кр. с человеком остается спорным и требует дальнейшего детального изучения.
- Разработка модели получения инсулин-продуцирующих клеток in vitro с использованием стволовых клеток
- Выделение примордиальных половых зародышевых клеток (ППЗК) из плодов свиней и их очистка
Выделение ППЗК из зачатков гонад млекопитающих с целью получения из них культур ЭПК позволяет создать экспериментальные модели для изучения in vitro процессов цитодифференцировки. Однако, получение и культивирование ППЗК весьма сложный и трудоемкий процесс. Для нас представляло интерес получить и охарактеризовать культуру ППЗК из плодов свиней.
ППЗК выделяли из плодов, взятых от свиноматок, которых забивали в различные сроки супоросности: на 23-и, 26-е, 31-е, 33-и сут.
Методом выделения и очистки от других клеточных типов, базирующимся на дифференциальной адгезии клеток к поверхности (Савченкова И.П., 2001), нами были получены популяции клеток, принятые за ППЗК (Таблица 6).
Таблица 6 - Результаты очистки свиных ППЗК с помощью дифференциальной адгезии к поверхности
| Возраст плода (сут.) | Количество плодов | Общее количество выделенных клеток на 1 плод | Количество ППЗК на 1 плод | Чистота клеточной популяции ППЗК (%) |
| 23 | 14 | 2475000 | 737428 | 30 |
| 26 | 16 | 3359362 | 1269524 | 38 |
| 31 | 15 | 5792876 | 3674279 | 63 |
| 33 | 6 | 5918444 | 4537000 | 77 |
Было установлено, что ППЗК свиней обладают низкой адгезивной способностью. Поэтому метод разделения гоноцитов от примеси соматических клеток позволяет сформировать популяцию клеток, в среднем на 52% представленную ППЗК свиньи.
Основными критериями, на которых базировался отбор предполагаемых ППЗК, были их морфологические особенности и наличие фермента щелочной фосфатазы. Свежеизолированные ППЗК свиней показывали положительную реакцию на эндогенную щелочную фосфатазу, для них были характерны шарообразная форма и наличие крупного ядра, окруженного узким ободком цитоплазмы, размер клеток достигал в среднем приблизительно 13 мкм в диаметре. Кроме того, мы также наблюдали наличие выростов цитоплазмы - псевдоподий у ППЗК, мигрирующих в зачатки гонад.
Таким образом, выявленные в данной работе морфологические и биохимические свойства ППЗК согласуются с описанными в литературе.
- Культивирование ППЗК свиньи
Культивирование ППЗК млекопитающих имеет большие трудности, связанные, прежде всего, с длительным поддержанием их в культуре, поэтому для нас представляло интерес изучить факторы, влияющие на длительное поддержание ППЗК in vitro.
После очистки ППЗК от примеси соматических клеток с использованием метода дифференциальной адгезии к поверхности и подсчета клеточной популяции, ростовую среду, содержащую ППЗК, в равных количествах переносили в чашки Петри с d=6 см на питательный слой, представленный монослоем из STO-клеток.
В результате эксперимента было установлено, что использование фидерного слоя в качестве подложки, является необходимым условием при культивировании ППЗК свиней. Мы обнаружили, что когда ППЗК культивировали в отсутствие питательного слоя, то они сохраняли жизнеспособность только на протяжение 24-х ч.
С целью получения клеточной линии ЭПК мы попытались провести клонирование колоний, которое осуществляли на 8-е сут. культивирования ППЗК.
В результате были получены клоны ЭПК на питательных слоях, представленных STO-клетками. Так, в одной из лунок на 6-е сут. культивирования мы наблюдали образование 3-х новых колоний, которые сохраняли фенотип, характерный для эмбриональных стволовых клеток (ЭСК), после перенесенных манипуляций.
В результате субклонирования было получено 28 компактных колоний клеток с типичным ЭСК-подобным фенотипом. Данные клетки не содержали жировых вакуолей и каких-либо других включений в цитоплазме, но каждая из них характеризовалась наличием ядрышка в ядре. Размер клеток в колониях достигал от 10 до 13 мкм в диаметре. При окраске таких колоний на ЩФ была отмечена позитивная реакция.
Представленная нами характеристика колоний ЭПК совпадает с имеющимися по этому вопросу литературными сведениями.
- Направленная in vitro дифференцировка ЭПК свиньи в инсулин-секретирующие клетки
Для индукции дифференцировки СК в клетки-продуценты инсулина мы использовали метод, описанный в работе O.Clark et al. (2007), для чего высевали очищенные ЭПК в коллагенизированные лунки планшета с добавлением 5 ммоль глюкозы, гидрокортизона, аскорбиновой кислоты, а также факторов роста – b-FGF (фибробластный), IGF (инсулиноподобный), VEGF (фактор роста эндотелия сосудов), EGF (эпидермальный).
На 14 день культивирования в индукционной среде отмечалось формирование клеточных кластеров сферической формы. Колонии с подобной морфологией мы отмечали при культивировании свежевыделенной островковой ткани ПЖ плодов кролика и собаки.
Для выявления секреции инсулина мы провели стимуляцию полученных колоний клеток глюкозой. В результате было установлено, что экспозиция с повышенными концентрациями глюкозы приводила к увеличению количества инсулина в культуральной среде в 7 раз, достигая максимальных значений 200-220 мкИЕ/мл при концентрации глюкозы 25 ммоль/л.
Иммуноцитохимическое окрашивание позволило выявить инсулин-позитивные клетки в полученной популяции.
С помощью ОТ-ПЦР был обнаружен продукт экспрессии гена инсулина, клетками, формирующими островково-подобные кластеры (Рис.8).
Актин Инсулин М.м К+ ЭПК К- К+ ЭПК К- 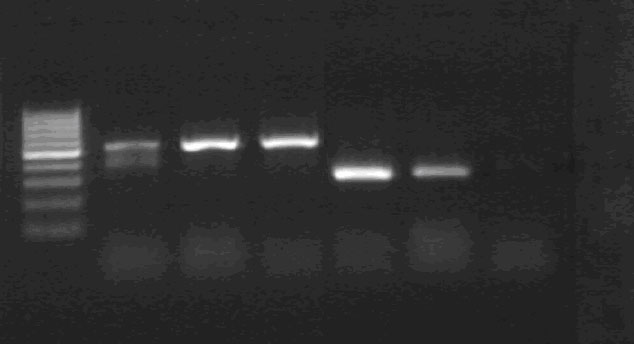 | К+ ЭПК К- 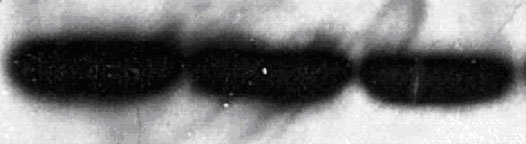 |
| Рис.8. Уровень экспрессии мРНК АСТ и INS в клетках. ОТ-ПЦР. | Рис. 9. Содержание белка инсулина в клетках. Вестерн-блот. |
| Примечание: ЭПК- Дифференцированные инсулин-продуцирующие клетки К- СПЭВ (Контроль -) К+ Свиная ПЖ (Контроль+) | |
Вестерн-блот анализ на выявление в клетках внутриклеточного инсулина показал достаточно высокое его количество в дифференцированных клетках (Рис.9).
На основании полученных данных мы сделали вывод, что ЭПК, полученные из ППЗК свиньи при индукции могут формировать in vitro инсулин-секретирующие клетки с морфологией -клеток ПЖ.
- Ксеногенная трансплантация -клеток поджелудочной железы плодов кролика лабораторным животным с индуцированным СД
В данной экспериментальной работе мы исследовали влияние ксеногенной культуры ОК, полученной из ПЖ плодов кролика, на организм мышей с экспериментальным (стрептозотоциновым) СД. Нам было важно подтвердить природу полученных нами -клеток ПЖ плодов кролика, изучить качество и степень очистки материала, а также показать эффект от трансплантации этих клеток на течение СД и развитие его осложнений у лабораторных мышей.
После внутривенного введения стрептозотоцина в дозе 150 мг/кг у всех подопытных мышей развился тяжелый СД с высокой гликемией (более 20 ммоль/л) без тенденции к спонтанной реверсии. Наблюдалась полифагия, полидипсия, полиурия, выпадение шерсти, похудание, гиподинамия.
Через 10 сут. после введения STZ произвели контроль гликемии, а затем интрапаренхиматозную внутрипеченочную ксенотрансплантацию культуры -клеток ПЖ кролика в дозе 105 кл/0,5 мл раствора на животное.
Таблица 7 - Характеристики экспериментальных групп мышей с индуцированным СД
| Группы | Сроки после трансплантации (сут.) | ||||||||||||
| -1 | 1 | 3 | 7 | 14 | 21 | 28 | 35 | 42 | 49 | 56 | |||
| Контроль | - | Глюк., ммоль/л | 7,1 ±0,3 | 7,0 ±0,2 | 7,5 ±0,3 | 7,3 ±0,4 | 7,1 ±0,4 | 7,4 ±0,3 | 7,4 ±0,2 | 7,0 ±0,3 | 7,8 ±0,4 | 7,2 ±0,3 | 7,3 ±0,3 |
| Масса, г. | 27 ±0,4 | 27,2 ±0,5 | 26,8 ±0,4 | 28,1 ±0,3 | 27,8 ±0,5 | 28,2 ±0,4 | 28,0 ±0,3 | 28,0 ±0,4 | 29,4 ±0,5 | 29,5 ±0,3 | 29,3 ±0,4 | ||
| Диабет | STZ | Глюк., ммоль/л | 20,3 ±0,5 | 23,5 ±0,7 | 25,8 ±0,3 | 38,2 ±0,5 | - | - | - | - | - | - | - |
| Масса, г. | 23,4 ±0,4 | 23,7 ±0,5 | 21,9 ±0,4 | 20,4 ±0,2 | - | - | - | - | - | - | - | ||
| Диабет + транспл. | STZ | Глюк., ммоль/л | 20,8 ±0,5 | 21,3 ±0,8 | 17,5 ±0,7 | 12,8 ±0,6 | 10,4 ±0,3 | 8,2 ±0,7 | 8,3 ±0,4 | 7,9 ±0,3 | 7,8 ±0,5 | 7,1 ±0,4 | 6,9 ±0,4 |
| Масса, г. | 22,8 ±0,4 | 23,4 ±0,5 | 23,0 ±0,5 | 23,5 ±0,4 | 23,7 ±0,3 | 24,1 ±0,4 | 25,1 ±0,5 | 27,2 ±0,6 | 28,0 ±0,4 | 27,2 ±0,5 | 28,4 ±0,4 | ||
После трансплантации у 7 из 8 мышей (88 %) группы «Диабет + трансплантация» на 21 сут. установилась нормогликемия (8,2±0,7 ммоль/л), что свидетельствовало о влиянии трансплантированных -клеток на течение диабета (Таблица 7). При этом наблюдали стабилизацию массы тела и нормализацию потребления воды. Эти характеристики сохранялись в течение 8 недель без иммуносупрессии.
В группе «Диабет» (животные с экспериментальным диабетом без трансплантации) отмечалось ухудшение общего состояния животных, нарастание всех признаков диабета, стойкая гипергликемия (20- 38 ммоль/л). Одна мышь погибла на 13-е сут. после введения STZ, 3 мыши на 14-е сут., 5 мышей погибли к 17-му дню эксперимента. Масса больных животных (20-23 г.) снизилась с начала эксперимента на 20-25 %. Таким образом, все мыши данной группы погибли в результате стойкой гипергликемии.
В контрольной группе животных изменений общего состояния и массы тела не отмечали при наличии стойкой нормогликемии (7,1-7,8 ммоль/л).
Статистическая обработка данных эксперимента показала достоверность результатов при Р<0,05.
Таким образом, результаты наших экспериментов показали, что трансплантация культуры фетальных кроличьих -клеток лабораторным мышам с экспериментальным СД позволяет добиться снижения уровня глюкозы крови и его нормализации на протяжении всего срока наблюдения (60 дней) без введения экзогенного инсулина. Полученные нами данные согласуются с таковыми отечественных и зарубежных исследователей (Rajotte R., 1983, Скалецкий Н.Н., 1987, Пужалин А. Н., 2006, Писарев В.Б. с соавт., 2009). Кроме того, нормализация уровня глюкозы после трансплантации происходила без применения иммуносупрессантов, что позволило нам сделать вывод о возможности исследования выделенных нами прокультивированных и очищенных ОК плодов кролика в клинической ксенотрансплантации домашним животным при лечении инсулинозависимого СД.
- Определение иммуногенности -клеток плодов кроликов и вероятности иммуноотторжения посредством экспериментальной трансплантации
Ксенотрансплантация культур ОК лабораторным собакам позволила оценить степень иммуногенности культуры клеток и необходимость применения иммуносупрессивной терапии животным-реципиентам, больным СД.
Существует мнение, что при использовании предварительно культивированных ОК длительная ремиссия диабетического статуса может быть достигнута без иммуносупрессии, а также повторная трансплантация таких клеток не вызывает сенсибилизации организма (Блюмкин В. Н. с соавт., 1983; Скалецкий Н.Н., 1987).
Мы проверили степень реакции организма реципиента на введение культивированных ОК на лабораторных беспородных собаках вивария ветеринарной клиники «Биоконтроль» (РОНЦ РАМН).
-клетки плодов кроликов на 6 сут. культивирования вводили лабораторным собакам подкожно в количестве 100 тыс. клеток на 1 кг веса в область холки двукратно с интервалом в 19 сут.
Иммуносупрессию при введении клеток не проводили. Наблюдение за собаками проводили неотрывно в течение 24 ч после каждого введения клеток, далее в течение 14 сут. после первого введения и 4 сут. после повторного введения. Оценивали общее состояние животного, а также биохимические и общеклинические показатели крови на 7-14 и 23 сут. после начала эксперимента.
У собаки №1 наблюдали до опыта нейтрофильный лейкоцитоз, однако, при этом отмечали динамику снижения палочкоядерных нейтрофилов на 14 и 23 сут. после опыта. На 14 сут. наблюдали увеличение числа эозинофилов, количество которых на 4 сут. после второго введения клеток вернулось к норме. Снижение количества тромбоцитов вместе с усилением активности аминотрансфераз и нейтрофилезом свидетельствует о наличии вирусной инфекции (в частности, аденовирозе) у собаки.
У собаки №2 до начала эксперимента наблюдали ярко выраженную форму анемии, нейтрофилез, в основном за счет сегментоядерных клеток, увеличение числа моноцитов и эозинофилез; снижение активности панкреатической амилазы. После первого введения клеток наблюдали увеличение количества эозинофилов, после повторного введения их число было ниже предыдущего. После обоих введений клеток наблюдали динамику роста активности аминотрансфераз и снижения активности панкреатической амилазы.
У собаки №3 наблюдали явления анемии после 2-х введений клеток. Количество тромбоцитов было понижено и оставалось примерно на одном уровне на всем продолжении эксперимента. Перед началом опытов у собаки наблюдали нейтрофилез (за счет палочкоядерных нейтрофилов) и эозинофилез. После введения клеток количество эозинофилов вернулось в пределы нормы, наблюдали динамику снижения числа нейтрофилов. Активность панкреатической амилазы снижена на протяжении всего эксперимента. Через 14 сут. после первого введения клеток наблюдали увеличение количества креатинина в сыворотке крови, что связано с эндогенными причинами и отношения к опыту не имеет.
Считаем, что эозинофилез у собак №1 и №2 не был связан с введением клеток, потому что второе введение спровоцировало бы еще более сильную аллергическую реакцию со стороны организма. Лейкоцитоза и тромбоцитоза после введения клеток не наблюдали. За время наблюдения состояние животных было удовлетворительным, признаков иммунных реакций, беспокойства, угнетения не наблюдали.
Данная работа позволила нам заключить, что иммунная реакция со стороны экспериментальных собак на введение -клеток плодов кроликов отсутствовала. Это является обоснованием возможности проведения клинической трансплантации -клеток животным, больным СД.
- Изучение влияния -клеток, выделенных из поджелудочной железы плодов кролика, на течение инсулинозависимого сахарного диабета после их введения собакам и кошкам
Было изучено влияние трансплантированных -клеток на течение СД у домашних животных: пяти собак и трёх котов.
В исследования включали животных с клиническими проявлениями СД: полидипсией, полиурией, полифагией, ожирением или нарастающей кахексией, с лабораторно установленной глюкозурией и гипергликемией, с согласия владельца животного.
По мнению Шумакова В.И. с соавт. (1995) и Shapiro J. et al. (2002), аллотрансплантация ОК считается более приоритетным методом, в связи с идентичностью клеточного материала донора и реципиента. При этом происходит синтез инсулина, что обеспечивает максимальную компенсацию СД и минимизирует риск развития осложнений ИЗСД. Однако Chu G. et al. (1997) продемонстрировали, что именно ксеногенные ОК не подвергаются аутоиммунному повреждению, что характерно для аллотрансплантации.
Ксеногенную трансплантацию -клеток использовали Блюмкин В. Н. с соавт. (1983) и Скалецкий Н.Н. (1987), которые показали, что предварительное культивирование -клеток ксеногенных культур позволяет достигнуть длительной ремиссии течения диабета без иммуносупресии. В связи с этим, представляло интерес изучить влияние -клеток, выделенных из ПЖ плодов кролика, на течение ИЗСД после их введения собакам и кошкам.
Собакам и котам очищенные предварительно путем культивирования -клетки ПЖ плодов кролика мы трансплантировали чрезкожно в паренхиму печени под эхографическим контролем в количестве 100 тыс. клеток на 1 кг массы тела.
При выборе иммунопривилигированной зоны для переноса клеточной суспензии мы руководствовались результатами многих учёных, показавших, что внутрипечёночная пересадка признана наиболее эффективным способом введения -клеток. Так, Bretzel R. et al. (1978) показали, что островки, трансплантированные в печень, способны к выживанию в течение нескольких лет, способствуя нормализации углеводного обмена и уровня гликозилированного гемоглобина, при отсутствии гипогликемии. При этом отсутствовали признаки отторжения и рецидива аутоиммунности, что было подтверждено гистологическими исследованиями. Ранее Najarian J. et al. (1977) вводя культуру -клеток в воротную вену, добились снижения потребности в инсулине у 3 из 4 больных сроком до 18 месяцев. Alejandro R. et al. (2002) использовали внутрипортальную трансплантацию и добились полного отсутствия инсулиновой зависимости в течение года.
Сразу после трансплантации мы отменяли либо значительно снижали дозу вводимого инсулина и наблюдения за животными выполняли под ежедневным контролем уровня глюкозы в крови. Назначение инсулина проводили только в случаях значительного превышения нормального уровня глюкозы и неудовлетворительного состояния животного.
В случае необходимости проводили симптоматическое лечение сопутствующих патологий. Уровень глюкозы в крови после трансплантации определяли хозяева животных глюкометром в домашних условиях 1-4 раза в сут. Биохимическое, клиническое исследование крови и общий анализ мочи проводили за 2-3 сут. до трансплантации и на 5, 21 и 60 сут. после трансплантации, затем по необходимости.
Об эффективности проведённой трансплантации судили по снижению потребности в экзогенном инсулине, уменьшении уровня глюкозы крови и мочи, нормализации показателей липидного обмена (кетоацидоза), течению диабетической полинейропатии и нефропатии, исчезновению полидипсии и полиурии, улучшению общего состояния и повышению активности.
В результате мы провели трансплантацию -клеток ПЖ плодов кроликов восьми инсулинозависимым животным с диагнозом СД. Следует заметить, что состояние животных, взятых в опыт, было изначально разным: у одних отсутствовали признаки осложнений, у других животных были ярко выражены, одним животным диагноз был поставлен давно, другие только недавно поступили на лечение. Как видно из данных, представленных в Таблице 8, положительного результата мы добились у 6 животных. Наблюдали улучшение лабораторных показателей, таких как снижение уровня глюкозы в крови и моче, исчезновение кетоацидоза. На Рис. 10-19 представлены графики, отражающие динамику изменения уровня глюкозы в крови и доз вводимого инсулина.
По результатам проведённого эксперимента можно сделать выводы, что внутрипечёночная трансплантация очищенных плодных -клеток кролика позволяет достичь нормоголикемии у больных СД животных с полным отказом от эндогенного инсулина в 4 случаях из 8 (50 % от общего числа экспериментальных животных). В 2-х случаях из 8 было продемонстрировано снижение дозы экзогенного инсулина на 60 % и на 80 % в течение 8 мес. (25 % от общего числа экспериментальных животных). Трансплантация оказалась неэффективной в 2 случаях из 8 (25%). Неудача в 1 случае из 2 объясняется наличием стероидного диабета-гиперкортицизма, при котором применяется принципиально другой тип лечения. Достоверно установлено, что у 6 животных из 8
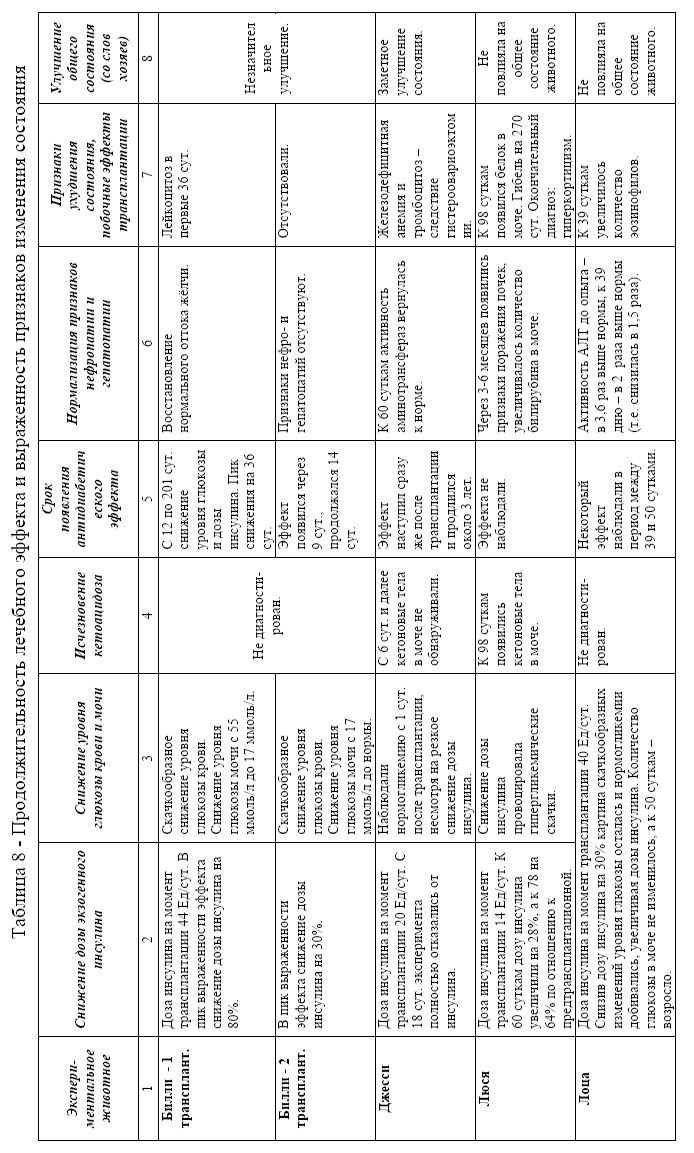

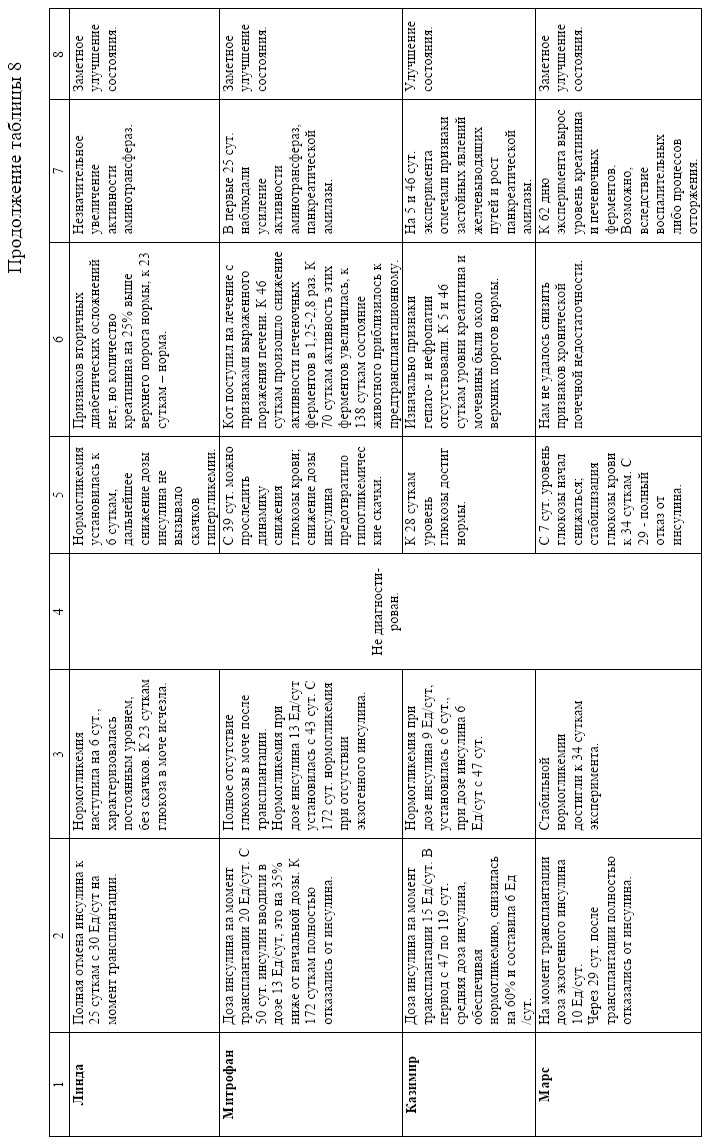

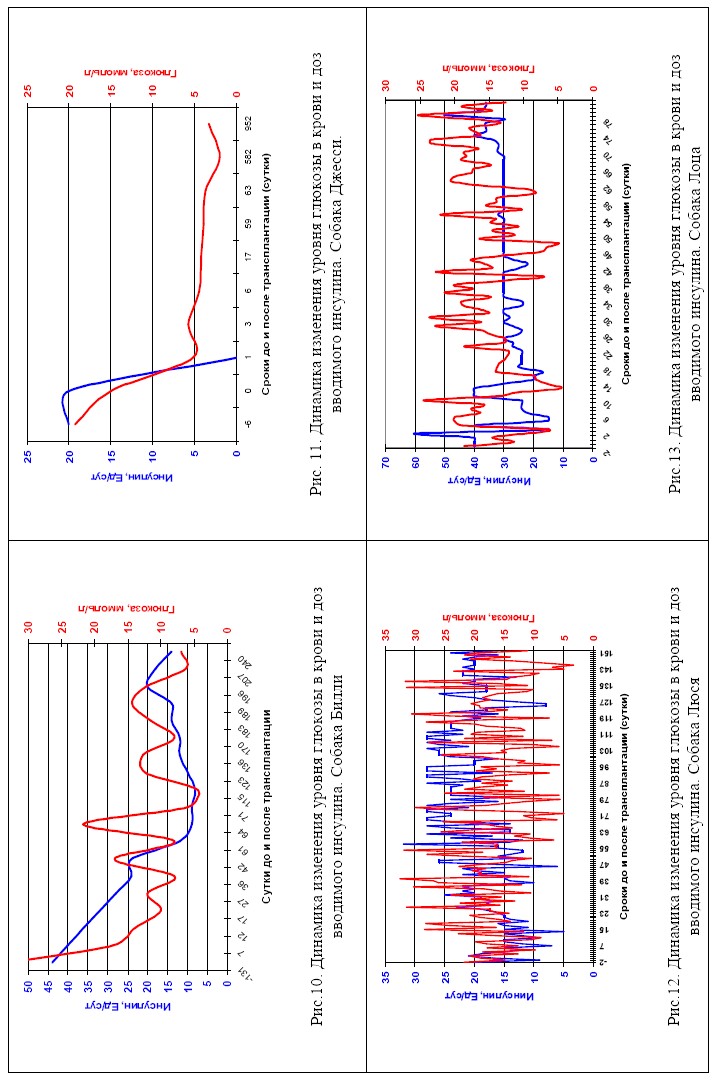

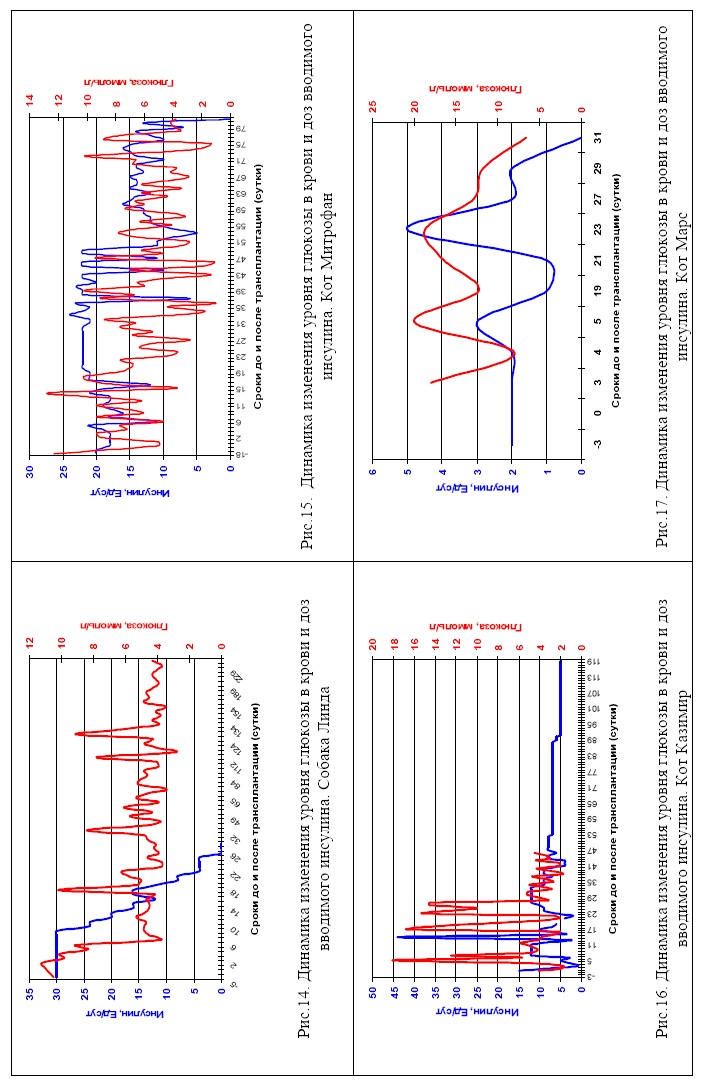

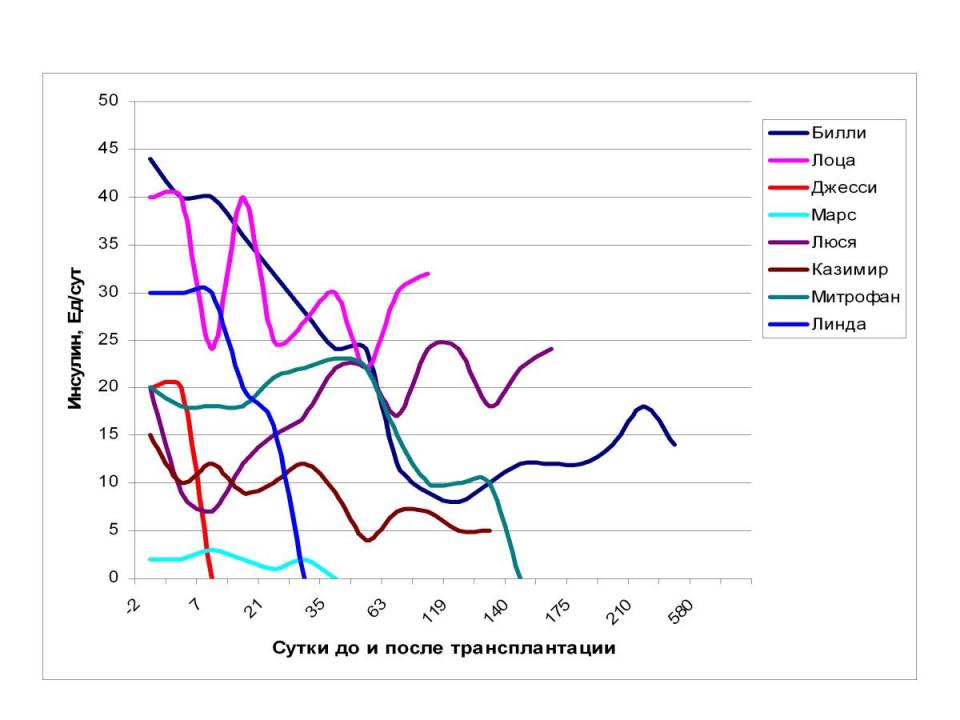
Рис.18. Сравнение динамики изменения дозы вводимого животным инсулина
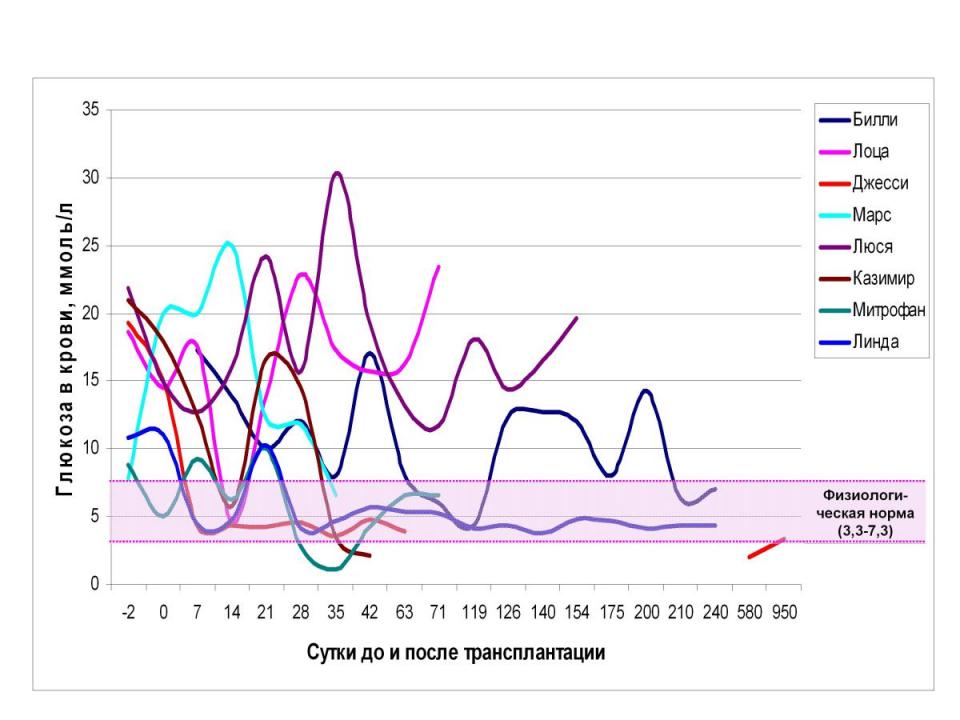
Рис.19. Сравнение динамики изменения уровня глюкозы у животных
испытуемых происходит улучшение лабораторных показателей: снижение уровня глюкозы в крови и моче, исчезновение кетоацитоза; значительное снижение доз экзогенного инсулина, либо отказ от него; улучшение течения сопутствующих СД осложнений (нефропатий, ангиопатий, гепатопатий).
Таким образом, можно предположить, что благодаря отсутствию «узнаваемости» очищенные путем культивирования -клетки ПЖ плодов кролика позволяют проводить ксеногенную трансплантацию материала собакам и кошкам без применения иммуносупрессантов. Кроме того, необходимо отметить, что способ трансплантации -клеток домашним животным в паренхиму печени, чрезкожно, под контролем ультразвука является неинвазивным способом и позволяет провести её без общей анестезии, без обездвиживания животного и без лапаротомии.
ВЫВОДЫ
- Получены культуры -клеток ПЖ, выделенные из плодов кроликов, собак и кошек, изучены их свойства и признаки:
а) по цитологическим признакам, наличию специфической альдегид-фуксин позитивной зернистости, специфическому окрашиванию мечеными АТ против инсулина, а также феномену дегрануляции, наступающему в ответ на повышение содержания глюкозы в культуральной среде, установлено, что выделенные клеточные популяции являются -клетками островков Лангерганса;
б) уровень продукции инсулина (в кондиционированных средах) - клетками кроликов составляет в среднем 80 мкИЕ/мл, собак - 84 мкИЕ/мл, кошек – 77 мкИЕ/мл, соответственно, на 3-4 сут культивирования;
в) выявлена низкая адгезивная способность -клеток ПЖ плодов кролика, которая позволяет их очистить от остальных типов клеток в процессе культивирования, посредством последовательного отбора и переноса в новые культуральные флаконы.
- Сравнительный анализ свойств и признаков -клеток, выделенных из ПЖ плодов кроликов, собак и кошек показал, что наиболее перспективным материалом для клеточной инженерии являются кроличьи -клетки.
- Получены межвидовые гибридные клоны – продуценты инсулина посредством слияния -клеток, выделенных из ПЖ плодов кролика, и клеток почки эмбрионов овец, дефектных по ТК (ПО ТК-), в соотношении 1:1, соответственно, в присутствии ПЭГ 1000:
а) сравнительный анализ межвидовых гибридных клонов ПО ТК- х кр. по способности продуцировать инсулин in vitro показал, что полученная популяция гетерогенна и представлена 4 клонами с повышенной продукцией инсулина (18-30 мкИЕ/мл).
б) отбор клонов с высокой продукцией инсулина и их последующее реклонирование позволяют сохранить продукцию инсулина in vitro в течение 24 пассажей и нормальный кариотип.
в) установлено, что длительное культивирование (до 54 пассажа) и перевод клеток в суспензионное культивирование приводит к снижению уровня продукции инсулина межвидовыми клеточными гибридами.
- Микролимфоцитотоксический тест показал, что межвидовая гибридная культура ПО ТК- х кр. обладает определенной гистологической совместимостью с антителами человека.
- Из 23-33-х суточных плодов свиньи выделены первичные половые клетки (ППЗК) и разработаны условия поддержания их в культуре. Установлено, что наличие фидерного слоя, представленного эмбриональными фибробластами мыши линии STO и среды ДМЕМ, дополненной 15% сыворотки плодов коров, 2mM альфа-глутамина, 10-6 mM 2-меркаптоэтанола позволяет получить колонии эмбриональных половых клеток (ЭПК) с фенотипом подобным ЭСК свиньи.
- Культивирование ЭПК свиньи в индукционной среде, содержащей глюкозу, гидрокортизон, аскорбиновую кислоту, а также факторы роста – b-FGF, IGF, VEGF, EGF ведет к их направленной дифференцировке in vitro в клетки с морфологией, подобной -клеткам ПЖ.
- Установлено, что трансплантация культуры фетальных кроличьих -клеток лабораторным мышам с экспериментальным СД позволяет добиться снижения уровня сахара в крови и его нормализации на протяжении 60 сут. без введения экзогенного инсулина. Нормализация уровня глюкозы после трансплантации происходит без применения иммуносупрессантов.
- Показано, что длительное культивирование -клеток ПЖ плодов кролика способствует снижению иммунной реакции у экспериментальных собак на их введение.
- Установлено, что ксеногенная трансплантация -клеток ПЖ плодов кролика позволяет добиться положительного результата у 6 животных из 8 испытуемых. В результате наблюдали: улучшение лабораторных показателей - снижение уровня глюкозы в крови и моче, исчезновение кетоацидоза; значительное снижение доз экзогенного инсулина, либо отказ от него; улучшение течения сопутствующих СД осложнений (нефропатий, ангиопатий, гепатопатий).
- Предложен новый неинвазивный способ введения -клеток домашним животным через брюшную стенку в паренхиму левой доли печени, под контролем ультразвука, который позволяет провести трансплантацию без общей анестезии, без обездвиживания животного и без лапаротомии.
ПРАКТИЧЕСКИЕ ПРЕДЛОЖЕНИЯ
- Очищенные путем культивирования -клетки ПЖ кролика могут быть использованы для клинической трансплантации животным, больным СД.
- Гибридную культуру ПО ТК- х кр. возможно использовать для дальнейших исследований, направленных на получение постоянной линии клеток, продуцирующей инсулин in vitro.
- -клетки, получаемые дифференцировкой из ППЗК, возможно применять в дальнейших исследованиях, направленных на разработку методов клеточной терапии для лечения СД.
- Трансплантация -клеток ПЖ плода кролика непосредственно через брюшную стенку в паренхиму левой доли печени, без применения иммуносупрессивной терапии, позволяет добиться снижения уровня глюкозы крови и улучшения течения ангиопатий у больных СД.
Список работ, опубликованных по теме диссертации
Статьи, опубликованные в журналах, рекомендованных ВАК РФ
- Приданцева Т.А. Выделение и культивирование примордиальных половых зародышевых клеток свиньи / Т.А. Приданцева, И.П. Савченкова, Абдрахманов И.К. // Ветеринарная патология. - 2003.- №1(5). – С. 37-39.
- Абдрахманов И. К. Стволовые клетки животных (История и перспективы) / И. К. Абдрахманов // Ветеринарная патология.– 2005.- №1(12).– С. 55-58.
- Сережина Л.А. Клинические наблюдения за результатами внутрипеченочной трансплантации ксеногенных островковых клеток поджелудочной железы плодов кролика трем животным при лечении сахарного диабета / Л.А. Сережина, Н.М. Туржанская, Л.П. Дьяконов, И.К. Абдрахманов, М.А. Селюгин, Ю.А. Кузнецов // Российский ветеринарный журнал. Мелкие домашние и дикие животные. -2005.- № 3.- С. 13-15.
- Кузнецов Ю.А. Сахарный диабет мелких домашних животных / Ю.А. Кузнецов, М.А. Селюгин, И.К. Абдрахманов // Ветеринарная патология. – 2006. - №2 (17). - С. 81-85.
- Абдрахманов И.К. Гибридные клеточные системы – новый подход в биотехнологии продуцентов биологически активных веществ / И.К. Абдрахманов, Т.В. Гальнбек, Н.Н. Скалецкий, М.Л. Фридман, Л.П. Дьяконов, П.М. Кленовицкий // Фундаментальные исследования.– 2008.- № 5.- С. 13.
- Фридман М.Л. Стволовые клетки кожи – перспективный источник генетического материала редких и исчезающих видов животных / М.Л. Фридман, И.К. Абдрахманов // Ветеринарная патология. - 2008. -№4. - С. 62-65.
- Абдрахманов И.К. Внутрипеченочная трансплантация островковых клеток поджелудочной железы для лечения сахарного диабета у домашних животных (Собаки и кошки) / И.К. Абдрахманов, М.А. Селюгин, Ю.А. Кузнецов, Л.П. Дьяконов, Л.А. Сережина, И.Ф. Вилковыский // Ветеринарный врач. -2008. -№6. - С. 37-38.
- Абдрахманов И.К. Клинические результаты внутрипеченочной трансплантации ксеногенных островковых клеток поджелудочной железы плодов кролика домашним животным при сахарном диабете / И.К. Абдрахманов, Л.А. Сережина, М.А. Селюгин, Н.М. Туржанская, Ю.А. Кузнецов, И.Ф. Вилковыский, Н.Б. Савенко, В.Н. Митин, Л.П. Дьяконов // Российский ветеринарный журнал. - 2011. - №2. – С. 14-18.
- Абдрахманов И.К. Пути преодоления иммунного отторжения при ксенотрансплантации островковых клеток поджелудочной железы в лечении сахарного диабета / И.К. Абдрахманов, Л.А. Сережина, М.А. Селюгин, Н.М. Туржанская, Ю.А. Кузнецов, И.Ф. Вилковыский, Н.Б. Савенко, В.Н. Митин, Л.П. Дьяконов // Ветеринарный врач. – 2011. - №4. – С. 31-34.
- Абдрахманов И.К. Культуры -клеток поджелудочной железы животных – источник материала для трансплантации в терапии сахарного диабета домашних животных / И.К. Абдрахманов, Н.Б. Савенко // Достижения науки и техники АПК. – 2011. - №8. - С.63-65.
Патент на изобретение
- Способ получения трансплантата для лечения сахарного диабета у собак и кошек и способ лечения сахарного диабета у собак и кошек. Абдрахманов И.К. [и др.]: патент, на изобретение РФ №2325921. - 2006.
Статьи, материалы, тезисы
- Приданцева Т.А. Влияние возраста плодов свиньи на выделение из них примордиальных половых зародышевых клеток / Т.А. Приданцева, И.П. Савченкова, И.К. Абдрахманов, Г.Ф. Жирков, Л.К. Эрнст // Материалы научно-практической конференции по проблеме «Повышение конкурентоспособности животноводства и задачи кадрового обеспечения». – РАМЖ – п. Быково, Московская область, 2000. - С. 84.
- Приданцева Т.А. Влияние возраста плодов свиньи на выделение из них примордиальных половых зародышевых клеток и получение колоний с морфологией эмбриональных стволовых клеток / Т.А. Приданцева, И.П. Савченкова, И.К. Абдрахманов, Г.Ф. Жирков, Л.К. Эрнст // Тезисы докладов научной конференции, посвященной 60-летию ВНИИ генетики и разведения сельскохозяйственных животных, «Селекционно-генетические методы повышения продуктивности сельскохозяйственных животных». – ВНИИРГЖ - Санкт- Петербург, 2000. – С. 64-65.
- Приданцева Т.А. Выделение примордиальных половых зародышевых клеток из плодов свиньи / Т.А. Приданцева, И.П. Савченкова, И.К. Абдрахманов, Г.Ф. Жирков, Л.К. Эрнст // Тезисы докладов II-ой Международной научной конференции «Биотехнология в растениеводстве, животноводстве и ветеринарии». – ВНИИСХБ – Москва, 2000. - С. 44-46.
- Pridantseva T. Isolation of primordial germ cells from pig fetuses / T. Pridantseva, I. Savchenkova, I. Abdrakhmanov // Proceedings of the VIIth International Congress of Andrology «Andrology in the 21st Century». - Montreal, Quebec, Canada, 2001. – рр. 143-148.
- Абдрахманов И.К. Сравнительный анализ эффективности ретровирусных векторов в переносе экзогенной ДНК в клетки млекопитающих, культивируемые in vitro / И.К. Абдрахманов, И.П. Савченкова, Т.А. Приданцева, Н.А. Зиновьева, Л.К. Эрнст // Доклады РАСХН. - 2001. - № 5. – С. 30-31.
- Teplyashin A. Characterization of human MSC-like cells isolated from bone marrow, adipose tissue, skin and placenta / A. Teplyashin, N. Tchupikova, S. Sharifullina, M. Rostovskaya, S. Korjikova, I. Abdrakhmanov, A. Dunaev, S. Petrin, I. Savtchenkova // Annual Fall Meeting of German Society for Biochemistry and Molecular Biology, Mnster, 2004.
- Абдрахманов И.К. Получение островковых клеток поджелудочной железы плодов кролика и предпосылки для их клинического применения в ветеринарной медицине / И.К. Абдрахманов, Л.П. Дьяконов, М.А. Селюгин, Ю.А. Кузнецов // Тезисы докладов международного симпозиума «Научные основы обеспечения защиты животных от экотоксикантов, радионуклидов и возбудителей опасных инфекционных заболеваний». – Казань, 2005. - С. 416-420.
- Дьяконов Л.П. Кариологическая характеристика некоторых межвидовых гибридных культур клеток животных. Актуальные проблемы инфекционной патологии и иммунологии животных / Дьяконов Л.П., Гальнбек Т.В., Сафина А.Н., Симонова А.С., Савенко Н.Б., Абдрахманов И.К., Кленовицкий П.М. // Сб. научн. тр. ВИЭВ, 2006. - С. 635-640.
- Каталог Специализированной коллекции перевиваемых соматических клеточных культур сельскохозяйственных и промысловых животных РККК(П), (СХЖ РАСХН). Л.П. Дьяконов, Т.В. Гальнбек, Г.Т. Акиншина, И.К. Абдрахманов [и др.]. Всерос. науч.-исслед. ин-т эксперим. ветеринарии им. Я.Р. Коваленко (ВИЭВ), Отдел клеточной биотехнологии и питательных сред. - 2-е изд. (доп., уточнен.). - Москва, 2006. - 115 с.
- Zhukova O.S. Cytotoxic effect of catalytic system containing phtalocyanine and naphtalocyanine complexes and ascorbic acid on normal and tumor cells / O.S. Zhukova, I.K. Abdrakhmanov, G.K. Gerassimova, L.P. Dyakonov // Abstracts 46th ETCS International Meeting “In vitro cytotoxicity mechanisms”. Verona, March 26-29, 2006. - Р.46.
- Абдрахманов И.К. Гибридные клеточные системы – новый подход в биотехнологии продуцентов биологически активных веществ / И.К. Абдрахманов, Т.В. Гальнбек, М.Л. Фридман, Л.П. Дьяконов // Материалы международной научно-практической конференции «Современное состояние и перспективы исследовании по инфекционной и протозойной патологии животных, рыб и пчел». – ВИЭВ, Москва, 2008. – С.307-311.
- Радиоэкотоксикологическая микробиология / Иванов А.В., Низамов Р.Н., Плотникова Э.М., Абдрахманов И.К.// – М.: Колос, 2009. – 680 с.

