Комплексное клинико-организационное исследование патологии почек у детей на территориях эколого-биогеохимического риска (на материалах чувашской республики)
На правах рукописи
ИВАНОВА
Ирина Евгеньевна
КОМПЛЕКСНОЕ КЛИНИКО-ОРГАНИЗАЦИОННОЕ ИССЛЕДОВАНИЕ ПАТОЛОГИИ ПОЧЕК У ДЕТЕЙ НА ТЕРРИТОРИЯХ ЭКОЛОГО-БИОГЕОХИМИЧЕСКОГО РИСКА
(на материалах Чувашской Республики)
14.01.08 – педиатрия
14.02.03 – общественное здоровье и здравоохранение
АВТОРЕФЕРАТ
диссертация на соискание ученой степени
доктора медицинских наук
Казань - 2011
Работа выполнена в Государственном образовательном учреждении дополнительного профессионального образования «Институт усовершенствования врачей» Министерства здравоохранения и социального развития Чувашской Республики
Научные консультанты:
доктор медицинских наук, профессор Скальный Анатолий Викторович
доктор медицинских наук Яковлева Татьяна Владимировна
Официальные оппоненты:
доктор медицинских наук, профессор Длин Владимир Викторович
доктор медицинских наук, профессор Софронов Валерий Викторович
доктор медицинских наук, профессор Альбицкий Валерий Юрьевич
Ведущая организация: Государственное образовательное учреждение высшего профессионального образования «Нижегородская государственная медицинская академия» Министерства здравоохранения и социального развития Российской Федерации
Защита диссертации состоится «9» сентября 2011 года в 9.30 часов на заседании диссертационного совета Д 208.034.03 при ГОУ ВПО «Казанский государственный медицинский университет» Министерства здравоохранения и социального развития Российской Федерации по адресу: 420012, Республика Татарстан, г. Казань, ул. Бутлерова, 49
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО «Казанский государственный медицинский университет» Министерства здравоохранения и социального развития Российской Федерации по адресу: 420012, Республика Татарстан, г. Казань, ул. Бутлерова, 49
Автореферат разослан «___» _______________________2011г.
Ученый секретарь
диссертационного совета
кандидат медицинских наук,
доцент Г.Р. Хасанова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность. Состояние здоровья детей и подростков в современной России является одной их наиболее актуальных проблем не только педиатрической науки, но и медицины в целом. Это связано с тем, что на рубеже ХХ-ХХI веков у подрастающего поколения значительно ухудшились его показатели, что привело к возникновению реальной угрозы дальнейшего усугубления неблагоприятной демографической ситуации, уменьшения трудового, оборонного и интеллектуального потенциала страны (Баранов А.А., 2005, 2008; Бондарь И.В. с соавт., 2008; Щепин О.П., 2007, 2010; Кучма В.Р. с соавт., 2005; Орел В.И. с соавт., 2003; Скляр М.С., 2005; Яковлева Т.В., 2005). Данные официальной статистики и специальных исследований повсеместно регистрируют увеличение общей заболеваемости и инвалидности, нарастание хронических форм заболеваний, врожденных дефектов развития и генетических отклонений в структуре детской патологии (Богомолова Е.С. с соавт, 2007; Ермолаев Д.О., 2004; Маткивский Р.А., 2009; Медик В.А., 2004; Садыков М.М., 2008; Скляр М.С., 2008; Стародубов В.И. с соавт., 2004; ЮНИСЕФ, 2007; Murray C.J.L. et al., 2000). Причинами этого большинство исследователей считает увеличивающееся с каждым годом воздействие на растущий организм ребенка многочисленных неблагоприятных социально-гигиенических, эколого-биогеохимических и биологических факторов (Аверьянова Н.И. с соавт., 2007; Вельтищев Ю.Е. с соавт., 1996; Ермолаев О.Д, 2004; Иванников А.И., 2001; Маковецкая Г.А. с соавт., 2006; Родионов В.А., 2002; Ramsey F., 2008).
За последние годы среди другой патологии значительно выросла распространенность болезней почек, мочевыделительной системы и их врожденных аномалий (Баранов А.А. с соавт., 2007; Игнатова М.С., 2007, 2008, 2009; Маковецкая Г.А. с соавт., 2009; 2007; Перепелкина Н.Ю., 2003; Царегородцев А.В. с соавт., 2001; Чугунова О.Л., 2006; Enrich J.H. et al., 2005; Hogg R.J., 2003). В медицине разработано множество новых современных подходов к лечению и профилактике нефропатий, однако, несмотря на это, отмечается повсеместный рост уровня патологии органов мочевой системы, т.е. проблема не только не ликвидируется, но становится все более актуальной. Болезни почек составляют 5-6% общей заболеваемости населения, причем более 60% нефрологических больных моложе 40 лет (Рудов И.В., 2008). Следует также отметить высокие уровни смертности у лиц трудоспособного возраста от хронической почечной недостаточности, в 8-10 раз превышающие аналогичные показатели в других странах (Марченко В.В., 2006).
По данным ряда авторов к инвалидности приводят недостаточная профилактическая работа со здоровыми детьми, оздоровительная и реабилитационная – с детьми с хронической патологией, а нефрологические заболевания, как правило, имеют хроническое течение и редко заканчиваются выздоровлением (Баранов А.А. с соавт., 2008; Игнатова М.С., 2009; Лильин Е.Т., 2008). Все это требует дальнейших исследований, направленных на оптимизацию оказания медицинской помощи детям с уронефрологической патологией на разных этапах их реабилитации.
Одним из важнейших научно-практических направлений социальной педиатрии и организации здравоохранения является региональный подход к изучению состояния здоровья детей. На его формирование оказывают влияние климатогеографические, экологические и экономические условия проживания, степень миграции населения, этнические и социокультурные особенности, а также существенные различия в материально-технической базе лечебно-профилактических учреждений по регионам (Альбицкий В.Ю. с соавт., 2006; Баранов А.А. с соавт., 2008; В.И. Стародубов с соавт., 2004). Для рациональной организации детской нефрологической службы в РФ большое значение имеют сведения об эпидемиологии и региональных особенностях заболеваний органов мочевой системы у детей. В то же время в последние десятилетия установлены закономерные корреляции между биогеохимическими характеристиками отдельных регионов страны и распространением ряда патологических состояний (Агаджанян Н.А. с соавт., 2001). В Чувашии выявлены значительные различия в показателях здоровья, как взрослого, так и детского населения, в зависимости от геохимических особенностей территории проживания. Однако до настоящего времени эколого-биогеохимические аспекты уронефрологической заболеваемости детей не изучались, что и определило цель нашей работы.
Цель исследования: изучить особенности патологии почек у детей на территориях эколого-биогеохимического риска и разработать рекомендации по оптимизации деятельности детской нефрологической службы в регионе (на примере Чувашской Республики).
Задачи исследования:
- Изучить структуру и динамику показателей заболеваемости и инвалидности детского населения ЧР, выявить их особенности на территориях эколого-биогеохимического риска.
- Проанализировать структуру и динамику нефрологической заболеваемости детей в различных эколого-биогеохимических субрегионах.
- Дать клинико-статистическую характеристику хронической болезни почек у детей ЧР.
- Выявить особенности распространения врожденных пороков и малых аномалий развития почек у детей в зависимости от территории проживания.
- Исследовать уровень микро- и макроэлементов в волосах и моче у здоровых детей и детей с пороками почек на территориях с высокой распространенностью врожденной патологии.
- Выявить факторы риска возникновения и клинико-лабораторные особенности течения пиелонефрита у детей, проживающих в гетерогенных эколого-биогеохимических субрегионах.
- Провести экспертную оценку качества диспансеризации и медицинского обслуживания детей с заболеваниями почек и показать эффективность комплекса лечебно-оздоровительных мероприятий при хроническом пиелонефрите.
- Обосновать и разработать рекомендации по оптимизации детской нефрологической службы в ЧР.
Научная новизна. В результате проведенного комплексного клинико-организационного исследования нефрологической заболеваемости у детей 0-17 лет на региональном уровне с учетом эколого-биогеохимических особенностей территории проживания была получена следующая новая научная информация:
- выявлен значительный рост заболеваемости болезнями мочеполовой системы у детей и подростков ЧР;
- показано влияние эколого-биогеохимических факторов среды проживания на нефрологическую заболеваемость детей;
- определены клинические особенности течения пиелонефрита у детей в гетерогенных эколого-биогеохимических территориях;
- установлена нозологическая структура хронической болезни почек у детей и доля детей с 3-5-й стадиями этой патологии на уровне отдельного региона;
- доказано, что распространенность почечных мальформаций зависит от эколого-биогеохимических характеристик территории проживания детей. Впервые установлена популяционная частота врожденных пороков почек и некоторых малых аномалий развития (расщепление чашечно-лоханочной системы гипертрофированным столбиком Бертена, ротации, пиелоэктазии) по данным ультразвукового скрининга;
- показано, что дети с неосложненными врожденными пороками почек по сравнению со здоровыми имеют повышенное содержание токсичных элементов (алюминия, свинца, кадмия, олова, никеля) в волосах на фоне сниженного содержания эссенциальных микроэлементов (цинка, бериллия).
Практическая значимость. Проведенное исследование позволило использовать полученные данные в качестве источника объективной информации для обоснования и реализации мер, направленных на сохранение и укрепление здоровья детей с болезнями мочевой системы:
- на основе экспертизы качества диспансерного наблюдения детей с заболеваниями почек разработан и апробирован комплекс мер по повышению эффективности деятельности детской нефрологической службы;
- внедрен ультразвуковой скрининг почек в программу диспансеризации детей старше 1 года;
- установлено, что клинические особенности течения и проявления хронического пиелонефрита у детей в гетерогенных эколого-биогеохимических субрегионах определяют разные подходы к его лечению и профилактике обострений;
- выявлены региональные особенности структуры хронической болезни почек у детей, внедрен способ оценки функции почек на основе расчета скорости клубочковой фильтрации по формуле Шварца при диспансеризации детей с уронефрологической патологией, выделены группы детей с хронической болезнью почек 3-5-й стадий;
- разработаны ультразвуковые нормативы размеров почек;
- организованы республиканская и городская «Нефрошколы» для пациентов и родителей, разработана программа и методические рекомендации к занятиям;
- в работу детских Центров здоровья внедрена анкета-опросник для раннего выявления детей из группы риска по уронефрологической патологии;
- основные положения и выводы диссертации использованы в учебном процессе при разработке циклов лекций и семинаров для преподавания в системе постдипломного образования.
Внедрение результатов исследования в практику. Материалы диссертационной работы широко внедрены в практику управления здравоохранением на региональном и федеральном уровнях, в деятельность учреждений и служб по охране материнства и детства, использованы при подготовке документов и информационных материалов, в их числе:
- аналитические доклады Совета Федерации;
- государственные доклады «О состоянии здоровья населения Чувашской Республики» (2006, 2007, 2008, 2009);
- Республиканская целевая программа «Дети Чувашии»
на 2007-2010 годы (утверждена постановлением Кабинета Министров Чувашской Республики от 21.09.2006. № 238); - Приказ Министерства здравоохранения и социального развития Чувашской Республики №460 от 21.04.2010 «О проведении в 2010-2012 годах диспансеризации детей в возрасте 4, 9, 10 лет».
Практическое использование материалов исследования подтверждается актами внедрения, полученными из Минздравсоцразвития Чувашии, управления здравоохранения г. Чебоксары, ГОУ ДПО «Институт усовершенствования врачей» Минздравсоцразвития Чувашии на следующие научно-практические материалы:
- Информационные письма «Анализ нефрологической заболеваемости у детей и подростков Чувашской Республики», «Анализ заболеваемости у детей и подростков Чувашской Республики за 7 лет (2002-2008 гг.)».
- Анкета-опросник для Центров здоровья.
- Программа диспансерного наблюдения детей с вторичным ПиН на педиатрическом участке.
- Программы восстановительного лечения детей с уронефропатиями (для центров восстановительного лечения и восстановительных отделений детских поликлиник).
- Учебно-методическое пособие для врачей-курсантов ГОУ ДПО «Институт усовершенствования врачей» «Восстановительное лечение при пиелонефрите у детей».
- Алгоритмы действия участкового врача при выявлении уронефропатий.
- Региональные нормативы ультразвуковых размеров почек.
Апробация работы. Основные положения и результаты исследования доложены и обсуждены на IХ Конгрессе педиатров России «Актуальные проблемы педиатрии» (Москва, 2004), IV Педиатрическом форуме Приволжского федерального округа «Педиатрия и детская хирургия в Приволжском федеральном округе» (Казань, 2007), II съезде Российского общества медицинской элементологии (Тверь, 2008), VI Педиатрическом форуме Приволжского федерального округа «Педиатрия и детская хирургия в Приволжском федеральном округе» (Казань, 2009), на Межрегиональной научно-практической конференции, посвященной 10-летию ГОУ «Институт усовершенствования врачей» Минздрасоцразвития Чувашии (Чебоксары, 2009), IV Евроконгрессе педиатров (Москва, 2009), ХIV Конгрессе педиатров России с международным участием (Москва, 2010), на IV Международном симпозиуме Федерации европейских обществ по изучению макро- и микроэлементов «Макро- и микроэлементы в медицине и биологии» (Санкт-Петербург, 2010), на Республиканских научно-практических конференциях (Чебоксары, 2008, 2009, 2010), заседаниях общества детских врачей Чувашии (2003, 2004, 2008, 2009, 2010, 2011).
На защиту выносятся следующие основные положения:
- В Чувашской Республики в течение последних 7 лет наблюдается негативная тенденция в состоянии здоровья детского населения, выражающаяся в значительном росте его заболеваемости.
- Нефрологическая заболеваемость имеет высокую степень зависимости от эколого-биогеохимических особенностей территории проживания детей.
- Хроническая болезнь почек у детей требует проведения комплексного клинико-эпидемиологического исследования.
- Для детей с врожденными пороками развития почек характерен дисбаланс макро- и микроэлементов на стадии предболезни.
- Организация медицинской помощи детям с нефрологической патологией должна учитывать региональные и эколого-биогеохимические особенности территорий их проживания.
Публикация результатов исследования. По теме диссертации опубликовано 66 научных работ, из них - 14 статей в ведущих научных рецензируемых журналах, рекомендованных Высшей аттестационной комиссией РФ. Общий объем публикаций составляет 28,2 усл. печ. л., в том числе авторский вклад 19,3 усл. печ.л.
Личное участие диссертанта. Диссертант принимал участие в формировании целей и задач исследования, разработке этапов и направлений выполнения диссертации, выборе методов и объема исследований. Сбор первичных материалов и анализ результатов лабораторных исследований, а также интерпретация полученных данных осуществлялась непосредственно соискателем. Выдвинутые на защиту научные положения и выводы диссертации являются результатом самостоятельных исследований соискателя. Подготовка печатных работ к публикации выполнена автором лично.
Объем и структура диссертации. Общий объем работы составляет 374 страницы машинописного текста. Диссертация состоит из введения, 7 глав, заключения, выводов, практических рекомендаций, списка литературы и приложений. Работа иллюстрирована 81 таблицей и 46 рисунками. Библиографический указатель содержит 500 источников, из них 368 – отечественных и 132 – иностранных авторов.
СОДЕРЖАНИЕ РАБОТЫ
Объем и методы исследования. Научной основой настоящего исследования является комплексный подход, позволяющий рассматривать анализ патологии почек у детей на региональном уровне с учетом эколого-биогеохимических особенностей территории проживания и оптимизацию деятельности детской уронефрологической службы как одну из актуальных задач современной отечественной педиатрии и организации здравоохранения.
Исследование выполнялось в несколько этапов (табл. 1).
На 1-м этапе была изучена отечественная и зарубежная литература по вопросам общей и нефрологической заболеваемости и инвалидности у детей, ВПР, ИМС, факторам риска развития нефропатий, связи эколого-биогеохимических характеристик среды проживания ребенка и его патологии, роли нарушений элементного гомеостаза при различных патологических состояниях. Для этого выборочно было использовано 500 литературных источников, в т.ч. 368 – отечественных и 132 – иностранных авторов.
Таблица 1
Программа исследования
| № | Этапы | Методы | Источники и объём |
| 1. | Аналитический обзор отечественной и зарубежной литературы | Библиометрический Аналитический Сравнительный | Массив центральных и специальных публикаций - 500 источников |
| 2. | Районирование территории Чувашии по эколого-биогеохимическому принципу | Аналитический Картографирование | |
| 3. | Анализ показателей общей заболеваемости и инвалидности детей и подростков за 2002-2008 гг. в ЧР, особенностей заболеваемости детей на территории различного эколого-биогеохимического риска. | Статистический Аналитический Графоаналитический Сравнительный Клинический | Формы статистической отчетности №№ 12; 19; 31 в ЧР за 2002-2008 гг. - 50 документов |
| 4. | Анализ общей и госпитализированной нефрологической заболеваемости у детей и подростков ЧР. Изучение структуры госпитализированной нефрологической заболеваемости на территориях различного эколого-биогеохимического риска. Изучение особенностей ХБП у детей ЧР. | Статистический Аналитический Графоаналитический Сравнительный Клинический | Отчетно-статистические формы №№ 12; 31 в ЧР за 2002-2008 гг. - 43 документа Паспорт врачебного участка (педиатрического) (ф. 030/у-пед) с общей численностью детей 245 000 - 31 документ Истории болезней детей (ф. 003/у) – 10 885 Контрольная карта диспансерного наблюдения (ф. №30/у-04) – 625 |
| 5. | Ультразвуковое исследование почек с определением размеров и объема. Расчет распространенности ВПР и МАР почек. Исследование микроэлементного состава волос и мочи у детей с ВПР. | Клинический Аналитический Статистический Лабораторный | 8333 ребенка Определение 25 микроэлементов в волосах (80 образцов – 2000 исследований) и моче (20 образцов – 240 исследований) |
| 6. | Анализ клиники и течения ПиН у детей, проживающих на гетерогенных эколого-биогеохимических территориях. | Клинический Аналитический | Истории болезни (форма 003/у) - 923 Истории развития ребенка (форма 112/у) - 923 |
| 7. | Экспертная оценка качества оказания медицинской помощи детям с хроническим ПиН в поликлинике и стационаре. Проведение организационного эксперимента. | Клинический Аналитический Экспертный | Истории развития ребенка (ф. 112/у) - 360 Истории болезни (ф.003/у) - 540 96 детей |
| 8. | Анализ и изложение результатов исследования в печатных изданиях, разработка практических предложений по оптимизации детской уронефрологической службы, оформление диссертации. | Статистический Системного подхода Сравнительный Обобщение материала | 65 публикаций материалов исследований, в т.ч. 13 печатных работ в изданиях, рекомендованных ВАК. Информационные письма – 2. Учебно-методические пособия – 4. Монография. |
На 2-м этапе в соответствии с критериями оценки районирования по В.Л. Сусликову (2002) на территории Чувашии были очерчены 3 эколого-биогеохимических субрегиона и выбраны наиболее типичные районы в рамках указанной градации (рис. 1).
1. Прикубнино-Цивильский (ПКЦ) субрегион занимает 1/3 территории республики в восточной и центральной ее части. Большая часть его площади является степной с отдельными островками широколиственных лесов. Здесь наиболее распространены серые лесные почвы. Во всех звеньях биогеохимической пищевой цепи отмечается умеренный недостаток йода, кобальта, цинка, меди, молибдена, бора, марганца и фтора, благоприятное соотношение микроэлементов к йоду и кремнию. В ПКЦ субрегионе сдвиги в гормональном, иммунном и микробном статусах выявляются у 50% практически здоровых людей. В целом по приоритетности биогеохимических параметров ПКЦ субрегион рассматривается как цинкдефицитный с регулируемым дисбалансом микроэлементов в пищевой цепи на фоне низкого содержания йода и фтора.
2. Приволжский (ПВ) субрегион занимает 1/3 территории республики в северной ее части, простирается от западной до восточной ее границы вдоль правого берега Волги. Для растительного покрова здесь характерно чередование участков широколиственного леса с островками луговой степи и сельскохозяйственных земель, наиболее распространены дерново-подзолистые почвы. Во всех звеньях биогеохимической пищевой цепи в условиях ПВ субрегиона отмечается недостаток йода, кобальта, цинка, молибдена, умеренный избыток кремния и нарушенное соотношение микроэлементов к йоду и кремнию. Кроме того на данной территории выше антропогенная нагрузка на природную среду за счет урбанизации и большого числа стационарных и подвижных источников загрязнения. В ПВ субрегионе сдвиги в гормональном, иммунном и микробном статусах выявляются более чем у 75% практически здоровых жителей. ПВ субрегион – цинк- и йоддефицитный с высокой антропогенной загрязненностью и дефицитно-дисбалансно-регулируемым соотношением элементов.
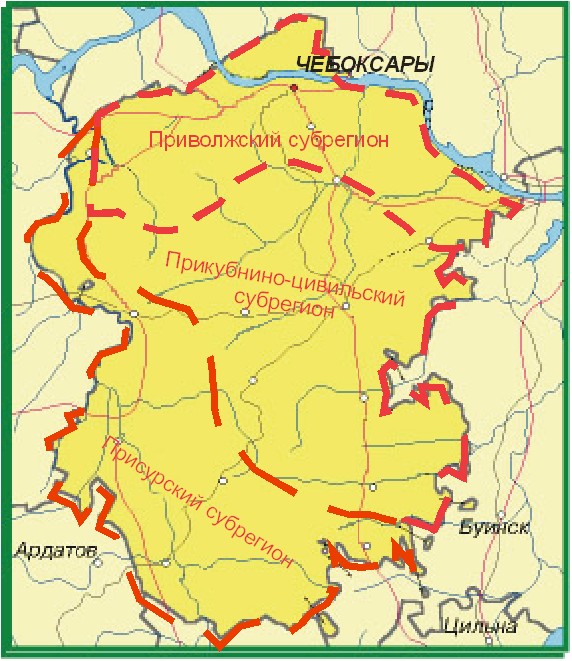
Рис. 1. Карта-схема эколого-биогеохимического районирования территории
Чувашской Республики
3. Присурский (ПС) субрегион занимает 1/3 территории республики в южной и западной ее части. Большая часть его площади - лесная с отдельными островками луговых степей и сельскохозяйственных земель. Леса преимущественно хвойные, наиболее распространены песчано-подзолистые почвы с участками торфяно-болотистых и черноземных. Наличие в ПС субрегионе открытых месторождений кремния в значительной степени отражается на циклах биогенной миграции микроэлементов, которые здесь носят специфический кремниевый характер. Во всех звеньях биогеохимической пищевой цепи в ПС субрегионе отмечается резкий избыток кремния, кальция, фтора и марганца, относительно высокое содержание цинка, меди и стронция и выраженный дефицит йода и кобальта, а также самые высокие доли токсичных элементов – свинца, кадмия и алюминия, неблагоприятное соотношение микроэлементов к йоду и кремнию. Сдвиги в гормональном, иммунном и микробном статусах выявляются у 85-95% практически здоровых жителей. ПС субрегион – высокоминерализованный, аномальный с повышенным содержанием большинства эссенциальных и токсичных элементов.
На 3-м этапе исследования оценены демографическая ситуация в ЧР, проведен статистический анализ общей, первичной и диспансерной заболеваемости у детей и подростков ЧР за 7 лет, особенностей заболеваемости детей на территориях различного эколого-биогеохимического риска, инвалидности детей. Источниками информации явились формы статистической отчётности: №№12, 19, 31
На 4-м этапе проведен анализ структуры нефрологической заболеваемости по обращаемости у сельских и городских детей на основе изучения паспортов врачебных участков городов и районов ЧР (31 паспорт с общим количеством 245000 детей, форма № 030/у-пед.).
Для определения доли больных с нефропатиями в структуре госпитализированной заболеваемости была проведена выкопировка данных из 5137 историй болезни детей 0-17 лет, получивших стационарное лечение в РДКБ, отделениях патологии новорожденных, отделениях детей раннего возраста и соматических отделениях детских городских больниц №1, 3 г. Чебоксары. Изучение структуры госпитализированной нефрологической заболеваемости у детей на территориях различного эколого-биогеохимического риска проводилось при анализе историй болезни 5123 детей (форма 003/у), госпитализированных в РДКБ Минздрасоцразвития Чувашии в 2002 -2008 гг.
Изучение особенностей ХБП у детей ЧР проведено на основе анализа медицинской документации 625 детей в возрасте от 3 месяцев до 17 лет, находящихся на диспансерном учете в связи с заболеваниями ОМС и проживающих в сельских районах и городах ЧР. Всем детям производился расчет СКФ по формуле Шварца:
СКФ (мл/мин/1,73 м2) = 0,0484 х рост (см)/ креатинин сыворотки крови (ммоль/л), для мальчиков 13 лет и старше коэффициент 0,0616.
Стадии ХБП классифицировали по уровню СКФ: 1-я стадия - 90 мл/мин/1,73 м2 и более, 2-я - 89-60 мл/мин/1,73 м2, 3-я - 59-30 мл/мин/1,73 м2, 4-я - 29-15 мл/мин/1,73 м2, 5-я - 15 мл/мин/1,73 м2 и менее.
Анализ структуры инвалидности детей с патологией ОМС, включая аномалии развития и онкологические заболевания, проведен на основе изучения историй болезни и формы №19 «Сведения о детях-инвалидах» за 3 года (2006-2008 гг.).
На 5-м этапе проводилось массовое ультразвуковое исследование почек у детей 0-17 лет методом сплошной выборки в 14 административно-территориальных районах различных эколого-биогеохимических субрегионов ЧР на аппаратах фирмы Алока (Япония). Всего обследовано 8333 ребенка.
Обследование проводилось по стандартной методике с оценкой размеров и структуры органов мочевыделительной системы с внесением полученных данных в разработанный нами протокол (Дворяковский И.В., 2008; Гендлин Г.Е. с соавт., 2009, Ольхова Е.Б., 2006). При постановке диагноза ВПР и МАР почек мы придерживались общепринятых ультразвуковых критериев (Пыков М.И., 2001; Дворяковский И.В., 2009).
Определена популяционная частота и структура ВПР у детей ЧР, оценены базовые частоты для ряда нозологических форм. Популяционная частота ВПР и частоты отдельных форм пороков рассчитаны как отношение детей с ВПР к общему числу обследованных детей и умноженное на 1000 (‰).
В целях разработки нормативов ультразвуковых размеров почек в зависимости от пола, возраста, роста и массы тела определялись размеры почек у 6662 детей в возрасте от первых суток жизни до 18 лет, не имевших заболеваний почек в анамнезе и по данным УЗИ аномалий развития ОМС.
Элементный гомеостаз исследован у 60 детей (29 здоровых детей - группа контроля, 31 ребенок с ВПР почек). Был проведен анализ волос на содержание 25 химических элементов, у 20 детей с ВПР почек повторно через 5 лет определено содержание тех же химических элементов, а также исследовано содержание 12 химических элементов в суточной моче. Анализ осуществлялся в лаборатории АНО «Центр биотической медицины» (Москва), аккредитованной при Федеральном центре Госсанэпиднадзора при Минздравсоцразвитии России, на приборах Optima 2000 DV (Perkin-Elmer, США) и ELAN 9000 (Perkin-Elmer, США) по стандартной методике атомно-эмиссионной и масс-спектрометрии в соответствии с методическими указаниями МУК 4.1.1482-03, 4.1.1483-03 (Иванов С.И. с соавт., 2003). Показатели элементограмм пациентов сравнивались с референтными значениями (Bertram H.P., 1992) и со средними значениями содержания данных химических элементов в волосах (межквартильный интервал), полученными при проведении популяционных исследований в различных регионах РФ (Скальный А.В., 2003).
6 этап. Изучены особенности проявления и течения пиелонефрита (ПиН) у детей в 3 эколого-биогеохимических субрегионах на основе ретроспективного анализа 923 историй болезни сельских детей, госпитализированных в нефрологическое отделение РДКБ Минздравсоцразвития Чувашии за 7 лет. Дети проживали на перечисленных территориях с антенатального периода вплоть до момента госпитализации. Диагноз ПиН основывался на клинико-лабораторных данных с учетом медико-биологического и генеалогического анамнеза, преморбидного фона. Всем детям проводились клинические анализы крови и мочи, исследование концентрационной функции почек в пробе по Зимницкому, определение мочевины, креатинина, микробиологическое исследование мочи из средней порции свободно выпущенной струи общепринятыми методами. Состояние почек и мочевыводящих путей оценивали по данным ультразвукового исследования, экскреторной урографии, микционной цистографии, цистоскопии, компьютерной томографии. Диагноз ПиН у детей был верифицирован в соответствии с классификацией, предложенной Студеникиным М.Я. и др. (1980 г.) и основывался на данных анамнеза, клинической картине заболевания и результатах лабораторно-инструментальных методов исследования.
На 7-м этапе проведено изучение качества диспансеризации детей с хроническим ПиН в условиях городских и сельских педиатрических участков и качество медицинского обслуживания детей с ПиН в специализированных нефрологическом и урологическом отделениях. Непосредственно экспертиза осуществлялась путем сравнения полученных данных, внесенных в специально разработанную анкету, с утвержденными стандартами и рекомендациями. Выкопировка сведений для изучения эффективности диспансеризации детей с хроническим ПиН проводилась из «Истории развития ребенка» (форма № 112/у). Для объективизации исследования для каждого пункта анкет были разработаны критерии, оцениваемые в баллах. Анализ качества оказания медицинской помощи детям с хроническим ПиН в нефрологическом (РДКБ) и урологическом отделениях (МУЗ ГДБ №3) проводился по историям болезни 540 детей, госпитализированных в эти отделения в 2005-2008 гг.
На 8-м этапе выполнен клинико-организационный эксперимент по восстановительному лечению детей с ПиН. В основную группу вошли 54 ребенка 5-10 лет (17 мальчиков и 37 девочек), страдающие хроническим ПиН и проживающие в ПВ субрегионе, группу сравнения составили 42 ребенка (15 мальчиков и 27 девочек) с хроническим ПиН того же возраста и проживающие в том же субрегионе, в реабилитации которых использовались только медикаментозные средства.
Проведено сравнение групп по возрасту, полу, факторам риска формирования заболевания, особенностям течения ПиН и преморбидному фону. Эффективность курса реабилитации в условиях детского восстановительного Центра изучена по данным медицинской документации («История развития ребенка» форма 112/у). Длительность наблюдения в катамнезе составила 1 год с момента окончания лечения в восстановительном Центре.
Проанализирована сеть ЛПУ ЧР, оказывающих первичную медико-санитарную и специализированную помощь детям, коечный фонд, кадровый потенциал, возможности санаторно-восстановительного лечения.
На основании результатов комплексного клинико-организационного исследования разработаны рекомендации по оптимизации уронефрологической службы в ЧР.
Для статистической обработки данных использовались методы параметрического и непараметрического анализа, регрессионный анализ, вычислялись интенсивные и экстенсивные показатели. Были применены следующие критерии параметрической и непараметрической статистики: средняя арифметическая и ее стандартная ошибка, средняя арифметическая и ее стандартное отклонение, медиана и квартили, для относительных величин определили долю (р,%) и ее ошибку (mp). Различия дискретных признаков, представленных в виде частоты события (% больных к общему числу наблюдений), оценивали с помощью критерия z с поправкой Йейтса на непрерывность. При малом объекте выборки или неправильности распределения согласно рекомендациям Е.В. Гублера использовали непараметрический критерий Манна-Уитни (рМ-U).
Анализ динамики изучаемых признаков проводился на основе частот их проявлений в исследуемых группах в виде вычисления частоты признаков в % с их ошибками (р ± m) с последующей проверкой статистической достоверности различий значений с помощью критерия t Стьюдента. Широко использовалось графическое изображение статистических величин с помощью структурных, динамических и сравнительных диаграмм. Результаты сравнения рассматривали как статистически значимые при р < 0,05 (Зайцев В.М., 2006; Kirkwood B., 2003).
Статистическая обработка полученных данных проводилась в операционной среде Windows ХР с использованием лицензионной программы «STATISTICА 6.0» (Плавинский С.Л., 2005).
Результаты исследования и их обсуждение. В связи с тем, что в последние годы в ЧР значительно улучшились основные демографические показатели, возникла необходимость переоценки приоритетов в развитии здравоохранения с переносом максимального внимания на повышение качества жизни больных с различными заболеваниями, в том числе и нефрологическими. Это связано также с неуклонным возрастанием за последние годы среди патологии детского возраста болезней почек, мочевыделительной системы и их врожденных аномалий.
Изучение заболеваемости детского населения ЧР выявило, что за 7 лет произошел рост общей заболеваемости детей 0-17 лет в 1,7 раза и в 2008 г. ее уровень достиг 2950,4‰, при этом первичная заболеваемость выросла в 1,6 раза, диспансерная группа – в 1,2 раза (табл. 2). Наиболее интенсивно показатели заболеваемости увеличились у детей 15-17 лет - в 2,2 раза, тогда как у детей 0-1 года и 0-14 лет - в 1,5 раза при самом высоком уровне заболеваемости у детей первого года жизни, достигшем в 2008 г. 3605,3‰.
Таблица 2
Общая, первичная, диспансерная заболеваемость детей ЧР в 2002-2008 гг.
(на 1000 детей)
| Год | Возраст, лет | |||||||||
| до 1 г. | 0-14 | 15-17 | 0-17 | 0-14 | 15-17 | 0-17 | 0-14 | 15-17 | 0-17 | |
| 2002 | 2394,9 | 1964,4 | 1334,2 | 1768,6 | 1406,9 | 729,7 | 1196,5 | 371,9 | 376,3 | 387,1 |
| 2003 | 2355,8 | 1792,9 | 2047,4 | 1855,1 | 1257,4 | 1125,7 | 1225,2 | 348,5 | 516,8 | 389,6 |
| 2004 | 3409,5 | 1959,5 | 2106,9 | 1997,4 | 1412,5 | 1137,9 | 1341,8 | 358,2 | 528,6 | 402,0 |
| 2005 | 3022,9 | 2235,7 | 2259,0 | 2241,7 | 1571,9 | 1204,7 | 1476,9 | 384,7 | 539,4 | 424,7 |
| 2006 | 3333,9 | 2669,5 | 2500,6 | 2552,0 | 1782,6 | 1368,0 | 1677,4 | 411,2 | 549,7 | 446,3 |
| 2007 | 3026,3 | 2876,8 | 2773,2 | 2813,2 | 2072,1 | 1590,0 | 1954,8 | 418,2 | 556,0 | 452,1 |
| 2008 | 3605,3 | 2971,9 | 2876,6 | 2950,4 | 2115,5 | 1598,5 | 1954,0 | 419,6 | 555,3 | 454,9 |
У детей 0-17 лет высокие темпы роста заболеваемости отмечались по 12 классам болезней, среди которых новообразования, отдельные состояния, возникающие в перинатальном периоде (в 2,8 раза), ВПР, деформации и хромосомные нарушения (в 2,5 раза), заболевания нервной системы (в 2,1 раза), болезни МПС (в 1,9 раза), костно-мышечной системы (в 1,9 раза), уха и сосцевидного отростка (в 1,8 раза), органов дыхания (в 1,7 раза), органов пищеварения (в 1,6 раза), кожи и подкожной клетчатки (в 1,6 раза), травмы и отравления (в 1,6 раза), болезни глаз и придаточного аппарата (в 1,5 раза). Среди детей 0-14 лет наиболее интенсивный рост заболеваемости отмечался по 10 классам, как-то: новообразования (в 2,8 раза), ВПР (в 2,6 раза), заболевания крови и кроветворных органов (в 1,8 раза), нервной системы (в 1,8 раза), костно-мышечной системы (в 1,8 раза), органов дыхания (в 1,6 раза), МПС (в 1,6 раза), органов пищеварения (в 1,6 раза), кожи и подкожной клетчатки (в 1,5 раза), травмы и отравления (в 1,4 раза). У подростков 15-17 лет самые высокие темпы роста заболеваемости отмечены по следующим классам: новообразования (в 3,3 раза), болезни уха и сосцевидного отростка (в 3,1 раза), МПС (в 2,6 раза), травмы и отравления (в 2,3 раза), болезни органов кровообращения (в 2,1 раза), костно-мышечной системы (в 2,1 раза), глаза и его придаточного аппарата (в 1,9 раза), органов пищеварения (в 1,9 раза), эндокринной системы (в 1,5 раза), психические расстройства и расстройства поведения (в 1,3 раза). Из полученных данных видно, что болезни МПС выделялись интенсивным ростом как среди детей 0-14 лет, так и среди подростков 15-17 лет.
Изучение особенностей заболеваемости детей и подростков в различных эколого-биогеохимических субрегионах выявило следующее. Наиболее высоким уровень заболеваемости был в ПС субрегионе у детей 0-14 лет, где темпы его прироста составили 17% за 3 года. У подростков 15-17 лет наблюдался одинаковый прирост общей заболеваемости во всех изучаемых субрегионах (в 1,2 раза) без достоверных различий в ее уровне.
Во всех возрастных группах детей имелись статистически значимые различия в уровнях заболеваемости по отдельным классам болезней в зависимости от эколого-биогеохимических характеристик территории их проживания. У детей 0-14 лет в ПС субрегионе наблюдались наиболее высокие показатели инфекционной патологии, новообразований, психических расстройств, болезней органов пищеварения, кожи и подкожной клетчатки, костно-мышечной системы, травм и отравлений (р < 0,05). Перечисленная патология имела сильную прямую корреляционную связь (r = от +0,78 до +0,99) с частотой отклонений от ГОСТа проб воды, почвы и воздуха, повышенным содержанием цинка, марганца, фтора, хрома и бериллия в водно-пищевых рационах детей и подростков. В ПКЦ субрегионе чаще встречались болезни эндокринной и нервной системы, крови и кроветворных органов, системы кровообращения, уха и сосцевидного отростка, МПС, отдельные состояния, возникающие в перинатальном периоде (р < 0,05), в ПВ – болезни органов дыхания и врожденные аномалии (р < 0,05). По нашим данным, указанные состояния имели среднюю и сильную прямую коррелятивную связь с частотой дефицита в водно-пищевых рационах цинка (r = + 0,79), кальция (r = + 0,89), меди (r = + 0,98) и калия (r = + 0,84) и среднюю обратную коррелятивную связь с частотой отклонений от ГОСТа проб воды, почвы и воздуха (r от - 0,58 до – 0,66). У подростков 15-17 лет в ПКЦ субрегионе достоверно чаще выявлялись эндокринные болезни, болезни нервной системы, системы кровообращения, МПС (р < 0,05), но здесь был ниже уровень болезней органов дыхания, инфекционных и паразитарных заболеваний, травм и отравлений. В ПВ субрегионе отмечена более высокая распространенность болезней уха и сосцевидного отростка (р < 0,05), в ПС регионе - психических расстройств, травм и отравлений, состояний, связанных с беременностью и родами, здесь же чаще диагностировались инфекционные и паразитарные заболевания, а также новообразования (р < 0,05). Высокие показатели по классам психических расстройств, травм и отравлений, состояний, связанных с беременностью и родами требуют дальнейшего изучения сложившейся ситуации и проведения дополнительных научных исследований для выявления более глубоких причин (социальных, экономических и др.) этого феномена.
В ПКЦ субрегионе у детей с возрастом наиболее значительно повышалась распространенность болезней системы кровообращения (в 3,2 раза), МПС и психических расстройств (в 3 раза), костно-мышечной системы (в 2,8 раза), глаза и придаточного аппарата (в 2 раза), органов пищеварения (в 1,9 раза). У подростков в ПВ субрегионе по сравнению с детьми 0-14 лет выявлен более интенсивный рост болезней уха и сосцевидного отростка (в 3 раза), психических расстройств (в 2,9 раза), болезней МПС (в 2,7 раза), новообразований (в 2,3 раза), болезней глаза и придаточного аппарата (в 2 раза) и системы кровообращения (в 1,9 раза) (р < 0,05). В ПС субрегионе также имелись определенные региональные особенности формирования заболеваемости у детей подростковой группы. Здесь наиболее высокие темпы роста отмечались по классу болезней системы кровообращения (в 3,5 раза), хотя по сравнению с другими субрегионами заболеваемость сердечно-сосудистой патологией была самой низкой. В ПС субрегионе высокими темпами нарастала патология МПС (в 2,1 раза), болезни глаза и придаточного аппарата (в 1,7 раза), психические расстройства и болезни эндокринной системы (в 1,5 раза). В отличие от других в ПС субрегионе с возрастом снизилась распространенность болезней уха и сосцевидного отростка, кожи и подкожной клетчатки и более интенсивно – инфекционных и паразитарных заболеваний (р < 0,05).
Как видно из представленных данных, структура заболеваемости в перечисленных субрегионах имела значительные различия как у детей 0-14, так и подростков 15-17 лет. Сформировавшаяся у детей 0-14 лет структура заболеваемости претерпевала незначительные изменения в подростковом возрасте. Следовательно, эколого-биогеохимические особенности, в том числе микроэлементные, территории проживания, могут способствовать формированию той или иной патологии с первых лет жизни.
Выявленные нами особенности приоритетности определенной патологии в изучаемых субрегионах важны, прежде всего, с точки зрения организации профилактической работы врачей-педиатров на территориях различного эколого-биогеохимического риска.
Распространенность инвалидности среди детей 0-17 лет имела незначительные колебания по годам с минимальными показателями в 2002 г. (179,0‰0) и максимальными в 2006 г. (206,5‰0). Максимальный выход на первичную инвалидность отмечался среди детей 0-4 лет, минимальный – 15-17 лет. Среди детей–инвалидов во всех возрастных группах преобладали мальчики.
В ЧР детская инвалидность обусловлена пятью основными классами заболеваний, которые в ранговом порядке распределились следующим образом: психические заболевания, врожденная патология, болезни нервной системы, болезни уха, болезни глаза. Хотя в целом уровень детской инвалидности в ЧР соответствовал таковому по РФ, доля соматической патологии в нем крайне низка (рис. 2). Однако низкий уровень детской инвалидности, обусловленной соматической патологией, в том числе и нефрологической, не является показателем хорошего состояния здоровья детей ЧР, а скорее всего, связан с недовыявлением детей-инвалидов. Об этом свидетельствует высокий уровень заболеваемости детей всех возрастных групп.
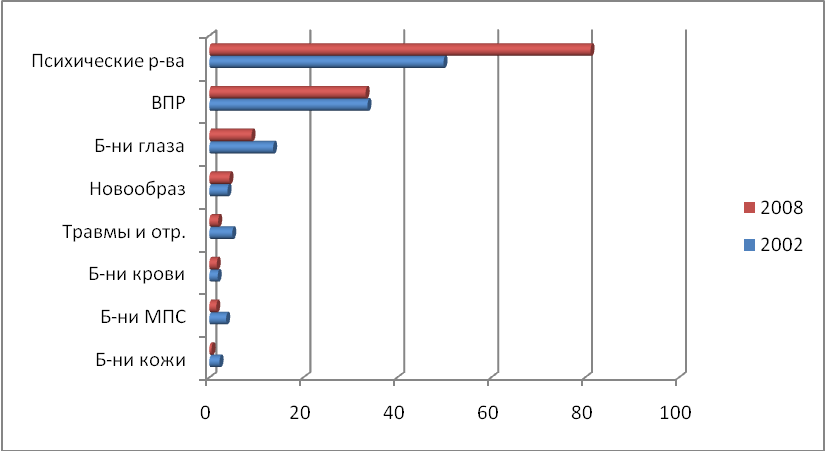
Рис. 2. Распределение детей 0-17 лет по основному заболеванию, приведшему к инвалидности (на 10 000 детей)
Рост болезней МПС за изучаемый период составил 80,0% и их уровень достиг в 2008 г. 119,0‰ (табл. 3).
Таблица 3
Распространенность болезней МПС у детей 0-17 лет в ЧР
в 2002-2008 гг. (на 1000)
| Заболеваемость | 2002 | 2003 | 2004 | 2005 | 2006 | 2007 | 2008 |
| Общая | 66,1 | 72,5 | 78,1 | 87,8 | 109,6 | 112,3 | 119,0 |
| Первичная | 30,9 | 32,2 | 35,0 | 44,5 | 56,2 | 59,6 | 46,8 |
| Диспансерная | 33,1 | 34,4 | 35,5 | 35,5 | 37,5 | 38,6 | 49,3 |
Доля нефрологической патологии в структуре болезней МПС колебалась по годам от 56,1 до 59,3%. Уровень общей заболеваемости у детей 0-14 лет вырос за изучаемый период в 1,6 раза (до 99,5‰), при этом отмечался опережающий рост первичной заболеваемости как в целом по классу МПС (в 1,8 раза), так и доли нефрологической патологии (в 1,6 раза) при стабильной численности группы диспансерного наблюдения. Среди заболеваний отмечался двукратный рост почечной недостаточности и в 1,8 раза - мочекаменной болезни. У детей 15-17 лет распространенность болезней МПС выросла в 2,6 раза (до 186,0‰), при этом нефрологической патологии - на 103,5%. Уровень первичной заболеваемости по классу МПС у них увеличился в 2,8, диспансерной группы – в 1,8 раза. Аналогичная картина наблюдалась при анализе нефрологической заболеваемости: более быстрыми темпами росла первичная патология (в 2,2 раза) по сравнению с диспансерной группой (в 1,8 раза). Таким образом, среди детей 15-17 лет за изучаемый период выявлен высокий рост распространенности болезней МПС и нефрологической патологии. Распространенность уронефрологической заболеваемости у детей ЧР зависит от эколого-биогеохимических особенностей территории проживания и наиболее высока в ПКЦ субрегионе - цинк- и кремний-дефицитной провинции с дисбалансом микроэлементов в пищевой цепи, где она увеличилась у детей 0-14 лет до 72,4, 15-17 лет – до 214,6‰.
Заболеваемость болезнями МПС у детей первого года жизни за 7 лет выросла в 2 раза и достигла в 2008 г. 125,0‰ (рис. 3). В ее структуре преобладала нефрологическая патология, что свидетельствует о значительной распространенности патологии ОМС в детской популяции начиная с самого раннего возраста.
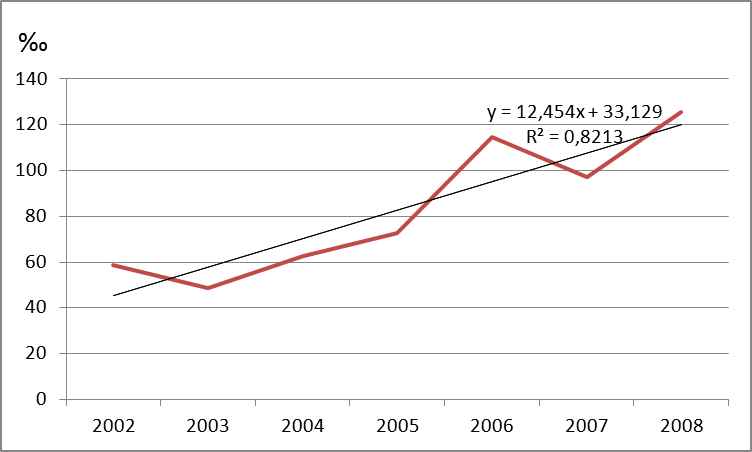
Рис. 3. Заболеваемость болезнями МПС детей первого года жизни
в ЧР в 2002-2008 годах, в ‰
По данным официальной статистики, доля болезней МПС в структуре госпитализированной заболеваемости в ЧР снизилась за 6 лет с 6,3 до 5,1%. Однако нами установлено, что с учетом сопутствующей патологии количество пациентов с нефропатиями в стационаре колеблется от 21,8% (в соматическом отделении) до 42,8% (в отделении раннего возраста). Во всех возрастных группах детей с болезнями ОМС по численности преобладали девочки. Городские дети почти в 2 раза чаще госпитализировались с ИМС, ВПР мочевой системы как основной диагноз у них отмечались в 9 раз реже; у сельских детей достоверно чаще диагностировалась дисметаболическая нефропатия, у городских – ТИН. ХПН, нейрогенная дисфункция мочевого пузыря и энурез преобладали у детей из села. В структуре госпитализированной нефрологической заболеваемости, как у сельских, так и городских детей, лидировали уронефропатии. В связи с этим мы считаем, что в современных условиях в детских стационарах более рациональна организация отделений сочетанного профиля - уронефрологических с наличием в штате врачей нефрологов и урологов.
У детей из ПКЦ субрегиона чаще диагностировались ИМС и ПиН, у них реже выявлялись ТИН, дисметаболическая нефропатия и гематурия неясного генеза, чем в остальных субрегионах. Из ПВ субрегиона дети чаще госпитализировались с ВПР ОМС и энурезом, а ПС регион отличался большей долей дисметаболических нефропатий, ТИН, наследственного нефрита, микрогематурии неясного генеза и почечной недостаточности. Следовательно, госпитализированная нефрологическая заболеваемость детей также зависела от эколого-биогеохимических особенностей территории их проживания.
При проведении корреляционного анализа установлено, что частота госпитализированных ИМС и ПиН имела среднюю обратную коррелятивную связь с уровнем цинка (r = - 0,60), кальция (r = - 0,64), железа (r = - 0,57), марганца (r = - 0,67), калия (r = - 0,63), сильную - меди (r = - 0,98), кремния (r = - 0,59), кадмия (r = - 0,76) и алюминия (r = - 0,81) в водно-пищевых рационах детей. В то же время уровень госпитализированной дисметаболической нефропатии имел прямую сильную коррелятивную связь с вышеуказанными макро-микроэлементами (r = от +0,88 до +0,99) и среднюю - с содержанием фосфора (r =+ 0,65) в водно-пищевых рационах. При этой патологии также установлена высокая прямая корреляция с качеством воды, почвы и проб воздуха, а также долей здоровых людей с дисбалансом уровня элементов в крови. Доля почечной недостаточности среди госпитализированных детей с нефрологической патологией наиболее тесно коррелировала с состоянием водных источников (r = + 0,97), нарушением элементного гомеостаза (r = + 0,69), повышенным содержанием в водно-пищевых рационах детей цинка (r = + 0,98), марганца (r = + 0,98), фтора (r = + 0,98), хрома (r = + 0,98) и кремния (r = + 0,99).
Таким образом, анализ госпитализированной патологии ОМС показал, что ее структура зависит от территории проживания детей, ее эколого-биогеохимических характеристик. Иммунная недостаточность на фоне дефицита цинка и йода в водно-пищевых рационах в ПКЦ субрегионе способствовала более частому развитию микробно-воспалительных процессов ОМС. Повышенная антропогенная нагрузка ПВ субрегиона реализовалась в преобладании ВПР ОМС, нарастании дисметаболических нарушений, микрогематурии. ПС субрегион с выраженным дисбалансом макро-микроэлементов, наличием повышенного уровня кремния и тяжелых металлов в почвах и воде способствовал еще более частому проявлению дисметаболических нарушений и их реализации в ТИН, высокую частоту микрогематурий неясного генеза (возможно, также как проявление нарушенного обмена веществ), большую долю почечной недостаточности.
При анализе структуры, возрастных и гендерных особенностей ХБП у детей установлено, что 1-ю стадию имели 52,2% детей, 2-ю стадию – 36,8, 3-ю стадию – 10,2, 4-ю стадию – 0,64, 5-ю стадию – 0,32% детей с нефропатиями (рис. 4).
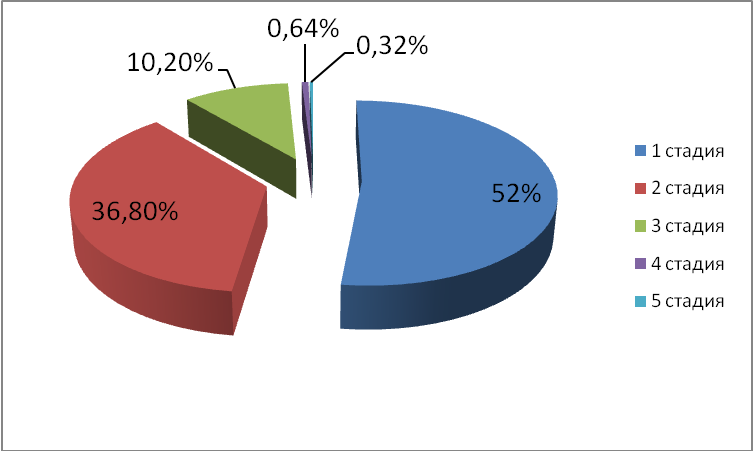
Рис. 4. Распределение детей с ХБП по стадиям, %
Структура ХБП в ЧР была представлена преимущественно врожденной патологией, среди которой ведущее место занимали обструктивные уропатии и АМС (табл. 4).
Гидронефрозы и уретерогидронефрозы составляли 1/3 часть от всей патологии, АМС - 1/4, 15,2% приходилось на единственную почку, 9,9% - на гломерулонефриты. Остальная патология (поликистоз, дисплазии почек, ТИН, наследственный нефрит и др.) составили от 2,0 до 3,7% от нозологий, формирующих ХПБ.
Таблица 4
Структура ХБП у детей ЧР, абс (%)
| Патология | Мальчики (n = 315) | Девочки (n = 310) | Всего (n = 625) |
| Обструктивная уропатия | 127 (40,4) | 80 (25,8) | 207 (33,1) |
| АМС | 55 (17,5) | 106 (34,2) | 161 (25,8) |
| Единственная почка | 53 (16,9) | 42 (13,5) | 95 (15,2) |
| Поликистоз | 7 (2,2) | 8 (2,6) | 15 (2,4) |
| Дисплазия почек | 9 (2,7) | 5 (1,6) | 14 (2,2) |
| Гломерулонефрит | 36 (11,4) | 26 (8,4) | 62 (9,9) |
| ТИН | 7 (2,2) | 9 (2,9) | 16 (2,6) |
| Наследственный нефрит | 6 (1,9) | 17 (5,5) | 23 (3,7) |
| Прочие | 15 (4,8) | 17 (5,5) | 32 (5,1) |
Количество девочек и мальчиков с ХБП было практически одинаковым, за исключением первого года жизни, где было достоверно больше мальчиков, половина пациентов имели возраст до 10 лет. У 53,6% детей с ХБП отмечался вторичный хронический ПиН, среди девочек это осложнение встречалось достоверно чаще, чем среди мальчиков. Наслоение микробно-воспалительного процесса у детей с обструктивными уропатиями, как правило, приводило к ухудшению фильтрационной функции почек (в среднем на 11,33 мл/мин/1,73 м2).
Доля детей, подвергшихся оперативным вмешательствам на органах ОМС, составила 28,6% от всей группы пациентов с ХБП.
Среди когорты детей с ХБП различные стадии ХПН имели 11,2% обследованных. Среди пациентов с ХПН преобладали дети младшего возраста, по количеству мальчики и девочки не различались. В структуре ХПН более половины всех патологических состояний занимали обструктивные уропатии (51,4%), на 2-м месте находились АМС, на 3-м - единственная почка в связи с оперативным удалением контрлатерального органа (табл. 5). С учетом других состояний (поликистоз, дисплазия, врожденный нефротический синдром) подавляющее большинство больных с ХПН имели врожденную патологию почек (94,3%) и только у 5,7% детей почечная недостаточность была связана с приобретенными нефропатиями. Наиболее угрожаемую группу по развитию ХПН представляли дети с единственной почкой. Особую тревогу вызывало то, что 65,7% детей с ХПН были младшего возраста и у них возникали большие трудности как при проведении нефропротективной, так и почечной заместительной терапии.
Таблица 5
Причины ХПН у детей и подростков ЧР
| Патология | Частота, абс (%) |
| Обструктивная уропатия | 36 (51,4) |
| Врожденные пороки развития ОМС, в том числе агенезия почки | 12 (17,1) |
| Нефрэктомия | 9 (12,9) |
| Дисплазия почек | 5 (7,1) |
| Хронический гломерулонефрит, ТИН | 3 (4,3) |
| Врожденный нефротический синдром | 2 (2,9) |
| Поликистоз | 1 (1,4) |
| Прочие (тубулопатия, диабетическая нефропатия) | 2 (2,9) |
| Всего | 70 (100) |
Исследование показало, что применение расчетной СКФ дает возможность у детей с уронефрологической патологией даже в амбулаторных условиях выделять различные стадии ХБП, что необходимо для своевременного проведения нефропротективной терапии и ранней диагностики ХПН.
Инвалидность, обусловленная болезнями МПС, снизилась в ЧР с 3,6 в 2002 г. до 1,5 на 10000 детского населения в 2008 г., ее показатели были в 2,5 раза ниже, чем в РФ. Доля заболеваний МПС у детей составляла 7,6% от соматической патологии, но с учетом пороков развития ОМС поражение органов МПС как причина инвалидизации детей наблюдалась с большей частотой. Среди детей-инвалидов с патологией ОМС достоверно больше мальчиков (58,6%), более половины (61,1%) - дети первых 9 лет жизни. Среди детей-инвалидов с поражением ОМС преобладали пациенты с ВПР, их доля составила 74,8% всей структуры уронефрологической инвалидности. Нефрологическая патология в структуре инвалидности была равна 25,5%. Большая часть нефрологической инвалидности у детей представлена врожденной патологией (78,7%). В группе детей-инвалидов с патологией ОМС 16,6% детей имели единственную почку, как правило, порочно заложенную или осложненную хроническим ПиН, 41,4% - подверглись оперативным вмешательствам по поводу ПМР, гидронефроза или других состояний. Анализ инвалидности, обусловленной патологией ОМС, ярко свидетельствует о сложности реабилитации данного контингента детей, о высоком риске формирования ХПН с потребностью в заместительной терапии или пересадке почки.
В связи с отсутствием современных ультразвуковых нормативов размеров почек, полученных на большом массиве исследований, нами проведена морфометрия почек 6662 здоровых детей с корреляционным анализом между линейными размерами и возрастом, ростом, массой тела и полом ребенка и составлением оценочных таблиц. Доказано, что в практической деятельности врача ультразвуковой диагностики при измерении линейных параметров почек у детей достаточно использовать объединенную таблицу размеров почек в зависимости от роста или возраста без разделения по полу (табл. 6).
Таблица 6
Ультразвуковые размеры почек (мм) в зависимости от роста детей, M ± 2
| Рост, см | n | Левая почка | Правая почка | ||||
| длина | ширина | толщина | длина | ширина | толщина | ||
| 45-49 | 61 | 46,8 ± 18,6 | 21,2 ± 7,8 | 19,9 ± 10,8 | 46,5 ± 14,6 | 20,3 ± 9,2 | 20,3 ± 6,2 |
| 50-59 | 842 | 50,2 ± 14,2 | 21,3 ± 6,8 | 21,5 ± 6,6 | 49,5 ± 13,2 | 21,8 ± 3,9 | 22,1 ± 3,2 |
| 60-69 | 443 | 58,3 ± 13,6 | 23,9 ± 7,0 | 24,3 ± 6,6 | 56,8 ± 12,4 | 24,6 ± 7,0 | 24,3 ± 5,8 |
| 70-79 | 264 | 64,3 ± 13,8 | 25,9 ± 7,4 | 26,6 ± 5,6 | 63,1 ± 12,6 | 26,1 ± 6,8 | 25,7 ± 6,0 |
| 80-89 | 289 | 69,4 ± 15,4 | 27,6 ± 8,6 | 27,9 ± 9,0 | 68,3 ± 13,2 | 28,2 ± 7,6 | 26,8 ± 6,6 |
| 90-99 | 292 | 73,7 ± 13,4 | 29,2 ± 7,8 | 28,7 ± 6,4 | 73,2± 12,0 | 29,7 ± 7,4 | 27,8 ± 6,0 |
| 100-109 | 314 | 78,4 ± 13,8 | 30,5 ± 9,2 | 30,3 ± 6,4 | 77,1 ± 13,8 | 31,2 ± 7,6 | 28,3 ± 6,4 |
| 110-119 | 413 | 82,3 ± 14,4 | 32,3 ± 9,0 | 32,1 ± 6,6 | 80,8 ± 15,0 | 32,7 ± 8,0 | 30,3 ± 6,8 |
| 120-129 | 493 | 85,9 ± 15,6 | 33,9 ± 8,8 | 33,2 ± 7,2 | 84,0 ± 16,2 | 34,5 ± 8,8 | 31,2 ± 7,2 |
| 130-139 | 583 | 90,1 ± 16,0 | 35,6 ± 8,4 | 34,7 ± 7,4 | 88,8 ± 14,4 | 36,3 ± 8,4 | 32,5 ± 7,8 |
| 140-149 | 636 | 94,5 ± 19,8 | 37,6 ± 11,4 | 36,7 ± 10,4 | 93,3 ± 17,0 | 37,9 ± 10,2 | 34,1 ± 8,2 |
| 150-159 | 793 | 100,7 ± 16,0 | 40,3 ± 11,6 | 39,2 ± 13,6 | 100,5 ± 17,0 | 41,0 ± 10,4 | 36,7 ± 10,8 |
| 160-169 | 786 | 104,7 ± 18,8 | 41,6 ± 10,8 | 40,4 ± 8,8 | 103,9 ±17,0 | 42,1 ± 11,0 | 37,7 ± 8,8 |
| От 170 | 378 | 110,4 ± 16,8 | 45,3 ± 10,8 | 42,3 ± 13,0 | 108, ± 17,6 | 45,2 ± 12,6 | 39,4 ± 9,6 |
Для установления распространенности врожденных пороков и МАР почек у детей ЧР нами был выбран метод ультразвуковой диагностики с учетом его преимуществ в выявлении морфологических нарушений органов и систем, а также неинвазивности, доступности и экономичности. Массовое ультразвуковое исследование у детей 0-17 лет показало, что суммарная распространенность аномалий развития почек составляет 161,3, ВПР - 48,7, МАР - 132,6, сочетанной патологии (ВПР + МАР) - 9,0, кистозных дисплазий - 2,6 на 1000 детей. Наиболее высокие показатели почечных мальформаций отмечались в ПВ субрегионе – 187,1, низкие – в ПС – 130,4 (р = 0,002), промежуточное место занимал ПКЦ субрегион - 164,8‰ (рис. 5).
По данным нашего исследования ВПР почек у детей ЧР являются распространенной патологией, и популяционная частота многих структурных вариантов пороков почек выше, чем в других регионах.
Нами установлены различия популяционной распространенности ВПР почек в зависимости от эколого-биогеохимических характеристик территории проживания детей. В ПКЦ субрегионе чаще выявлялись гипоплазия, дистопия, была меньше распространенность агенезии, удвоения почек, кистозной дисплазии (р < 0,05), в ПС субрегионе выше распространенность агенезии (р < 0,05), в ПВ субрегионе - удвоения почек, кистозной дисплазии и гидронефроза (р < 0,05). Распространенность некоторых МАР почек (ротаций и их разновидностей, расщепления ЧЛС) нами установлена впервые.
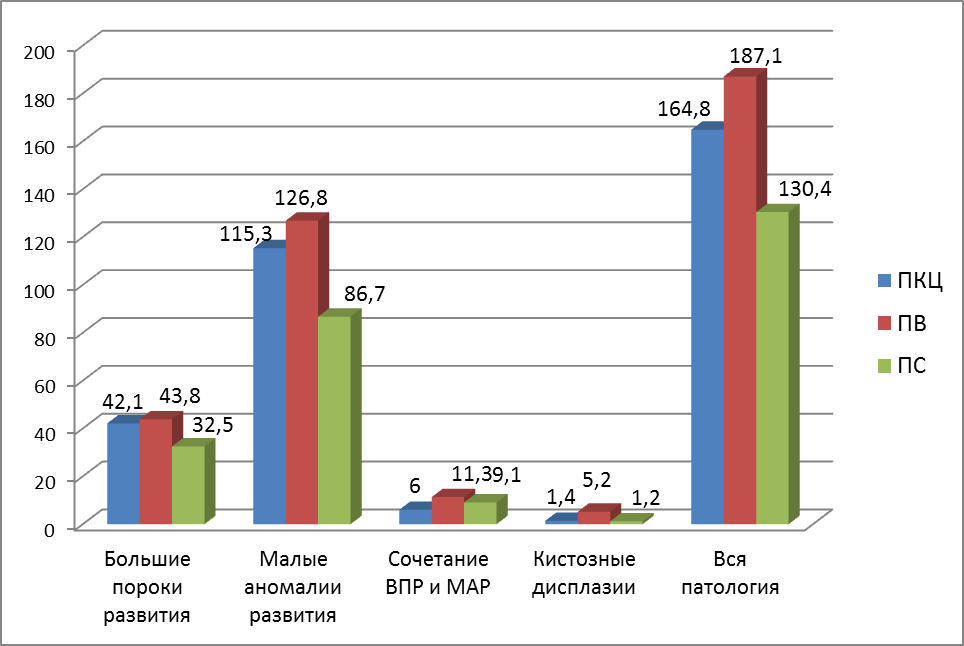
Рис. 5. Распространенность ВПР и МАР почек у детей 0-17 лет в различных эколого-биогеохимических регионах ЧР, ‰
Известно, что патология почек может непосредственно сказываться на элементном статусе организма, и напротив, нарушения минерального обмена могут повлечь за собой развитие патологических процессов в органах мочевой системы. В связи с этим нами исследовано содержание химических элементов в волосах детей в зависимости от наличия у них аномалий развития почек (табл. 7).
Таблица 7
Содержание химических элементов в волосах здоровых детей и детей с пороками почек в Чувашии, мг/кг, Мe (q25-q75)
| Элемент | Все дети (n = 60) | Здоровые (n = 29) | С пороками (n = 31) |
| Al | 11,1 (5,7 - 15,2) | 9,5 (3,1 - 14,4) | 11,5 (7,9 - 20) * |
| As | 0,094 (0,059 - 0,124) | 0,099 (0,046 - 0,117) | 0,093 (0,06 - 0,127) |
| B | 2,12 (1,36 - 2,87) | 1,84 (1,09 - 2,75) | 2,23 (1,45 - 3,19) |
| Be | 0,002 (0,002 - 0,009) | 0,004 (0,002 - 0,012) | 0,002 (0,002 - 0,007) * |
| Са | 527 (424 - 743) | 564 (435 - 749) | 516 (417 - 690) |
| Cd | 0,098 (0,06 - 0,171) | 0,084 (0,049 - 0,113) | 0,124 (0,066 - 0,226) * |
| Со | 0,018 (0,007 - 0,029) | 0,013 (0,005 - 0,029) | 0,022 (0,012 - 0,032) |
| Cr | 0,795 (0,592 - 1,082) | 0,809 (0,606 - 1,115) | 0,793 (0,584 - 1,034) |
| Сu | 9,88 (8,58 - 11,22) | 9,44 (8,22 - 10,69) | 10,19 (8,58 - 11,51) |
| Fe | 25,6 (17 - 33,1) | 24,5 (16,2 - 32,5) | 25,9 (17,5 - 34,6) |
| Hg | 0,193 (0,12 - 0,273) | 0,207 (0,136 - 0,27) | 0,189 (0,119 - 0,275) |
| I | 1,09 (0,55 - 2,65) | 1,31 (0,48 - 3,12) | 1,07 (0,59 - 2,45) |
| K | 345 (106 - 827) | 157 (67 - 697) | 425 (129 - 1140)* |
| Li | 0,063 (0,043 - 0,097) | 0,051 (0,04 - 0,09) | 0,065 (0,046 - 0,098) |
| Mg | 65,6 (43,9 - 113,2) | 75 (45,6 - 125) | 55,4 (39,2 - 100) |
| Mn | 1,56 (0,92 - 2,65) | 1,57 (0,79 - 2,66) | 1,56 (0,97 - 2,63) |
| Na | 682 (339 - 1401) | 484 (193 - 1378) | 779 (368 - 1423) |
| Ni | 0,458 (0,278 - 0,694) | 0,407 (0,254 - 0,62) | 0,524 (0,319 - 1,64) * |
| Р | 149 (127 - 165) | 149 (130 - 165) | 151 (121 - 165) |
| Рb | 2,24 (1,56 - 4,12) | 1,92 (1,33 - 2,64) | 2,27 (1,69 - 5,21) * |
| Se | 0,271 (0,13 - 0,399) | 0,176 (0,113 - 0,353) | 0,291 (0,195 - 0,404) |
| Si | 27,2 (20,2 - 36,5) | 26,2 (21 - 31,8) | 32,2 (17,8 - 42,3) |
| Sn | 0,119 (0,088 - 0,178) | 0,099 (0,067 - 0,136) | 0,148 (0,105 - 0,199) ** |
| V | 0,165 (0,13 - 0,234) | 0,153 (0,127 - 0,24) | 0,17 (0,13 - 0,228) |
| Zn | 175 (141 - 193) | 184 (157 - 206) | 149 (132 - 183) * |
Примечание: Me – медиана, q25 – нижний квартиль, q75 – верхний квартиль;
Достоверность отличия от группы здоровых детей: * - p < 0,05; ** - p < 0,01.
Исследования показали, что одной из характерных особенностей детей с пороками развития почек является относительно повышенное содержание элементов-экотоксикантов из группы тяжелых металлов, к которым принадлежат свинец, кадмий, олово и никель, на фоне высокой частоты встречаемости пониженного уровня цинка и бериллия (p < 0,05). Для гидронефрозов было характерным повышенное содержание хрома и пониженное - магния, аномалии количества почек ассоциировались с высоким содержанием бора и кадмия, а аномалии расположения и взаимоотношения – с низким содержанием бериллия.
По нашему мнению, элементный дисбаланс, сопровождающий тот или иной порок развития почек, даже в отсутствии какого-либо клинически проявляющегося патологического процесса, например, ИМС, является важным маркером минимальных почечных дисфункций.
К подростковому возрасту по мере дозревания почечных, и прежде всего, канальцевых функций, дисбаланс химических элементов в организме детей с ВПР почек значительно уменьшился. Уровень основных элементов-экотоксикантов в волосах большинства детей соответствовал возрастной норме, но сохранялись изменения, характеризующие биогеохимические особенности среды проживания детей, а именно повышенное содержание кремния и низкая концентрация цинка. Однако наличие элементного дисбаланса у растущего ребенка даже на протяжении небольшого периода не может быть безопасным для его развития. Поэтому мы считаем необходимым введение в общепринятую схему диспансеризации детей с пороками почек дополнительных исследований, направленных на изучение их элементного гомеостаза и целенаправленной коррекции его изменений еще на стадии предболезни.
В связи со значительным распространением вторичного хронического ПиН у детей ЧР и его вкладом в прогрессирование врожденных нефропатий, а также возможным влиянием на клинические проявления заболевания эколого-биогеохимических факторов, нами проанализированы особенности течения ПиН у детей в 3 гетерогенных субрегионах.
Большинство госпитализированных детей с ПиН из ПКЦ субрегиона были школьного возраста (57%), заболевание у них дебютировало позднее и реже рецидивировало, чем в соседних областях. Дети имели более благоприятное течение анте,- интра- постнатального периодов, большинство родились здоровыми, среди них меньше доля рожденных недоношенными. Из факторов риска следует отметить более высокий процент часто болеющих и худшие показатели физического развития детей. Почти каждый четвертый ребенок был из семьи, отягощенной по патологии почек. Дети из ПКЦ субрегиона чаще имели синдром интоксикации, но у меньшего числа пациентов были выражены другие проявления заболевания (болевой, дизурический и отечный синдромы). В мочевом синдроме у них чаще выявлялась лейкоцитурия, реже – протеинурия и бактериурия, чем у детей ПВ и ПС субрегионов. В ПКЦ субрегионе было больше детей с сохранной концентрационной функцией почек. В структуре вторичного ПиН в 3 раза реже, чем у детей ПС субрегиона, выявлялся дисметаболический вариант, в 2 раза реже отмечались рецидивы заболевания, была меньшей доля структурных изменений почек, чаще диагностировался первичный ПиН.
В ПВ субрегионе каждый третий ребенок имел острое начало ПиН, чаще выявлялась отягощенность анте-, интранатального анамнеза, среди больных было больше недоношенных, из семей с заболеваниями почек и мочевыводящих путей (45,1%). У каждого второго ребенка отмечался высокий инфекционный индекс, частота сопутствующей патологии составила 2,9 коморбидных состояния. Характерной для этого субрегиона была высокая частота болевого синдрома, протеинурии и бактериурии. Выявление у 64,5% детей в острый период заболевания кристаллурии с преобладанием оксалурии свидетельствовало о выраженной вторичной мембранопатии, тогда как истинный дисметаболический ПиН диагностирован только в 5% случаев. У детей с ПиН этого субрегиона отмечен самый высокий уровень ВПР и МАР почек, а также хронических циститов (17,0%) и энуреза (25,0%). Раннее начало заболевания (в среднем в 2,4 года) и частые рецидивы (2,3 в год) способствовали развитию функциональных нарушений почечных канальцев почти у 40% детей. Для достижения ремиссии детям требовалось более длительное стационарное лечение, однако не все они выписывались домой в состоянии полной ремиссии. Указанные особенности позволяют отнести детей ПВ субрегиона с хроническим ПиН в группу повышенного риска по развитию почечной недостаточности с необходимостью проведения у них более активной нефропротективной терапии, регулярного стационарного лечения и последующей реабилитации в условиях восстановительного центра (отделения) или санатория.
Среди пациентов с ПиН из ПС субрегиона преобладали дети дошкольного возраста с отягощенной наследственностью по заболеваниям почек, патологическим течением анте-, интра-, постнатального периодов. В среднем на 1 ребенка приходилось 3,2 сопутствующих заболевания. Средний возраст начала заболевания был ниже, частота рецидивов – выше, чем у детей из ПКЦ и ПВ субрегионов. В клинической картине чаще выявлялся болевой (46,9%), дизурический (48,6%) и отечный (9,8%) синдромы. Мочевой синдром характеризовался большей частотой гематурии, кристаллурии, нарушением концентрационной функции почек. В то же время по сравнению с соседними субрегионами в генезе вторичного ПиН меньшее значение имели пороки развития почек и МАР, однако чаще выявлялись дисметаболические нарушения. Выявленные особенности анамнеза, клиники, факторов риска рецидивирования и хронизации ПиН в зависимости от эколого-биогеохимических характеристик территории длительного проживания детей являются основой для разработки индивидуальной программы реабилитации с целью длительного поддержания функционального состояния почек и предотвращения развития почечной недостаточности.
При экспертизе качества оказания медицинской помощи детям с ПиН в амбулаторных условиях нами выявлены существенные недостатки при диспансеризации детей с этим заболеванием. У большинства пациентов отсутствовала индивидуальная программа реабилитации, не осуществлялось в полном объеме необходимое лабораторное и инструментальное обследование, у половины - не проводились консультации профильных специалистов, противорецидивная терапия не соответствовала современным стандартам/протоколам, нефропротективная терапия препаратами иАПФ и БРА II назначалась крайне редко. В реабилитации детей не применялись методы восстановительного лечения (физиотерапия, бальнеотерапия, ЛФК и пр.), были недостаточными рекомендации по модификации образа жизни, диетотерапии, питьевому режиму. У детей не оценивалось функциональное состояние почек и не определялись стадии ХБП. В итоге такого формального подхода к диспансерному наблюдению сохранялись частые рецидивы заболевания со снижением почечных функций и ранним развитием ХПН.
Экспертиза качества оказания медицинской помощи детям с ПиН в стационаре показала, что как в соматическом отделении многопрофильной городской больницы, так и в нефрологическом стационаре, имелся целый ряд недостатков в обследовании и лечении пациентов. Среди наиболее значимых замечаний следует отметить неполный объем диагностических исследований, среди которых - отсутствие лабораторных показателей, определяющих активность воспалительного процесса (протеинограмма, С-реативный белок), расчета СКФ, биохимического исследования мочи. У значительного количества пациентов, несмотря на показания, не проводились исследование почечного кровотока, цистография и цистоскопия, экскреторная урография (в городском стационаре), суточное мониторирование АД. Не все дети были осмотрены профильными специалистами, особенно урологом и нефрологом (в городском стационаре), что, в конечном итоге, приводило к недостаточной диагностике сопутствующей патологии и ее неполной коррекции.
Одним из самых больших, на наш взгляд, недостатков является формальный подход к рекомендациям при выписке пациента из стационара и при реабилитации пациента с ПиН, таким образом, не соблюдается принцип преемственности между стационаром, поликлиникой, отделением (центром) восстановительной терапии, врачами-специалистами, врачами дошкольных учреждений и школ, и проводимые на этапе амбулаторного долечивания, а затем - диспансерного наблюдения лечебно-диагностические мероприятия при этом не имеют систематического характера.
Учитывая частое развитие ПиН у детей с обструктивными уропатиями и возможность раннего развития у этой группы пациентов почечной недостаточности, нами проведена экспертиза качества ведения детей с обструктивным ПиН, госпитализированных в урологическое отделение. Полученные результаты свидетельствовали о том, что дети в отделении получали достаточно полный объем необходимых обследований (за исключением уродинамических), оперативную коррекцию пороков, антибактериальную терапию при обострениях микробно-воспалительного процесса. Однако врачами-урологами гораздо меньше внимания уделялось диетотерапии с учетом возраста ребенка и дисметаболических нарушений, медикаментозному лечению, включая нефропротекцию, рекомендациям по дальнейшему восстановительному лечению после выписки из стационара. У детей не учитывались стадии ХБП, не выявлялись симптомы канальцевых нарушений, сопутствующая соматическая патология, нарушения гомеостаза, характерные для начальных стадий ХПН.
Учитывая современные тенденции детской нефрологии, а именно возможность использования расчетной СКФ для оценки функции почек и степени ХБП, доступность инструментального обследования (УЗИ, СМАД), внедрение скрининговых лабораторных методов (определение микроальбуминурии тест-полосками), мы предлагаем включить в протоколы диспансерного наблюдения с хроническим ПиН эти методы исследования, что позволит выявлять прогрессирование почечной патологии на ранних стадиях и применять в амбулаторных условиях современные медикаментозные методы нефропротективной терапии.
При проведении клинико-организационного эксперимента в основную группу вошли 54 ребенка 5-10 лет (17 мальчиков и 37 девочек), страдающие хроническим ПиН и проживающие в сельских районах Чувашии, относящихся к зоне эколого-биогеохимического риска – ПВ региону - цинк-, кремний-, йоддефицитной провинции с высокой техногенной загрязненностью. Группу сравнения составили 42 ребенка (15 мальчиков и 27 девочек) с хроническим ПиН того же возраста и проживающие в том же регионе, в реабилитации которых использовались только медикаментозные средства. Выбор ПВ региона в качестве экспериментального по изучению эффективности восстановительного лечения у детей с ПиН обусловлен особенностями течения заболевания у детей, проживающих в нем, а именно ранним и острым началом, высокой отягощенностью сопутствующей патологией, частыми болевым синдромом, протеинурией и бактериурией, вторичной мембранопатией, самым высоким уровнем ВПР и МАР почек, частыми рецидивами, быстрым развитием функциональных нарушений почечных канальцев. Это заставило отнести пациентов с хроническим ПиН из этого региона к группе повышенного риска по раннему развитию почечной недостаточности и обосновывало применения более активной тактики при их реабилитации.
Сравниваемые группы были сопоставимы по возрасту, полу, факторам риска формирования заболевания, особенностям течения ПиН, функции почек, и преморбидному фону. Эффективность курса реабилитации в условиях детского восстановительного Центра изучена по данным медицинской документации (форма 112/у). Длительность наблюдения в катамнезе составила 1 год с момента окончания лечения.
В восстановительный Центр дети поступали в состоянии полной клинико-лабораторной ремиссии сразу после выписки из стационара или по направлению поликлиник для проведения комплекса реабилитационных мероприятий, направленных на восстановление нарушенных функций ОМС. Длительность курса лечения составила 3 недели. Перед поступлением всем пациентам было выполнено ультразвуковое исследование почек и мочевого пузыря, клинические анализы крови и мочи, проведена санация хронических очагов инфекции и при необходимости - дегельминтизация.
У детей обеих групп (основной и сравнения) хронический ПиН был вторичным. Среди причин вторичного ПиН наиболее часто выявлялись АМС и обструктивные уропатии, реже – ПМР, нейрогенная дисфункция мочевого пузыря и хронический цистит. При изучении анамнеза патология анте-, интранатального и раннего неонатального периодов выявлена у большинства детей, недоношенными родились 9,2 и 7,1, из семей с нефропатиями - 46,3 и 45,2% детей. У детей отмечались сопутствующие заболевания в стадии компенсации, группа часто болеющих детей составила 16,7 и 19,0%.
В восстановительный комплекс входили:
- диетотерапия;
- охранительный режим;
- физиотерапия;
- фитотерапия;
- климатотерапия;
- бальнеотерапия;
- психотерапия.
Особое внимание при составлении дифференцированной программы лечения уделялось немедикаментозным методам терапии.
Оздоровительный комплекс для детей с вторичным хроническим ПиН на фоне гидронефроза 1-2 степени состоял из следующих назначений:
- Диетотерапия – стол №5 по Певзнеру.
- Минеральная вода щелочная, слабой минерализации («Волжские зори-1»), по 5 мл/кг массы 3 раза в день за 20 минут до еды комнатной температуры без газа.
- Фурагин в дозе 2 мг/кг массы однократно на ночь.
- Синусоидальные модулированные токи (СМТ) с помощью аппарата «Амплипульс-5» или ультразвук на пояснично-крестцовую область № 10.
- Хлоридные натриевые ванны №10.
- Альгинатол по 1 свече 3 раза в день ректально 10 дней.
- Магне В6 15 мг/кг в сутки за 2 приема в течение 2 месяцев.
- ЛФК – комплекс упражнений для детей с вторичным хроническим ПиН по методике гидронефротической трансформации почек.
- Психотерапия групповая.
Оздоровительный комплекс для детей с вторичным хроническим ПиН на фоне дистопии почек:
- Диетотерапия – стол №5 по Певзнеру.
- Минеральная вода «Волжские зори-1» по 5 мл/кг массы 3 раза в день за 20 минут до еды комнатной температуры без газа.
- Канефрон в возрастной дозе 3 раза в сутки.
- Дециметровые волны (ДМВ) с помощью аппаратов “Волна-2”, “Волна-2М” в слаботепловой дозе, продолжительность процедуры - 10-15 мин ежедневно, курс лечения - 10 процедур.
- Полисорб МП по 1 г 3 раза в сутки (разведенный в стакана воды) за 1,5 часа до еды 14 дней.
- Цинктерал 0,124 по 1 табл. 1 раз в сутки 14 дней.
- ЛФК – комплекс упражнений для детей с вторичным хроническим ПиН по методике поясничной дистопии почек.
- Психотерапия групповая.
Оздоровительный комплекс для детей с вторичным хроническим ПиН на фоне ПМР 2-3 степени:
- Диетотерапия – стол №5 по Певзнеру.
- Минеральная вода «Волжские зори-1» по 5 мл/кг массы 3 раза в день за 20 минут до еды комнатной температуры без газа на 3 недели.
- Динамические токи на область мочеточников, ритм синкопа в течение 7-10 мин, на курс лечения – 10 процедур.
- Фурагин в дозе 2 мг/кг массы тела однократно на ночь в течение 3 месяцев.
- Элькар 20% раствор по 1 мл 2 раза в сутки в течение 3 месяцев.
- Митамин, капсулы 100 мг янтарной кислоты, по капсулы в сутки, 1-1,5 месяца, 3 раза в неделю.
- Массаж пояснично-крестцовой области по методике для вторичного хронического ПиН №10.
- ЛФК – комплекс упражнений для детей с вторичным хроническим ПиН по методике пузырно-мочеточникового рефлюкса.
- Психотерапия групповая.
Оздоровительный комплекс для детей с вторичным хроническим ПиН на фоне хронического цистита:
- Диетотерапия – стол №5 по Певзнеру.
- Минеральная вода «Волжские зори-1» по 5 мл/кг массы 3 раза в день за 20 минут до еды комнатной температуры без газа на 3 недели.
- Фурагин в дозе 2 мг/кг массы тела однократно на ночь в течение 3 месяцев.
- Пеллоид-терапия (аппликации в виде трусов из озокерита или парафина) – 8-10 процедур.
- Инстилляции мочевого пузыря 0,02% водным раствором хлоргексидина №5, затем - 2,5% раствором колларгола №5 с последующим введением масла шиповника.
- Микроклизмы антисептиков в прямую кишку (теплые отвары эвкалипта или ромашки) одновременно с инстилляциями через день.
- Массаж пояснично-крестцовой области по методике для вторичного хронического ПиН №10.
- ЛФК – комплекс упражнений для детей с вторичным хроническим ПиН по методике пузырно-мочеточникового рефлюкса.
- БОС-терапия.
- Психотерапия групповая.
Оздоровительный комплекс для детей с вторичным хроническим ПиН на фоне нейрогенной дисфункции мочевого пузыря по гипорефлекторному типу.
- Режим принудительного мочеиспускания (через каждые 3 часа).
- Диетотерапия – стол №5 по Певзнеру.
- Минеральная вода «Волжские зори-1» по 5 мл/кг массы 3 раза в день за 20 минут до еды комнатной температуры без газа на 3 недели.
- Фурагин в дозе 2 мг/кг массы тела однократно на ночь в течение 3 месяцев.
- Электрофорез с 0,05% раствором прозерина на низ живота, на курс лечения – 6 процедур.
- Ультразвук на область мочевого пузыря, на курс лечения – 8 процедур.
- Ванны с морской солью, на курс лечения – 10 процедур.
- Экстракт элеутерококка жидкий по 2 капли на год жизни в первой половине дня.
- Пикамилон из расчета 2 мг/кг массы тела в сутки на 1 месяц.
- Массаж пояснично-крестцовой области по методике для вторичного хронического ПиН №10.
- ЛФК – комплекс упражнений для детей с вторичным хроническим ПиН по методике нейрогенной дисфункции мочевого пузыря по гипорефлекторному типу.
- БОС-терапия.
- Психотерапия индивидуальная и групповая.
Оздоровительный комплекс для детей с вторичным хроническим ПиН на фоне нейрогенной дисфункции мочевого пузыря по гиперрефлекторному типу.
- Режим принудительного мочеиспускания (через каждые 3 часа).
- Диетотерапия – стол №5 по Певзнеру.
- Минеральная вода «Волжские зори-1» по 5 мл/кг массы 3 раза в день за 20 минут до еды комнатной температуры без газа на 3 недели.
- Фурагин в дозе 2 мг/кг массы тела однократно на ночь в течение 3 месяцев.
- Настойка пустырника спиртовая по 1 капле на год жизни 3 раза в сутки.
- Дриптан по 5 мг 2 раза в день на 3 недели.
- Пикамилон из расчета 2 мг/кг массы тела в сутки на 1 месяц.
- Электрофорез 0,5% раствора атропина на область мочевого пузыря, на курс лечения - 8 процедур.
- Аппликации парафина или озокерита на пояснично-крестцовую область или магнитотерапия, на курс лечения – 10 процедур.
- Массаж пояснично-крестцовой области по методике для вторичного хронического ПиН №10.
- ЛФК – комплекс упражнений для детей с вторичным хроническим ПиН по методике нейрогенной дисфункции мочевого пузыря по гиперрефлекторному типу.
- БОС-терапия.
- Психотерапия индивидуальная и групповая.
При сочетании хронического ПиН с оксалурией назначалась гипооксалатная диета и высокожидкостный режим (при отсутствии обструктивных нарушений). В лечебные комплексы дополнительно включались витамин В6 из расчета 1 мг/кг в сутки, Канефрон в возрастной дозе, витамин А 3,44% масляный раствор по 1 капле 2 раза в сутки и витамин Е из расчета 2 мг/кг в сутки.
При выписке из восстановительного Центра дети получали подробные рекомендации по дальнейшей реабилитации в амбулаторных условиях с учетом полученного комплекса оздоровительных мероприятий.
Клинико-организационный эксперимент по изучению эффективности реабилитации детей с хроническим ПиН в условиях восстановительного Центра показал большую эффективность комплексного воздействия оздоровительных факторов при этом заболевании (табл. 8). В течение года после курса восстановительной терапии у детей основной группы в 1,8 раза снизилось количество рецидивов ПиН, это привело к меньшей потребности в госпитализациях в профильное отделение, лучшей социализации детей в связи с более редкими пропусками занятий в школе и детском саду. Уменьшение потребности в антибактериальной терапии, визитов в поликлинику косвенно снижало риск рецидивов заболевания и положительно повлияло на почечные функции. Все это обосновывает необходимость более широкого включения методов восстановительного лечения в индивидуальную программу реабилитации детей с ПиН.
Таблица 8
Оценка эффективности восстановительного лечения
у детей с пиелонефритом
| Показатель (из расчета на 1 ребенка) | Основная группа (n = 54) | Группа сравнения (n = 42) |
| Число рецидивов ПиН за год, эпизоды на чел. | 1,3 ± 0,12 | 2,1 ± 0,13* |
| Количество госпитализаций за год, эпизоды на чел. | 0,8 | 1,5* |
| Число дней пропуска занятий в школе и детском саду, дни на чел. | 23,4 | 34,5* |
| Число острых респираторных заболеваний, случаи на чел. | 3,8 | 4,1 |
| Потребность в курсах антибактериальной терапии, на чел. | 2,8 | 4,5* |
| Количество посещений врача, эпизоды на чел. | 15,1 | 18,3 |
| Гипостенурия, абс/% | 1 (1,9) | 2 (4,8) |
| СКФ, мл/мин/1,73 м2 | 96,5 ± 6,83 | 97,6 ± 7,78 |
Достоверность отличия от основной группы * - p < 0,05.
Широкая распространенность нефроуропатий среди детского населения, трудности своевременной диагностики, лечения и реабилитации пациентов с этой патологией, отсутствие эффективных методов профилактики делает особо значимой проблему совершенствования детской специализированной нефрологической службы на региональном уровне. С учетом выявленных тенденций в распространенности нефрологических заболеваний и инвалидности, ВПР, МАР, структуры, стадий, возрастно-полового состава больных с ХБП, недостатков при обследовании, лечении и диспансерном наблюдении пациентов с хроническим ПиН, нами предложено в качестве оптимизации помощи детям с нефропатиями в ЧР создание регионального центра по детской уронефрологии, координирующего деятельность всей уронефрологической службы (рис.6).
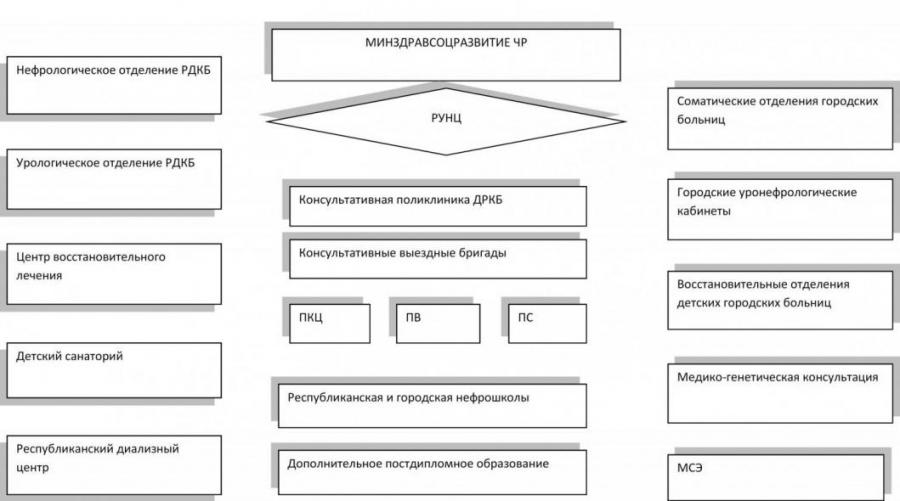
Рис. 6. Структура Республиканского детского уронефрологического центра (РУНЦ)
Основными действующими подразделениями РУНЦ (Республиканский уронефрологический центр) являются:
- консультативная поликлиника РДКБ,
- нефрологическое отделение;
- урологическое отделение;
- хирургическое отделение РДКБ;
- Республиканский восстановительный центр;
- санаторий.
Руководство Центром осуществляет главный детский нефролог МЗ и СР ЧР, деятельность которого основывается на законодательных документах МЗ и СР РФ и ЧР.
В составе консультативной поликлиники работает выездная бригада, укомплектованная следующими специалистами: нефролог, уролог, гинеколог, врач ультразвуковой диагностики, реабилитолог. Бригада создана для оказания консультативной помощи пациентам в сельских районах республики. Она выезжает по установленному графику в районы с учетом превалирующей патологии на основе биогеохимического районирования территории.
Задачами выездной бригады являются:
- консультативная помощь детям с врожденными пороками, выявленными при ультразвуковом скрининге;
- консультативная помощь детям с заболеваниями почек и мочевыводящих путей, не нуждающимся в госпитализации в специализированные учреждения;
- отбор детей на плановую госпитализацию в нефрологическое и урологическое отделения;
- отбор детей на лечение в хирургический стационар одного дня;
- отбор детей на восстановительное лечение в Республиканский восстановительный центр;
- отбор детей на медико-генетическое консультирование;
- контроль эффективности диспансеризации детей с уронефропатиями после оперативного вмешательства на ОМС;
- отбор детей на МСЭ;
- рекомендации по диетической, медикаментозной, физиотерапевтической коррекции при заболеваниях ОМС;
- профилактическая работа по коррекции факторов эколого-биогеохимического риска, характерных для конкретного субрегиона.
Целенаправленная деятельность выездных бригад будет способствовать своевременному выявлению, госпитализации, комплексной реабилитации детей из сельских районов, координации деятельности врачей первичного звена здравоохранения (участковый педиатр, врач общей практики, семейный врач) по оказанию помощи детям с патологией ОМС. Оказание уронефрологической помощи городским детям предусматривается уронефрологическими кабинетами городских поликлиник в тесном взаимодействии с участковыми врачами педиатрами и под руководством РУНЦ.
Итак, результаты комплексного клинико-организационного исследования убедительно доказали влияние эколого-биогеохимических факторов среды постоянного проживания детей на:
- общую заболеваемость;
- распространенность нефрологической патологии;
- структуру госпитализированной заболеваемости;
- популяционную частоту ВПР и МАР почек и их анатомических вариантов;
- факторы риска и клинико-параклинические проявления пиелонефрита.
Региональные особенности нефрологической патологии определяют основные направления оптимизации деятельности специализированной службы по ее лечению и профилактике.
ВЫВОДЫ
1. Уровень общей заболеваемости детей 0-17 лет в Чувашской Республике за 2002-2008 гг. увеличился в 1,7 раза и составил в 2008 г. 2950,4‰. Более высокие темпы его роста отмечались у подростков 15-17 лет. Показатели детской инвалидности в Чувашской Республике соответствуют таковым в РФ, но при этом доля соматической патологии в ее структуре ниже в 2 раза.
Уровень и структура заболеваемости детей, проживающих на территориях гетерогенного эколого-биогеохимического риска, достоверно отличаются. Наиболее высокий уровень общей заболеваемости выявляется у детей Присурского субрегиона - высокоминерализованной, аномальной кремниевой биогеохимической провинции с повышенным содержанием большинства эссенциальных и токсичных элементов в водно-пищевой цепи.
2. Уровень заболеваемости детей 0-17 лет по классу болезней мочеполовой системы вырос в 1,8 раза и достиг в 2008 г. 119,0 на 1000. Доля нефрологической патологии в структуре этого класса болезней составляет 56,1-59,3%. Распространенность и структура уронефрологической заболеваемости у детей ЧР зависит от эколого-биогеохимических особенностей территории проживания и наиболее высока в Прикубнино-Цивильском субрегионе - цинк- и кремний-дефицитной провинции с дисбалансом микроэлементов в пищевой цепи. Более половины (52,1%) госпитализированной заболеваемости занимает инфекция мочевой системы, включая пиелонефрит.
Доля заболеваний органов мочевой системы в структуре соматической инвалидности в ЧР равна 7,6%.
3. Структура хронической болезни почек у детей ЧР представлена преимущественно врожденной патологией, среди которой ведущее место занимают обструктивные уропатии и аномалии мочевой системы (33,1 и 25,8% соответственно). В структуре хронической болезни почек у детей отсутствуют половые различия, половина пациентов имеет возраст до 10 лет, доля детей с хронической почечной недостаточностью составляет 11,1%. Наиболее угрожаемы по развитию хронической почечной недостаточности дети с единственной почкой и обструктивными уропатиями.
4. В Чувашии выявлен высокий уровень распространения врожденных пороков развития и МАР почек (161,3‰). В структуре почечных мальформаций на долю малых аномалий приходится 71,7%, врожденных пороков развития – 21,1%, их сочетаний – 5,6%. Установлена статистически значимая разница в уровне распространения врожденных пороков и малых аномалий развития почек у детей, проживающих в гетерогенных эколого-биогеохимических субрегионах. Наиболее высокие показатели отмечаются в Приволжском субрегионе (187,1‰), низкие – в Присурском (130,4‰), промежуточное место занимал Прикубнино-Цивильский субрегион (164,8‰).
5. У детей с пороками развития почек по сравнению со здоровыми выявлено статистически значимое повышение содержания в волосах алюминия, кадмия, никеля, свинца, олова и снижение – бериллия и цинка (р < 0,05). Для гидронефрозов характерно повышенное содержание хрома и пониженное - магния, аномалии количества почек ассоциированы с высоким содержанием бора и кадмия, аномалии расположения и взаимоотношения – с низким содержанием бериллия.
6. Течение пиелонефрита и факторы риска его возникновения и прогрессирования на гетерогенных эколого-биогеохимических территориях имеют достоверные различия. В Прикубнино-Цивильском субрегионе отмечается более позднее начало заболевания, редкие рецидивы, меньше доля врожденных пороков почек, чаще диагностируется первичный вариант заболевания. Для Приволжского субрегиона характерно острое начало пиелонефрита, отягощенный биологический анамнез, большая частота болевого синдрома и протеинурии, самый высокий уровень почечных мальформаций. В Присурском субрегионе дети начинают болеть в раннем возрасте, имеют частые рецидивы, у них выражены дизурический синдром, дисметаболические нарушения, быстрее снижаются функции почек. Выявленные особенности клиники пиелонефрита у детей в зависимости от эколого-биогехимических характеристик территории проживания являются основой для разработки индивидуальной программы реабилитации.
7. При проведении экспертизы качества диспансеризации детей с пиелонефритом наиболее типичными недостатками являются отсутствие индивидуальной программы реабилитации, неполное лабораторное и инструментальное обследование, нерегулярное противорецидивное лечение, недостаточная восстановительная и нефропротективная терапия. Дефектами ведения детей с пиелонефритом в стационаре являются частичное выполнение стандартов медицинской помощи.
8. Клинико-организационный эксперимент доказал эффективность комплексного лечения детей с хроническим пиелонефритом, проживающих на территории высокого эколого-биогеохимического риска, выражавшуюся в снижении количества обострений (с 2,4 до 1,3 в год), потребности в госпитализациях (в 2 раза) и антибактериальной терапии (на 60%).
9. В основе оптимизации детской уронефрологической службы в ЧР лежит соблюдение принципов преемственности в лечении и диспансеризации детей с патологией органов мочевой системы с учетом эколого-биогеохимических особенностей территории проживания. Создание Республиканского уронефрологического центра позволит в условиях региона с компактным проживанием населения улучшить качество оказания специализированной уронефрологической помощи детям и подросткам.
РЕКОМЕНДАЦИИ ДЛЯ ВНЕДРЕНИЯ В ПРАКТИКУ.
- В целях оптимизации оказания помощи детям с уронефропатиями рекомендуется организация в регионах уронефрологических центров, координирующих и выполняющих лечебно-профилактическую работу с пациентами этого профиля.
- Необходимо проводить многоуровневые экспертизу и мониторинг качества оказания амбулаторно-поликлинической и стационарной помощи детям с уронефропатиями в целях выявления недостатков в ее организации и их своевременного устранения.
- Рекомендуется включить ультразвуковой скрининг почек в программу диспансеризации детей старше 1 года, не обследованных ранее.
- В целях улучшения качества обследования и лечения детей с уронефропатиями рекомендуется ввести в штат профильных урологических отделений врачей- нефрологов, в штат нефрологических отделений – врачей-урологов или организовывать детские уронефрологические отделения.
- При диспансеризации детей с хроническим пиелонефритом необходимо особое внимание уделять динамическому контролю за состоянием почечных функций на основе расчетной скорости клубочковой фильтрации, выделять стадии хронической болезни почек, проводить суточное мониторирование артериального давления, исследовать микроальбуминурию, вести лист контроля биометрических размеров почек.
- В работе врача ультразвуковой диагностики при измерении линейных параметров почек у детей можно использовать объединенную таблицу размеров почек в зависимости от роста или возраста без разделения по полу.
- Данные по распространенности почечных мальформаций, полученные при ультразвуковом скрининге органов мочевой системы у детей, рекомендуется использовать при составлении республиканских регистров врожденных пороков и в практике медико-генетического консультирования.
- Выделять детей с врожденными пороками почек в группу риска по нарушению элементного статуса с последующим обследованием и коррекцией нарушений.
- Учитывать особенности течения пиелонефрита на территориях различного эколого-геохимического риска при разработке индивидуальной программы реабилитации детей.
- Использовать анкету-опросник для выявления патологии органов мочевой системы в работе детских Центров здоровья.
- Включить в тематику циклов усовершенствования и повышения квалификации врачей-педиатров и врачей общей практики разделы по вопросам детской нефрологии и урологии, а именно по ранней диагностике врожденных пороков, определению стадий хронической болезни почек, нефропротективной терапии, комплексной восстановительной терапии при заболеваниях почек.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Иванова И.Е., Газымова Д.М. Аномалии развития почек и мочевыводящих путей у детей и их диагностика // Актуальные вопросы неонатологии. Материалы 3 объединенного съезда детских врачей и акушеров-гинекологов Чувашской Республики. - Чебоксары, 1992. - С. 104-105.
- Иванова И.Е., Зольникова Т.А., Паргунькина Н.А., Бушуева Э.В. Пиелонефриты и пороки мочевыводящей системы у детей раннего возраста // Сб. научных работ «Актуальные проблемы хирургии детского возраста в Чувашской Республике». - Чебоксары, 1994 - С. 73-74.
- Иванова И.Е. Инфекция мочевыводящих путей и пиелонефрит у детей раннего возраста. Учебное пособие // Чебоксары: Изд. ЧГУ, 2000. - 46 с.
- Родионов В.А., Емельянова Н.Н., Бушуева Э.В., Иванова И.Е. Комплексная оценка состояния здоровья сельских школьников чувашей // Детское здравоохранение России: стратегия развития: Материалы 9 съезда педиатров России. - М., 2001. - С. 490.
- Иванова И.Е., Трефилов А.А., Родионов В.А., Козлова М.В. Массовое ультразвуковое исследование почек у детей Чувашской Республики // Материалы III конгресса педиатров-нефрологов России. - СПб, 2003. - С. 112.
- Иванова И.Е., Соснин В.Ю., Трефилов А.А., Родионов В.А. Распространенность и структура пороков развития почек у детей раннего возраста // Материалы 8 Конгресса педиатров России. - М., 2003. - С. 125.
- Иванова И.Е., Родионов В.А., Соснин В.Ю. Семиотика и диагностика заболеваний органов мочевой системы у детей. Методические указания // Чебоксары: Изд. ЧГУ, 2003. - 72 с.
- Родионов В.А., Иванова И.Е. Эффективность вторичной профилактики у детей на территориях эколого-биогеохимического риска // Материалы XI Конгресса детских гастроэнтерологов России. - М., 2004. - С. 55-57.
- Иванова И.Е., Трефилов А.А., Родионов В.А. Распространенность и структура пороков развития почек у детей в Чувашской республике // Вопросы современной педиатрии. - 2004. - Т.3, приложение 1. Материалы IX Конгресса педиатров России. – С. 168.
- Иванова И.Е., Трефилов А.А., Родионов В.А. Малые аномалии развития почек у детей Чувашской республики по данным УЗ-скрининга // Материалы X Конгресса педиатров России. - М., 2004. – С. 246.
- Иванова И.Е., Карягин В.А, Родионов В.А., Скворцова Р.П. Анализ госпитализированной заболеваемости по данным соматического отделения МУЗ «ДГБ №3» // Сб. научных трудов «Актуальные вопросы педиатрии». - Чебоксары, 2004. - С. 30-32.
- Соснин В.Ю., Иванова И.Е., Родионов В.А. К вопросу улучшения диагностики заболеваний почек у детей // Сб. научных трудов «Актуальные вопросы педиатрии». - Чебоксары, 2004. - С. 102-105.
- Соснин В.Ю., Иванова И.Е. Ранняя диагностика заболеваний почек новорожденных и детей раннего возраста // Сб. научных трудов «Актуальные вопросы педиатрии». - Чебоксары, 2004. – С. 105-110.
- Иванова И.Е., Трефилов А.А., Родионов В.А. Региональные стандартные размеры органов брюшной полости и почек у детей при ультразвуковом скрининге // Материалы Всероссийского научного форума «Радиология 2005». - М., 2005. – С. 460.
- Иванова И.Е., Родионов В.А., Трефилов А.А. Регионарные нормативы органов мочевой системы у детей по данным ультразвукового скрининга // Сборник материалов X Конгресса педиатров России «Актуальные проблемы педиатрии». - М., 2006. – С. 583.
- Трефилов А.А, Иванова И.Е., Родионов В.А. Эколого-биохимические аспекты распространенности врожденных пороков развития почек у детей по данным массового ультразвукового скрининга // Сборник тезисов V Съезда Российской Ассоциации специалистов Ультразвуковой диагностики в медицине. – М., 2007. – С. 213.
- Дворяковский И.В., Скутина Л.Е. Дворяковская Г.М., Иванова И.Е. Морфофункциональные показатели здорового ребенка: пособие для врачей // М.: Научный центр здоровья детей, 2007. – 51 с.
- Дворяковский И.В., Скутина Л.Е. Дворяковская Г.М., Иванова И.Е. Ультразвуковая диагностика нефросклероза у детей с обструктивными уропатиями: пособие для врачей // М.: Научный центр здоровья детей, 2007. - 24 с.
- Трефилов А.А., Иванова И.Е., Родионов В.А. Патологическая подвижность почек у детей по данным ультразвукового скрининга // Материалы VI Российского Конгресса «Современные технологии в педиатрии и детской хирургии». - М., 2007. - С. 160.
- Трефилов А.А., Иванова И.Е., Родионов В.А. Пиелоэктазия у детей и подростков по данным ультразвукового скрининга // Материалы VI Российского Конгресса «Современные технологии в педиатрии и детской хирургии». - М., 2007. – С. 411.
- Трефилов А.А., Иванова И.Е., Родионов В.А. Малые аномалии развития почек у детей в различных биогеохимических зонах по данным массового ультразвукового скрининга // Вопросы современной педиатрии. – 2007. - Т.6, №2. – С. 146-147.
- Трефилов А.А., Иванова И.Е., Родионов В.А. Нормативы почек у детей в уронефрологической практике по результатам массового ультразвукового обследования // Неврологический вестник. Журнал имени В.М. Бехтерева. Т. XXXIX, выпуск 3. Материалы IV региональной научно-практической конференции «Педиатрия и детская хирургия в Приволжском федеральном округе». - Казань, 2007. - С. 181.
- Иванова И.Е., Трефилов А.А. Особенности элементного статуса у детей с пороками почек // Сб. материалов к 5 Региональной научно-практической конференции «Педиатрия и детская хирургия в Приволжском Федеральном округе». - Казань, 2008. - С. 48-49.
- Иванова И.Е. Элементный статус детей и пороки развития почек // Вестник восстановительной медицины. – 2008. - №5а (28). – С. 30-33.
- Иванова И.Е., Грабеклис А.Р. Анализ зависимости элементного состава волос детей и наличия аномалий развития почек // Микроэлементы в медицине. - 2008. - Т.9, вып. 12. – С. 53.
- Иванова И.Е., Скальный А.В., Родионов В.А. Роль дефицита цинка и избыточного накопления металлов-поллютантов у детей с аномалиями развития почек // Микроэлементы в медицине. - 2008, Т.9, вып. 3-4. - С. 31-36.
- Иванова И.Е., Семенова Л.В. Нефрологическая заболеваемость у детей Чувашской Республики // Материалы 16 съезда педиатров России. – М., 2009. - С. 235.
- Иванова И.Е.. Трефилов А.А., Русанова Н.И. Анализ элементного состава волос детей с аномалиями развития почек // Материалы 16 съезда педиатров России. – М., 2009. – С. 236.
- Иванова И.Е., Трефилов А.А. Анализ элементного статуса детей с аномалиями развития почек // Вопросы клинической и экспериментальной медицины. – Чебоксары, 2009. - С. 91-95.
- Иванова И.Е., Трефилов А.А., Родионов В.А., Семенова Л.В. Ultrasonic screening of kidneys at infants: the first results // East and West, Nost and South: Balansed Paediatric Care in Europe: 4-th Europaediatrics (3-6 July 2009, Moscow). – Moscow, 2009. – Р. 236.
- Лукоянов Д.В., Иванова И.Е. Применение заместительной почечной терапии при органных дисфункциях у детей // Здравоохранение Чувашии. – 2009. - №4. - С. 19-23.
- Иванова И.Е., Трефилов А.А. Первые итоги ультразвукового скрининга почек у новорожденных детей в рамках национального проекта «Здоровье» // Сборник материалов к VI Региональной научно-практической конференции «Педиатрия и детская хирургия в Приволжском федеральном округе». - Казань, 2009. – С. 39.
- Иванова И.Е., Семенова Л.В. Место уронефрологической патологии в структуре хронической болезни почек (ХБП) у детей Чувашской Республики // Сборник материалов к VI Региональной научно-практической конференции «Педиатрия и детская хирургия в Приволжском федеральном округе». - Казань, 2009. - С. 39-40.
- Иванова И.Е. Актуальные вопросы нефрологической заболеваемости у детей Чувашской Республики // Материалы межрегиональной научно-практической конференции «Современные аспекты организации медицинской помощи населению». – Чебоксары, 2009. – С. 229-235.
- Иванова И.Е., Скальный А.В., Родионов В.А. Элементный статус детей с аномалиями развития почек // Микроэлементы в медицине. - 2009. – №1-2, Т. 10. - С. 47-52
- Иванова И.Е. Заболеваемость детей Чувашской Республики в современных условиях // Материалы 14 Конгресса педиатров. – М., 2010. – С. 310.
- Иванова И.Е. Нефрологическая инвалидность у детей Чувашской Республики // Материалы 14 Конгресса педиатров. – М., 2010. – С. 311.
- Иванова И.Е., Семенова Л.В. Инвалидность детей в Чувашии, обусловленная заболеваниями органов мочевой системы // Девятый Российский Конгресс «Инновационные технологии в педиатрии и детской хирургии». - М., 2010. - С. 15.
- Иванова И.Е., Макарова Т.А., Семенова Л.В. Структура хронической болезни почек у детей Чувашской Республики // Девятый Российский Конгресс «Инновационные технологии в педиатрии и детской хирургии». - М., 2010. - С. 226-227.
- Иванова И.Е., Семенова Л.В., Родионов В.А., Макарова Т.А. Региональные особенности патологии органов мочевой системы у детей Чувашской Республики // Девятый Российский Конгресс «Инновационные технологии в педиатрии и детской хирургии». - М., 2010. - С. 227-228.
- Иванова И.Е. Хроническая болезнь почек как педиатрическая проблема (лекция) // Сб. научных трудов «Актуальные вопросы педиатрии». – Чебоксары, 2010. – С. 78-88.
- Иванова И.Е. Особенности течения пиелонефрита у детей в различных эколого-биогеохимических регионах Чувашии // Сб. научных трудов «Актуальные вопросы педиатрии». – Чебоксары, 2010. – С. 88-95.
- Карягин В.А., Иванова И.Е. Волкова З.В., Варикова К.С. Детское соматическое отделение городской больницы – ведущее звено в оказании стационарной помощи детскому населению города // Сб. научных трудов «Актуальные вопросы педиатрии». – Чебоксары, 2010. – С. 117-124.
- Трефилов А.А., Пигаваева А.Н., Иванова И.Е. Результаты ультразвукового скрининга детей первых месяцев жизни в рамках национального проекта «Здоровье» // Сб. научных трудов «Актуальные вопросы педиатрии». – Чебоксары, 2010. – С. 207-215.
- Иванова И.Е. Нефрологическая заболеваемость у детей Чувашской Республики // Российский педиатрический журнал. – 2010. - №3. – С. 44-48.
- Иванова И.Е., Семенова Л.В., Егорова И.Н. Болезни органов мочевой системы как одна из причин формирования инвалидности у детей в Чувашской Республике // Общественное здоровье и здравоохранение. – 2010. - №3. - С. 26-31.
- Иванова И.Е. Заболеваемость детей и подростков Чувашской Республики в начале XXI века // Российский педиатрический журнал. – 2010. - №4. - С. 37-43.
- Иванова И.Е., Родионов В.А., Трефилов А.А., Лаврентьева И.Н. Региональные особенности хронической болезни почек у детей Чувашии // Вестник Чувашского университета. Естественные и технические науки. - 2010. - №3. - С. 109-114.
- Трефилов А.А., Иванова И.Е. Результаты ультразвукового скрининга почек у детей в рамках национального проекта «Здоровье» // Вестник Чувашского университета. Естественные и технические науки. – 2010. - №3. - С. 162-165.
- Иванова И.Е., Скальный А.В., Родионов В.А., Трефилов А.А. Эколого-биогеохимические аспекты элементного статуса и распространенности врожденных пороков почек у детей // Технологии живых систем. – 2010. - №6. - С. 14-18.
- Иванова И.Е., Родионов В.А. Оптимизация восстановительного лечения детей с пиелонефритом // Вестник восстановительной медицины. – 2010. - №5. - С. 62-64.
- Иванова И.Е., В.А. Родионов. Заболеваемость детей и подростков в различных эколого-биогеохимических регионах Чувашии // Общественное здоровье и здравоохранение. – 2010. - №4. – С. 20-24.
- Иванова И.Е., Лаврентьева И.Н. Оценка эффективности диспансеризации детей с хроническим пиелонефритом на педиатрическом участке // Медицинский альманах. – 2010. – Т. 13, №4. – С. 214-218.
- Иванова И.Е.. Трефилов А.А., Ладыкова О.В., Петрова А.А. Ультразвуковое исследование почек у детей при проведении плановой диспансеризации // Материалы к 7 Российской конференции «Педиатрия и детская хирургия в Приволжском федеральном округе». - Практическая медицина. - 2010. - № 7. - С. 60.
- Иванова И.Е. Патология почек у детей на территориях эколого-биогеохимического риска (по материалам Чувашской Республики). – Монография. - Чебоксары, 2010. – 190 с.
- Иванова И.Е. Экспертиза качества диспансеризации детей с хроническим пиелонефритом // Актуальные проблемы гуманитарных и естественных наук. - 2010. - №5. - С. 244-249.
- Иванова И.Е. Расстройства мочеиспускания у детей (нейрогенный мочевой пузырь, энурез): практические рекомендации // Чебоксары: ГОУ ДПО ИУВ, 2010. – 78 с.
- Иванова И.Е. Восстановительное лечение при пиелонефрите у детей: учебно-методическое пособие // Чебоксары: ГОУ ДПО ИУВ, 2010. - 85 с.
- Ivanova I.E., Skalny A.V., Lakarova E.V., Eisazadeh S. Elemental status of children with renal malformations // Материалы IV Международного симпозиума Федерации европейских обществ по изучению макро-микроэлементов «Макро- и микроэлементы в медицине и биологии». - Микроэлементы в медицине. – 2010. - №2. - С. 35.
- Иванова И.Е. Республиканский уронефрологический центр как наиболее эффективная структура оказания специализированной помощи детям с патологией органов мочевой системы // Материалы юбилейной конференции, посвященной 25-летию ГУЗ «РДКБ» Минздравсоцравития Чувашии «Республиканская клиническая больница и ее роль в оказании высокоспециализированной помощи детскому населению». - Чебоксары, 2010. – С. 197-207.
- Иванова И.Е., Макарова Т.А., Трефилов А.А., Карягин А.В. Патология органов мочевой системы у детей Чувашской Республики на современном этапе // Материалы юбилейной конференции, посвященной 25-летию ГУЗ «РДКБ» Минздравсоцравития Чувашии «Республиканская клиническая больница и ее роль в оказании высокоспециализированной помощи детскому населению». - Чебоксары, 2010. – С. 211-225.
- Иванова И.Е., Трефилов А.А., Родионов В.А. Нормативы размеров почек у здоровых детей Чувашской Республики по данным ультразвуковой диагностики. - Ультразвуковая и функциональная диагностика. – 2010. - № 6. – С. 50-55.
- Иванова И.Е., И.Н. Сергеева, Скальный А.В. Нарушения обмена макро- и микроэлементов и особенности нефрологической заболеваемости у детей с пороками почек // Вопросы биологической, медицинской и фармацевтической химии. - 2011.- №1. – С. 56-63.
- Иванова И.Е., Трефилов А.А., Русанова Н.И., Скворцова А.Г. Результаты ультразвукового скрининга почек при диспансеризации детей 9-10 лет // Сб. материалов XV Конгресса педиатров России с международным участием «Актуальные проблемы педиатрии». – М., 2011. – С. 327.
- Иванова И.Е. Хроническая болезнь почек у детей Чувашской Республики // Сб. материалов XV Конгресса педиатров России с международным участием «Актуальные проблемы педиатрии». – М., 2011. – С. 328.
- Иванова И.Е., Трефилов А.А., Родионов А.А. Эколого-биогеохимические аспекты распространенности вариантов развития почек у детей // Ультразвуковая и функциональная диагностика. – 2011. - № 1. – С. 25-32.
Список сокращений.
АД – артериальное давление
АМС – аномалия мочевой системы
ВПР – врожденный порок развития
ЗПТ - заместительная почечная терапия
ИМС – инфекция мочевой системы
МАР – малая аномалия развития
МПС – мочеполовая система
ОМС – органы мочевой системы
ПКЦ – Прикубнино-Цивильский
ПВ – Приволжский
ПС – Присурский
ПиН – пиелонефрит
ПФО – Приволжский федеральный округ
ПМР – пузырно-мочеточниковый рефлюкс
РФ – Российская Федерация
СКФ – скорость клубочковой фильтрации
ТИН – тубулоинтерстициальный нефрит
ХБП – хроническая болезнь почек
ХПН – хроническая почечная недостаточность
ЧЛС – чашечно-лоханочная система
ЧР – Чувашская Республика

