Химико-фармакологическое исследование урологического сбора
На правах рукописи
Лукша Елена Александровна
ХИМИКО-ФАРМАКОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ УРОЛОГИЧЕСКОГО СБОРА
15.00.02 – фармацевтическая химия, фармакогнозия
Автореферат
диссертации на соискание ученой степени
кандидата фармацевтических наук
Томск – 2006
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Сибирский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Научный руководитель:
доктор фармацевтических наук, профессор Калинкина Галина Ильинична
Официальные оппоненты:
доктор биологических наук, профессор Замощина Татьяна Алексеевна
кандидат фармацевтических наук, доцент Нурмухаметова Карлыгаш Абековна
Ведущая организация:
ГОУ ВПО Иркутский государственный медицинский университет Росздрава
Защита состоится 22 декабря 2006 г. в 1000 часов на заседании диссертационного совета Д 208.096.04 при ГОУ ВПО СибГМУ Росздрава
634050, г. Томск, Московский тракт, 2
С диссертацией можно ознакомиться в научно-медицинской библиотеке
ГОУ ВПО СибГМУ
634050, г. Томск, пр. Ленина, 107
Автореферат разослан « » ноября 2006 г.
Ученый секретарь
диссертационного совета Е. В. Ермилова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Современная фармакотерапия урологических заболеваний включает широкий спектр лекарственных препаратов различных фармакологических групп. Лечение больных с воспалительными заболеваниями почек и мочевыводящих путей представляет собой одну из наиболее сложных проблем современной урологии. Необходимость длительного применения лекарственных средств при консервативном лечении неспецифических воспалительных заболеваний мочеполовой системы позволяет отдать предпочтение препаратам растительного происхождения.
Особенности этиологии, патофизиологического механизма и симптоматических проявлений воспалительного процесса в почках, диктуют необходимость поиска новых фитосредств с поливалентным терапевтическим воздействием на основные звенья патологического процесса. Поставленная задача успешно решается применением многокомпонентных растительных композиций или сборов.
В перечне урологических фитопрепаратов, разрешенных к медицинскому применению в Российской Федерации, доля растительных сборов незначительна – менее 2%. Кроме того, анализ лекарственных растительных средств, используемых в урологической практике, показывает, что в основном в их составе содержатся компоненты, обладающие выраженным диуретическим действием и в незначительной степени влияющие на другие звенья патогенеза. Это диктует необходимость в разработке нового средства, проявляющего мягкий диуретический эффект в сочетании с антимикробным и противоспалительным действием.
Цель исследования. Целью диссертационной работы явилось теоретическое и экспериментальное обоснование разработки и стандартизации многокомпонентного урологического сбора, обладающего антимикробным, противовоспалительным и умеренным диуретическим действием.
Для реализации поставленной цели необходимо было решить следующие задачи:
- Провести анализ проблемы урологической патологии и лекарственных растительных средств, используемых при неспецифических воспалительных заболеваниях МП для обоснования направления поиска нового фитосредства.
- Составить и обосновать пропись урологического сбора на основе официнальных и перспективных для медицинской практики видов лекарственного растительного сырья.
- Провести оценку диуретических, антимикробных и противовоспалительных свойств предложенной прописи сбора.
- Провести исследование химического состава сбора для обоснования его стандартизации. Разработать методики определения подлинности и качества лекарственного урологического сбора.
- Разработать проект фармакопейной статьи предприятия (ФСП) на предлагаемый растительный урологический сбор.
Научная новизна работы. На основании анализа банка данных литературы и собственных фармакологических исследований разработана пропись лекарственного растительного сбора «Урофит» (листья березы, трава горца птичьего, побеги курильского чая, корни лопуха, плоды рябины обыкновенной, плоды рябины черноплодной, трава хвоща полевого, побеги черники), обладающего комплексным действием на основные звенья патогенеза неспецифических урологических заболеваний. Установлено, что водный экстракт сбора обладает выраженным антимикробным и противовоспалительным действием и проявляет умеренный диуретический эффект. Новизна предлагаемого фитосредства защищена приоритетной справкой на изобретение «Лекарственное средство, обладающее комплексным диуретическим, противомикробным и противовоспалительным действием – сбор Урофит» (№ 2006 122 786 (024727) от 26.06.2006 г).
Установлен качественный и количественный состав основных биологически активных веществ (БАВ) сбора: дубильные вещества, флавоноиды, фенолокислоты, кумарины, полисахариды, аскорбиновая кислота, витамин К, каротиноиды, сапонины, соединения кремния, микроэлементы. Методами хроматографии на бумаге, в тонком слое сорбента и ВЭЖХ в составе сбора идентифицированы: арбутин, хлорогеновая кислота, кофейная, п-кумаровая, феруловая кислоты, кумарин, кверцетин, рутин, кверцитрин, апигенин, гиперозид, авикулярин, кемферол, лютеолин, 6-метокси-7-О--D- глюкопиранозилкумарин.
Обоснована стандартизация сбора по содержанию флавоноидов. Разработаны методики качественного обнаружения и количественного определения флавоноидов в сборе «Урофит» методами хроматографии в тонком слое сорбента и спектрофотометрии, которые включены в проект ФСП.
Для идентификации сбора «Урофит» предложены внешние и микроскопические диагностические признаки входящих в него ингредиентов. С учетом многокомпонентности сбора разработан «Определитель компонентов сбора Урофит по микроскопическим признакам», включенный в проект ФСП.
Практическая значимость работы. Теоретические и экспериментальные исследования показали целесообразность дальнейшего фармакологического исследования предложенного сбора «Урофит» в качестве нового урологического средства.
Разработан проект ФСП «Сбор урологический Урофит».
Предложенный состав урологического сбора и методики его стандартизации использованы ООО «Биолит» для разработки и производства гранулированной БАД к пище «Уролизин» (Акты внедрения от 02.02.2005 г).
Разработано учебное пособие «Проблема урологических заболеваний и основные направления их решения с помощью фитотерапии», которое используется в учебном процессе кафедры фармакогнозии Иркутского государственного медицинского университета, кафедры фармакогнозии с курсом ботаники Алтайского государственного медицинского университета, кафедры фармакогнозии с курсами ботаники и экологии Сибирского государственного медицинского университета, Центрами фарминформации.
На защиту выносятся следующие положения и результаты:
Разработан состав нового урологического сбора, обладающего противовоспалительным, антимикробным и умеренным диуретическим действием. Стандартизацию сбора необходимо проводить по содержанию флавоноидов и экстрактивных веществ, извлекаемых водой.
Апробация работы. Основные положения диссертационной работы доложены на Всероссийской научно-практической конференции «Современные проблемы фармакологии и фармации» (г. Новосибирск, 2005); 63-ей международной студенческой научной конференции им. Н.И. Пирогова (г. Томск, 2004), на заседании проблемной комиссии «Изыскание и изучение новых лекарственных средств. Вопросы фармации» (Томск, 2006), а также на заседаниях кафедры фармакогнозии с курсами ботаники и экологии СибГМУ (г. Томск, 2004 – 2006 ).
Связь задач исследования с проблемным планом фармацевтических наук. Работа выполнена в соответствии с планом научных исследований кафедры фармакогнозии с курсами ботаники и экологии Сибирского государственного медицинского университета и комплексной целевой программой СО АМН Российской Федерации «Здоровье человека в Сибири» (№ Государственной регистрации 01.9.2002479).
Публикации. По материалам диссертации опубликовано 7 статей и тезисов докладов, из них 1 статья журнальная, 1 учебное пособие. Получена приоритетная справка на изобретение «Лекарственное средство, обладающее комплексным диуретическим, противомикробным и противовоспалительным действием». Приоритетная справка № 2006 122 786 (024727) от 26.06.2006 г.
Экспериментальные исследования по теме диссертации выполнены на кафедре фармакогнозии с курсами ботаники и экологии, на кафедре фармакологии СибГМУ (г.Томск), в Центральной научно-исследовательской лаборатории (ЦНИЛ СибГМУ), на кафедре фармакологии Алтайского государственного медицинского университета (г.Барнаул), в Новосибирском институте органической химии СО РАН. Сотрудникам данных подразделений выражаем глубокую благодарность.
Структура и объем диссертации. Диссертация изложена на страницах машинописного текста и состоит из введения, обзора литературы, четырех глав экспериментальных исследований, выводов, списка литературы и приложения. Работа иллюстрирована 27 таблицами и 77 рисунками. Библиографический указатель включает 149 источников литературы, из них 22 зарубежных.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Объекты и методики исследования
Объектом исследования являлись образцы пяти сборов, содержащих лекарственные растения, разрешенные для применения в медицинской практике или используемые в народной медицине для лечения урологических заболеваний. Лекарственное растительное сырье собирали в различные фазы вегетации в соответствии с требованиями нормативной документации.
Приготовление сборов отбор проб для анализа, изучение характеристик подлинности и показателей качества осуществляли, руководствуясь общими статьями ГФ XI издания.
При разработке и оформлении проекта ФСП на сбор руководствовались ОСТ 91500.05.001-00 «Стандарты качества ЛС. Основные положения».
Для фармакологических исследований использовали отвары, водные и водно-спиртовые экстракты, а также этилацетатную и бутанольную фракции, полученные в результате последовательного разделения сгущенного водного извлечения сбора методом избирательной жидкостной экстракции. Из жидких экстрактов и фракций удаляли растворитель, получали сухие остатки, которые представляли собой порошки бурого цвета, растворимые в воде.
Для качественного и количественного определения БАВ сбора использовали методы и приемы фитохимического анализа: хроматографические (ВЭЖХ, хроматография в тонком слое сорбента, на бумаге, колоночная), методы избирательной экстракции различными растворителями, спектральный анализ, спектрофотоскопические, хроматоспектрофотометрические, титриметрические, гравиметрические методы.
Для идентификации компонентов в сборе использовали макро- и микроскопические методы анализа. Морфологические признаки компонентов сбора изучали и описывали под стереоскопическим микроскопом МБС-10 (увеличения 8х1; 8х2; 8х4) по известным методикам.
Микроскопические признаки компонентов сбора устанавливали на основании анатомического исследования частей растений, входящих в состав сбора, для чего были приготовлены плоскостные препараты. Сухое сырье предварительно разваривали в 2,5 % растворе натрия гидроксида, в растворе хлоралгидрата. Для получения объективных результатов анализировали не менее десяти препаратов. Готовые препараты изучали под микроскопом МИКМЕД-1 (увеличения 7х1,5х8; 7х1,5х40). Объекты фиксировали цифровым фотоаппаратом «LG» с помощью фотонасадки МФН-3. Снимки обрабатывали на компьютере в программе «Photoshop 7.0».
Антибактериальное действие извлечений из сбора оценивали in vitro по степени чувствительности к ним микроорганизмов, являющихся причиной возникновения большинства урологических инфекционных заболеваний. Антибактериальную активность изучали методами дисков и серийных разведений в жидкой питательной среде.
Антигрибковые свойства экстрактов сбора исследовали in vitro методом двукратных серийных разведений в жидкой питательной среде Сабуро по методике Вичкановой С.А.
Противовоспалительное действие сбора изучали на модели острой воспалительной реакции, вызванной введением 0,05 мл 1% раствора агара под плантарный апоневроз правой задней лапки. Об интенсивности воспаления судили по массе отека. Эксперимент проводили на беспородных мышах-самцах массой 18-24 г.
Исследование действия экстрактов на функцию почек проведено на беспородных белых крысах-самцах массой 200-300 г. Всех животных содержали в соответствии с правилами Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и научных целей.
Статистическую обработку полученных результатов проводили путем расчета средней (М) и средней квадратичной ошибки (). О достоверности различий судили, используя параметрический (t-критерий Стьюдента) и непараметрический (Т-критерий Манна-Уитни) методы. Значимость различий считали достоверной при Pt, Pu<0,05. Расчеты проводили с использованием программ STATISTICA 6.0 и SPSS 12.0.
Теоретическое и экспериментальное обоснование компонентного состава сбора
При создании урологического сбора руководствовались следующими критериями: подбор компонентов в соответствии с известными особенностями патофизиологии урологических инфекционно-воспалительных заболеваний; доступность компонентов, как в плане сырьевой базы, так и в экономическом отношении; технологичность производства на современном оборудовании; хорошие потребительские свойства.
На основании анализа данных литературы и с учетом вышеперечисленных критериев в качестве перспективных для составления сборов нами было отобрано сырье 12 видов растений, произрастающих в Сибири: трава горца птичьего, листья березы, плоды рябины обыкновенной, плоды рябины черноплодной, трава череды трехраздельной, трава зверобоя, трава хвоща полевого, корни лопуха, побеги черники обыкновенной, трава тысячелистника, побеги курильского чая, листья крапивы. Все растения применяются в официнальной и народной медицине для лечения заболеваний почек и МВП.
С учетом фармакологических свойств вышеперечисленных растений были составлены пять прописей сборов, состоящих из шести-восьми компонентов, взятых в равных весовых соотношениях.Так как терапия инфекционно-воспалительных заболеваний не требует достижения форсированного диуреза, нами была поставлена цель: на основании фармакологического скрининга выявить пропись рецептуры сбора, проявляющего «мягкое» диуретическое действие в сочетании с антимикробным и противовоспалительным эффектом. Для оценки антибактериального действия в качестве тест-культуры использовали стандартный штамм Escherichia coli. Действие сборов сравнивали с официнальным фитосредством «Сбор урологический (мочегонный)» (ВФС 42-2717-96)
Результаты исследования, представленные в таблице 1, показали, что перспективным для дальнейшего изучения является сбор по прописи № 3, который сопоставим по величине диуретического эффекта с официнальным сбором урологическим (мочегонным) и проявляет более выраженный антимикробный эффект. В состав сбора включены 8 видов сырья: листья березы, трава горца птичьего, побеги курильского чая, корни лопуха, плоды рябины обыкновенной, плоды рябины черноплодной, трава хвоща полевого и побеги черники.
Таблица 1
Оценка антимикробного и диуретического эффекта водных отваров сборов
| Исследуемый препарат | Диуретический эффект по отношению: | Антимикробный эффект (диаметр задержки роста культуры E. Coli, мм) | |
| к интактным животным, % | Отношению к препарату сравнения, % | ||
| Сбор урологический официнальный (препарат сравнения) | 257 | 100 | 25 |
| Пропись сбора № 1: листья березы, трава горца птичьего, трава хвоща полевого, корни лопуха, трава тысячелистника, трава череды | 144 | 56 | 12 |
| Пропись сбора № 2: листья березы, трава горца птичьего, трава хвоща полевого, корни лопуха, трава зверобоя, побеги черники, листья крапивы | 211 | 82 | 9 |
| Пропись сбора № 3: листья березы, трава горца птичьего, трава хвоща полевого, корни лопуха, плоды рябины обыкновенной, плоды рябины черноплодной, побеги курильского чая, побеги черники | 250 | 97 | 32 |
| Пропись сбора № 4: листья березы, трава горца птичьего, трава хвоща полевого, корни лопуха, плоды рябины черноплодной, трава тысячелистника, побеги курильского чая, трава зверобоя | 126 | 49 | 20 |
| Пропись сбора № 5: листья березы, трава горца птичьего, трава хвоща полевого, корни лопуха, плоды рябины обыкновенной, плоды рябины черноплодной, трава тысячелистника, трава череды. | 189 | 74 | 18 |
Кроме того, анализ данных литературы о химическом составе растений, входящих в состав прописи сбора № 3 позволили обосновать рациональность применения каждого компонента в составе урологического сбора, названного нами «Урофит».
Для оценки фармакологических свойств комплекса БАВ сбора и возможного выявления группы действующих веществ, проявляющих специфическую активность, нами была проведена серия исследований по антимикробному, противовоспалительному действию, изучено влияние на выделительную функцию почек у крыс водного, водно-спиртового экстрактов, сбора «Урофит», а также их этилацетатной и бутанольной фракций.
Оценка фармакологических свойств сбора «Урофит»
Острая токсичность. Оценка острой токсичности водного экстракта сбора проведена по общепринятой методике. Все исследованные экстракты в дозах 500-2000 мг/кг не вызывали гибели животных в течение 2 недель наблюдения. Согласно существующей классификации (ГОСТ 12.1.007-76), они соответствуют IV классу «Вещества малоопасные».
Влияние однократного введения извлечений сбора на функцию почек у крыс. В экспериментах на крысах в условиях однократного введения изученные экстракты вызвали снижение диуреза на 6-20 % в основном за счет снижения скорости клубочковой фильтрации. Также наблюдалось снижения уровня калия и натрия в моче. Данные факты не позволяют сделать каких-либо выводов о характере влияния извлечений сбора на функцию почек у экспериментальных животных, так как для препаратов растительного происхождения только длительное введение дает более объективную и достоверную информацию.
Влияние длительного введения извлечений сбора на функцию почек у крыс. Длительное введение экстрактов не оказало токсического влияния на животных. На это указывает зарегистрированный прирост массы тела крыс с 220,0±13,1 до 230,0±13,4 г. Результаты влияния экстрактов и их фракций на функцию почек крыс суммированы в таблицах 2, 3, 4 и 5.
Длительное введение показало постепенное нарастание показателей диуреза после снижения в результате однократного введения исследуемых извлечений. Максимальный уровень диуреза был зарегистрирован к 5-му дню при введении водного экстракта, и к 9-му дню при введении вводно-спиртового экстракта. Этилацетатная фракция показала наименьший уровень диуретической активности на протяжении всего времени введения. Все препараты вызывали задержку натрия в течение первых трех дней введения. Экскреция натрия возрастала к 5-7 дню при введении водного, водно-спиртового экстрактов и бутанольной фракции. Этилацетатная фракция вызывала более длительную задержку натрия, и показатели экскреции возрастали только к концу эксперимента. Водное извлечение не оказывало калийуретического эффекта. Бутанольная фракция показала снижение уровня калия в моче на 25%. Введение спиртового экстракта и этилацетатной фракции показало увеличение экскреции калия на 4% и 20% соответственно, что рассматривается как нежелательный эффект и показывает преимущество использования водного извлечения сбора.
Исследование противовоспалительной активности извлечений сбора.
Введение мышам 1% раствора агара приводило к развитию острого воспаления; прирост массы отека при этом составлял 65,5% (рис. 1). Введение животным индометацина (препарат сравнения) снижало прирост массы отека на 28% по сравнению с животными контрольной группы. Все исследуемые экстракты и их фракции препятствовали развитию острой воспалительной реакции у животных, уменьшая прирост массы отека. Наименьший прирост массы отека был зафиксирован при профилактическом введении спиртового экстракта и этилацетатной фракции (22,62 и 25,38 % соответственно). Необходимо отметить, что ни одно извлечение не превысило показателя противовоспалительной активности препарата сравнения.
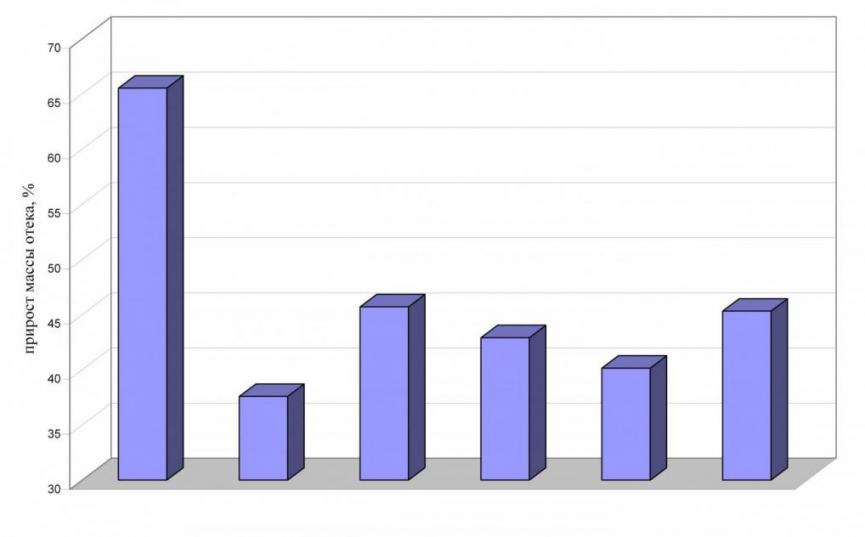
Рис. 1 – Влияние экстрактов сбора на развитие реакции острого воспаления
Исследование антибактериальной активности экстрактов сбора показало наличие антибактериального эффекта в отношении грамположительных и грамотрицательных микроорганизмов. Как видно из таблицы 6, водный экстракт проявляет более выраженный эффект по сравнению с водно-спиртовым.
Таблица 6
Антибактериальная активность экстрактов сбора (мкг/мл)
| Экстракты | Тест-микроорганизмы | |||
| грамотрицательные | грамположительные | |||
| Ps. aeruginosa | Proteus vulgaris | E. coli | Staph. aureus | |
| Водный | 15,6 | 31,25 | 15,6 | 15,6 |
| Спиртовый | 31,25 | 62,5 | 15,6 | 31,25 |
Таким образом, оценка фармакологической активности в экспериментах in vitro и на животных позволяет сделать вывод о наличии у исследуемого сбора противовоспалительного, антимикробного и диуретического эффекта. Следует отметить, что в результате проведенных исследований не была выявлена наиболее активная фракция, проявляющая одновременно все исследуемые эффекты. Данный факт экспериментально подтверждает предположение о комплексном воздействии всех БАВ компонентов сбора. Результаты оценки фармакологической активности также позволяют обосновать рациональность включения компонентов в состав сбора в равных массовых соотношениях.
Таблица 2
Влияние 11-дневного введения экстрактов сбора и их фракций на диурез у крыс (мл/сут)
(M±m), n=10, где M – среднее значение, m – доверительный интервал, n – количество измерений
| Экстракт | До введения | Дни введения | Через 2 дня после введения | |||||
| 1 | 3 | 5 | 7 | 9 | 11 | |||
| Водный | 9,00±0,57 | 8,40±0,45 | 9,78±0,39 | 11,00±1,50* | 11,60±2,28 | 10,70±3,07* | 9,50±1,50 | 8,90±1,72 |
| В.-спиртовый | 10,50±0,52 | 8,30±0,91 | 9,00±0,52 | 9,50±0,95 | 9,70±1,13 | 9.90±1,19 | 9,80±1,76 | 11,70±1,04* |
| ЭАФ водного | 7,70±0,71 | 5,75±0,46 | 6,87±0,25 | 7,34±0,51 | 7,80±0,51 | 7,95±0,48 | 7,53±0,30 | 7,50±0,68 |
| БФ водного | 8,5±0,61 | 6,40±0,80 | 7,10±0,57* | 8,69±0,81 | 8,70±0,91 | 8,60±1,2* | 8,70±0,60 | 8,90±0,86 |
Примечание *- здесь и далее звездочками отмечены достоверные отличия по сравнению с исходными показателями
Таблица 3
Влияние 11-дневного введения экстрактов сбора и их фракций на экскрецию креатинина у крыс (мкМ/сут)
(M±m), n=10, где M – среднее значение, m – доверительный интервал, n – количество измерений
| Экстракт | До введения | Дни введения | Через 2 дня после введения | |||||
| 1 | 3 | 5 | 7 | 9 | 11 | |||
| Водный | 38,00±4,4 | 38,00±6,50 | 37,56±1,90 | 37,00±7,40* | 44,00±6,00 | 43,00±7,40 | 44,00±7,10 | 36,00±6,30 |
| В.-спиртовый | 32,15±1,66 | 30,58±1,11 | 32,54±2,66 | 34,46±2,74 | 32,56±1,91 | 33,25±0,91 | 31,17±1,55 | 33,14±1,66 |
| ЭАФ | 24,14±1,61 | 24,00±1,11 | 23,12±1,19 | 23,57±1,14 | 19,59±1,10 | 18,12±2,11 | 18,40±1,6 | 22,19±1,12 |
| БФ | 23,18±2,10 | 18,70±2,01 | 21,37±0,98 | 20,94±1,80 | 21,52±1,50 | 22,56±1,92 | 23,46±1,55 | 24,11±1,41 |
Таблица 4
Влияние 11-дневного введения экстрактов сбора и их фракций на экскрецию натрия у крыс (мкМ/сут)
(M±m), n=10, где M – среднее значение, m – доверительный интервал, n – количество измерений
| Экстракт | До введения | Дни введения | Через 2 дня после введения | |||||
| 1 | 3 | 5 | 7 | 9 | 11 | |||
| Водный | 68,58±7,8 | 53,16±2,60 | 62,35±4,71 | 69,10±6,50 | 71,12±6,00* | 70,12±8,00 | 68,45±10,90* | 66,15±8,20 |
| В.-спиртовый | 59,21±2,26 | 56,13±2,31 | 56,97±3,14 | 59,84±2,35 | 59,97±2,31 | 59,89±3,29 | 57,98±3,24 | 58,98±3,38 |
| ЭАФ | 54,18±2,32 | 47,70±2,19 | 48,11±2,15 | 48,94±3,14* | 49,50±3,22 | 47,80±2,13 | 54,68±3,18 | 45,78±2,23 |
| БФ' | 35,48±1,12 | 32,77±2,16* | 44,36±2,87 | 49,72±2,22 | 45,92±2,28 | 41,60±2,19 | 42,67±4,31* | 33,11±3,27* |
Таблица 5
Влияние 11-дневного введения экстрактов сбора и их фракций на экскрецию калия у крыс (мкМ/сут)
(M±m), n=10, где M – среднее значение, m – доверительный интервал, n – количество измерений
| Экстракт | До введения | Дни введения | Через 2 дня после введения | |||||
| 1 | 3 | 5 | 7 | 9 | 11 | |||
| Водный | 231,00±21,5 | 225,67±45,1* | 235,22±35,12 | 238,00±130,10* | 233,00±141,8* | 227,0±191,0 | 224,00±134,0 | 229,00±133,7* |
| В.-спиртовый | 340,45±32,10 | 330,00±25,10 | 334,87±26,28 | 336,12±24,80 | 337,12±34,12 | 345,12±23,11 | 344,54±22,40 | 341,28±79,89 |
| ЭАФ | 249,12±21,45 | 314,29±25,44 | 299,78±38,57 | 274,95±36,12* | 367,90±58,14 | 243,19±87,50 | 226,73±98,55* | 236,22±99,23* |
| БФ | 381,80±87,56 | 203,77±79,96 | 267,22±41,37 | 289,11±99,12* | 253,88±99,87 | 239,40±99,00 | 286,88±55,23 | 331,07±74,12 |
Исследование химического состава сбора «Урофит»
Данные, представленные в таблице 7, показывают, что в составе сбора содержатся: фенольные соединения, сапонины, полисахариды, витамины, макро- и микроэлементы. Учитывая значительную роль фенольных соединений в проявлении антимикробных, противовоспалительных и диуретических свойств фитопрепаратов, предпринято более детальное изучение веществ этой группы.
Таблица 7
Результаты анализа химического состава урологического сбора.
(М ± m), n=5; M- среднее значение, m– доверительный интервал, n–количество определений)
| Наименование БАВ | Содержание в абс. сухой массе сырья, % |
| 1 | 2 |
| Фенольные соединения Сумма фенольных соединений в том числе: Дубильные вещества Арбутин Флавоноиды Антоцианы Фенолокислоты Кумарины | 6,60±0,22 1,10±0,06 0,21±0,01 0,80 ±0,03 0,07±0,01 0,34±0,04 0,27±0,01 |
| Сапонины | 0,22±0,01 |
| Полисахариды Водорастворимые полисахариды Пектиновые вещества Гемицеллюлоза А Гемицеллюлоза В | 6,70±0,17 1,10±0,07 4,42±0,40 6,58±0,32 |
| Витамины Аскорбиновая кислота Каротиноиды Витамин К | 0,56±0,02 2,34±0,11 мг% 0,10±0,00 |
| Макро- и микроэлементы Соединения кремния | 5,71±0,32 2,37±0,11 |
Хроматографическое исследование фенольных соединений
При хроматографическом исследовании фенольных соединений методами БХ, ТСХ в составе сбора идентифицированы флавоноиды, фенолокислоты, кумарины, фенологликозиды (табл. 8).
Таблица 8
Результаты идентификации фенольнольных соединений сбора «Урофит»
| Название вещества | Окраска в УФ-свете | Величина Rf** | |
| До проявления | После проявления* | ||
| 1 | 2 | 3 | 4 |
| Арбутин (гидрохинон-О--D-глюкопиранозид) | Бледно-фиолетовая | Коричневая (диазотированая сульфаниловая к-та) | 0,85 I 0,90 VI 0,89 V |
| Хлорогеновая кислота (5-О-кофеил-D-хинная) | голубая | Зеленая (пары аммиака) | 0,62 I 0,44 III 0,66 VII |
| Кофейная кислота (3,4-диоксикоричная) | голубая | Усиление окраски (пары аммиака) | 0,82 I 0,26 III 0,78 VII |
| п-кумаровая кислота | фиолетовая | Синяя (пары аммиака) | 0,90 I 0,76 III 0,30 VII |
| Феруловая (4-окси-3-метоксикоричная) | Фиолетово-голубая | Фиолетовая (пары аммиака) | 0,84 I 0,71 III 0,30 VII |
| Кумарин (бензо--пирон) | - | Зеленоватая (этанольный р-р NaOH) | 0,89 I |
| Кверцетин (3,5,7,3,4-пентаоксифлавонол) | желтая | Желто-бурая (AlCl3) | 0,68 I 0,12 IV |
| Рутин (кверцетин-3-О--D-глюкопиранозидо-(16)-О--D-рамнопиранозид) | бурая | Темный желто-зеленый (AlCl3) | 0,48 I 0,54 IV |
| Гиперозид (кверцетин-3-О--D-галактопиранозид) | желто-бурая | Темно-желтая (AlCl3) | 0,57 I 0,38 IV |
| Авикулярин (кверцетин-3-О--D-арабинозид) | бурая | Темно-желтая (AlCl3) | 0,70 I 0,32 IV |
| Кемпферол (3,5,7,4-тетраоксифлавонол) | желто-зеленая | Усиление окраски(AlCl3) | 0,85 I 0,55 II |
| Апигенин (5,7,4'-триоксифлавон) | бурая | Зелено-желтый (AlCl3) | 0,92 I 0,83 II 0,05 IV |
| Лютеолин (5,7,3',4'-тетрагидроксифлавон) | Темно-коричневая | Желто-зеленый (AlCl3) | 0,85 I 0,10 IV |
Примечание: * - В скобках указаны реактивы для проявления хроматограмм.
** - Цифрами обозначены системы растворителей для хроматографирования:
I – н-бутанол-кислота уксусная-вода (4:2:1) – БХ; II – кислота уксусная- кислота хлороводородная конц.-вода (5:1:5) – БХ; III – 2 % раствор кислоты уксусной – БХ; IV – 15 % раствор кислоты уксусной – БХ; V – 60 % раствор кислоты уксусной ТСХ; VI – этилацетат-кислота муравьиная-вода (3:1:1) – БХ; VII - н-бутанол-25%-кислота уксусная (1:1) – БХ.
Для уточнения полученных результатов использовали метод высокоэффективной жидкостной хромато-масс-спектрометрии. Для этого водно-спиртовый экстракт сбора фракционировали по общепринятой схеме на хлороформную, этилацетатную и бутанольную фракции. Анализу подвергали этилацетатную и бутанольную фракции, так как сравнительное хроматографическое исследование показало присутствие значительного числа соединений фенольной природы именно в этих фракциях.
Для идентификации использовали достоверные образцы фенолокислот, кумаринов и флавоноидов. Основными критериями при выборе предполагаемой структуры являлись: время удерживания исследуемых веществ в сравнении с известными образцами, УФ-спектры и масс-спектры веществ, а также базы данных и обзорные статьи, содержащие сведения о спектральных и физико-химических характеристиках природных соединений.
Полученные хроматограммы УФ-детектирования при длине волны 280 и 340 нм имели различный вид и различное число пиков (рисунки 2, 3, 4, 5). Многокомпонентность изучаемого сбора обусловила наличие большого количества пиков (свыше 30).
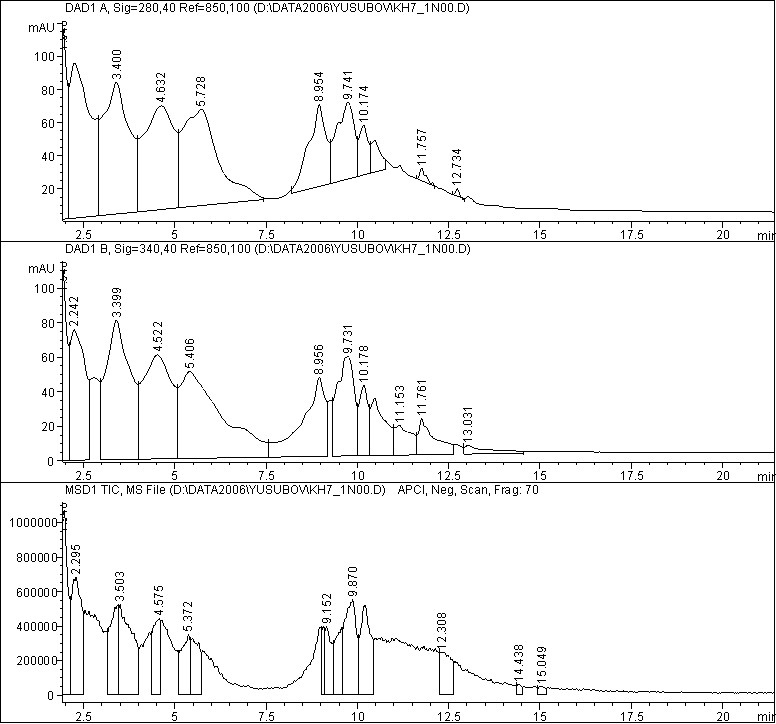
Рис.2. – Хроматограмма этилацетатной фракции в режиме УФ-детектирования при длине волны 280 нм.

Рис. 3. – Хроматограмма этилацетатной фракции в режиме УФ-детектирования при длине волны 340 нм.
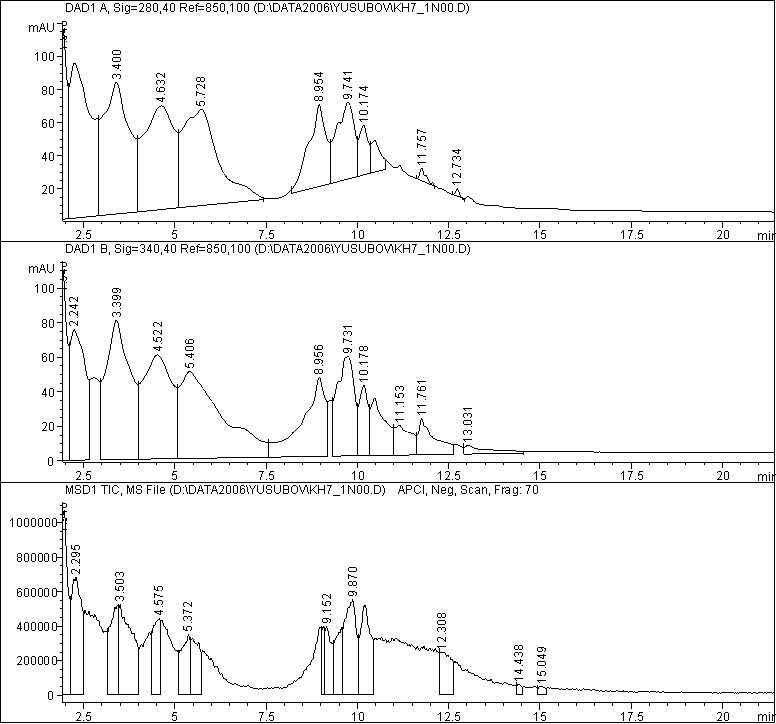
Рис. 4 – Хроматограмма этилацетатной фракции с масс-селективным детектором в режиме APCI, Neg. Scan.
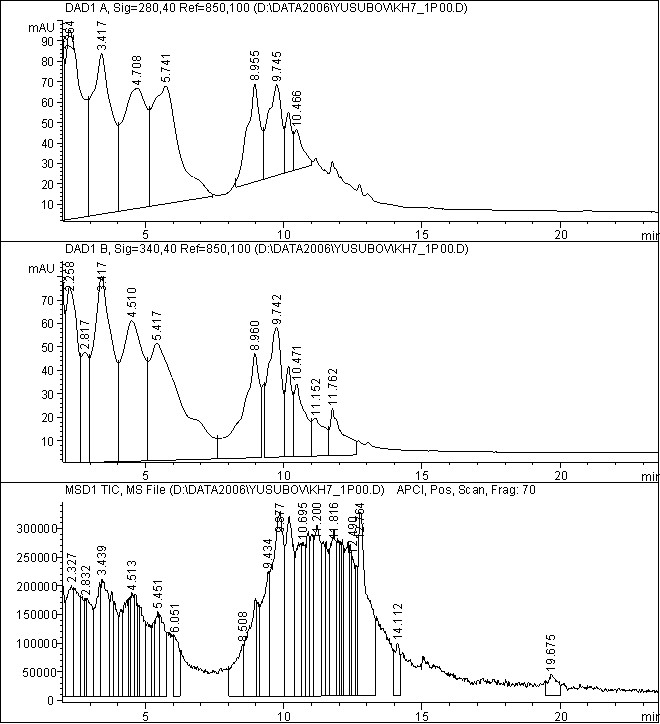
Рис. 5 – Хроматограмма этилацетатной фракции сбора с масс-селективным детектором в режиме APCI, Pos. Scan.
Наиболее информативной является хроматограмма масс-селективного детектирования в двух режимах (APCI positive scan. и APCI negative scan.) При регистрации положительных ионов в режиме химической ионизации (ХИ) при атмосферном давлении (APCI) обычно фиксируется псевдомолекулярный ион - [М+Н]+ (APCI, Pos. Scan.). В этом случае для вычисления молекулярной массы необходимо сделать поправку на «-1» от максимального значения m/z (из интенсивных пиков). При регистрации отрицательных ионов а режиме ХИ при атмосферном давлении (APCI) фиксируются депротонированные молекулы. В этом случае на масс-спектрах режима APCI, Neg. Scan. для вычисления молекулярной массы вещества необходимо сделать поправку на «+1» к максимальному значению m/z (из интенсивных пиков).
На хроматограмме этилацетатной фракции пик со временем удерживания 1,67 мин имеет УФ-спектр с тремя основными максимумами поглощения: 248, 298 и 324 нм (рис. 6). Предположительно мы идентифицировали это вещество как производное кумарина. В режиме ХИ APCI, Pos. Scan. (рис. 7) в масс-спектре присутствует пик с m/z=355,1 (50 %), а в режиме ХИ APCI, Neg. Scan с m/z=353,1 (100 %) (рис. 8), что отвечает пикам молекулярного иона+протон [М+Н]+ и [М-Н]+ соответственно.
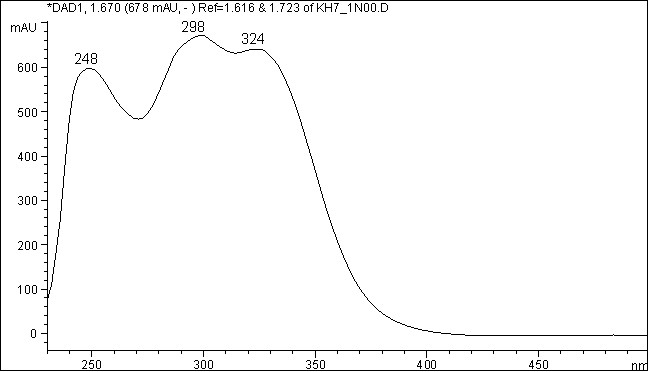
Рис. 6 – УФ-спектр веществ со временем удерживания 1,67 мин
Пик фрагмента молекулярного иона m/z 163,1 (100 %) в режиме ХИ APCI, Pos. Scan. доказывает гликозидную природу вещества, а пик фрагмента молекулярного иона m/z 191,1 (18 %) в режиме ХИ APCI, Neg. Scan. подтверждает наличие агликонового остатка (рисунки 7, 8). Таким образом, предполагаемое вещество можно отнести к 6-метокси-7-О--D-глюкопиранозилкумарину
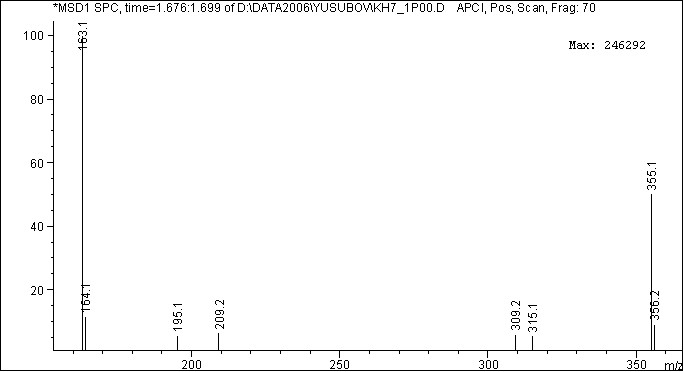
Рис. 7 – Масс-спектр фрагментов молекулярного иона 6-метокси-7-O--D-глюкопиранозилкумарина в режиме ХИ APCI, Pos. Scan.
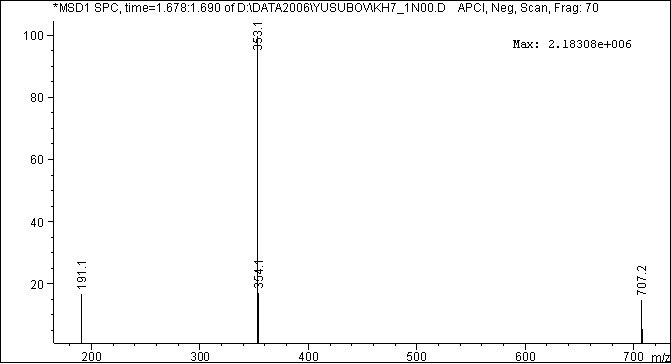
![]()
Рис. 8 – Масс-спектр фрагментов молекулярного иона 6-метокси-7-O--
D-глюкопиранозилкумарина в режиме ХИ APCI, Neg. Scan.
Таким образом, опираясь на УФ- и масс-спектры, снятые в двух режимах химической ионизации, получена информация, позволяющая подтвердить качественный состав БАВ сбора. Результаты представлены в таблице 9.
Таблица 9
Результаты идентификации биологически активных веществ
| Время удерживания | Величина m/z (молекулярная масса) | Вещество |
| 1,67 | 354 | 6-метокси-7-О--D- глюкопиранозилкумарин |
| 4,6 | 464 | Гиперозид (кверцетин-3-О--D-галактопиранозид) |
| 5,7 | 434 | Авикулярин (кверцетин-3-О--D-арабинозид) |
| 6,2 | 448 | Кверцитрин (кверцетин-3-О--L-рамнопиранозид) |
| 9,3 | 302 | Кверцетин (7,5,3,3,4 - тетраоксифлавон) |
| 10,2 | 446 | О-гликозид лютеолина |
сбора «Урофит» методом ВЭЖХ-МС
Обобщая результаты исследования химического состава урологического сбора (табл.8, 9), следует отметить, что доминирующим компонентом БАВ сбора являются соединения фенольной природы, среди которых идентифицированы: арбутин, хлорогеновая, кофейная, п-кумаровая, феруловая кислоты, кумарин, кверцетин, рутин, кверцитрин, апигенин, гиперозид, авикулярин, лютеолин, кемферол, гликозид 6-метоксикумарина. Анализ состава сбора показывает, что фенольный комплекс представлен, в основном, флавоноидами, среди которых доминируют гликозиды флавонола кверцетина. В связи с этим стандартизацию сбора рационально проводить по сумме флавоноидов в пересчете на кверцетин.
Разработка методик стандартизации сбора «Урофит»
Разработка характеристик подлинности сбора. Важнейшими характеристиками подлинности сбора являются внешние признаки и микроскопия.
Изучение внешних признаков сбора проводили в 2 этапа: вначале осматривали невооруженным глазом, отмечая общую структуру растительной смеси, цвет, запах и вкус водного извлечения, затем сбор изучали под стереомикроскопом, выделяя все составляющие каждого компонента и детально их характеризуя.
При исследовании сбора под стереомикроскопом все компоненты, принадлежащие к разным морфологическим группам, идентифицировались без затруднений. Два вида побегов, плодов и травы дифференцировались по специфическим морфологическим признакам.
Микроскопические признаки сбора «Урофит» установлены на основании анатомического исследования листьев березы, травы горца птичьего, побегов курильского чая, плодов рябины обыкновенной, плодов рябины черноплодной, побегов черники, травы хвоща полевого. При анализе все диагностические анатомические признаки компонентов сбора визуализировались, как правило, в совокупности и соответствовали описанию, приведенному в статьях нормативной документации.
Принимая во внимание сложность состава сбора, нами был разработан определитель, с помощью которого можно поэтапно дифференцировать компоненты вначале на группы, а затем выделить составляющие каждого компонента и диагностировать его по микроскопическим признакам. Работа с определителем при диагностике компонентов сбора «Урофит» нам представляется более объективной и экспрессной, чем работа с простым перечнем диагностически значимых микроскопических признаков. Следовательно, целесообразно включить «Определитель компонентов сбора «Урофит» по микроскопическим признакам» в нормативную документацию.
Для определения подлинности сбора наряду с «Внешними признаками» и «Микроскопией» нормативная документация должна содержать описание методик качественного обнаружения действующих веществ. Для разработки данной характеристики подлинности нами были использованы результаты хроматографического исследования суммы фенольных соединений сбора, которые позволили обосновать проведение стандартизации по флавоноидам. Наиболее целесообразным является использование метода хроматографии в тонком слое сорбента на пластинках «Сорбфил». Анализу подвергали гидролизат сбора, полученный для проведения количественного определения суммы флавоноидов в сборе. Хроматографию проводили в системе хлороформ-этанол (1:3) в присутствии стандартного образца кверцетина. Проявление хроматограммы осуществляли в УФ-свете при длине волны 365 нм.
Разработка методики количественного определения флавоноидов в сборе. Спектральное исследование в ультрафиолетовой области водно-этанольного извлечения сбора не выявило наличия выраженных пиков, характерных для каких-либо индивидуальных веществ флавоноидной природы. Прибавление к извлечению спиртового раствора алюминия хлорида в качестве комплексообразующей добавки также не дало информативных результатов. Данные факты можно объяснить многокомпонентностью состава сбора и, в результате этого, одновременным присутствием большого числа веществ, в том числе и флавоноидов, индивидуальные концентрации которых не позволяют выявить доминирующий компонент в суммарном извлечении методами спектрофотоскопии.
Следовательно, необходимо ввести этап пробоподготовки извлечения, позволяющий выделить сумму флавоноидов и провести их количественное определение в пересчете на доминирующий компонент. Ранее проведенный химический анализ выявил присутствие флавонола кверцетина и его гликозидов в составе БАВ сбора. В связи с этим, проведение кислотного гидролиза суммарного извлечения сбора, в результате которого возрастет концентрация агликона кверцетина, представляется наиболее рациональной стадией пробоподготовки. Дальнейшие исследования показали, что целесообразно провести избирательную экстракцию агликонов этилацетатом из гидролизата сбора с целью устранения влияния на результаты измерения сопутствующих веществ.
При разработке методики анализа отрабатывали степень измельчения сырья, условия экстракции и гидролиза, в качестве экстрагента использовали этанол различной концентрации. Оптимальными параметрами методики являются: измельченность сбора – 2 мм; экстрагент – 70%-ый этанол, подкисленный хлороводородной кислотой до показателя рН 2-3; соотношение сырья и экстрагента 1:30; водяная баня (70-80°С); время экстракции и гидролиза – 60 минут; однократная экстракция; соотношении извлечения и раствора алюминия хлорида 1:2; время экспозиции 30 мин.
Содержание суммы флавоноидов в пересчете на кверцетин колебалась от 0,8 до 1,10 %. В проект ФСП предлагаем внести показатель содержания флавоноидов в пересчете на кверцетин не менее 0,8 %.
Результаты статистической обработки полученных данных показали, что методика отличается хорошей воспроизводимостью, относительная ошибка определения при доверительной вероятности 95% не превышает 5%.
Кроме содержания действующих веществ показателями качества сбора являются влажность, содержание золы и примесей, пределы которых установлены экспериментально.
ВЫВОДЫ:
- На основании анализа банка данных литературы и собственных исследований предложена пропись нового урологического сбора «Урофит», для которого установлена диуретическая, противовоспалительная и антимикробная активность сбора «Урофит».
- В составе сбора «Урофит» определено содержание: фенольных соединений–6,60±0,22 %, из них флавоноидов–0,80±0,03% (кверцетин, рутин, кверцитрин, апигенин, гиперозид, авикулярин, лютеолин, апигенин, кемпферол), антоцианов–0,07±0,00% фенолокислот – 0,34±0,04 % (хлорогеновая, феруловая, кофейная кислоты), дубильных веществ – 1,10±0,06 %, кумаринов 0,27±0,01; сапонинов – 0,22±0,01; полисахаридов: водорастворимых полисахаридов – 6,70±0,17 %, пектиновых веществ – 1,10±0,07 %, гемицеллюлозы А – 4,42±0,40 %, гемицеллюлозы В – 6,58±0,32 %; аскорбиновой кислоты – 0,56±0,02 %; каротиноидов 2,34±0,11 мг %, витамин К 0,10±0,01 %, соединения кремния – 2,37±0,01 %.
- Элементный состав сбора «Урофит» представлен 30 макро- и микроэлементами, из которых в наибольших количествах содержатся (%): кальций (0,37), железо (0,041), цинк (6,0710-4), кобальт (0,4110-4), и селен (0,2310-4 ).
- Стандартизацию сбора предложено проводить по содержанию флавоноидов и экстрактивных веществ, извлекаемых водой. Разработаны методики качественного обнаружения методом ТСХ и количественного определения флавоноидов методом спектрофотометрии в присутствии раствора алюминия хлорида в пересчете на кверцетин.
- Разработаны показатели определения доброкачественности сбора «Урофит», включенные в проект ФСП: содержание флавоноидов в пересчете на кверцетин не менее 0,8%, количество экстрактивных веществ, извлекаемых водой не менее 25 %; показатели влажности, зольности и примесей.
- Для идентификации сбора «Урофит» предложены внешние и микроскопические диагностические признаки, входящих в него ингредиентов.
- Разработан определитель микроскопических признаков компонентов сбора, включенный в проект ФСП.
- На основании выполненных исследований разработан проект фармакопейной статьи предприятия «Урофит (урологический) сбор)».
СПИСОК ОПУБЛИКОВАННЫХ РАБОТ
ПО ТЕМЕ ДИССЕРТАЦИИ
1. Разработка состава и методики стандартизации урологического сбора // Сб. статей по материалам Всероссийской 63-й итоговой научной конференции им. Н. И. Пирогова. - Томск, 19-20 апреля 2004. – С. 254-255.
2. Проблема рационального использования экологически чистого ЛРС // Труды постоянно действующей научно-технической школы-семинара студентов, аспирантов и молодых ученых «Информационные системы мониторинга окружающей среды». – Томск, 2004. – Выпуск 3. – С. 51-53 (Соавт. Г. И. Калинкина, Н. Э. Коломиец, И. А. Туева, А. С. Ангаскиева, Е. Н. Сальникова, И. М. Смолякова, Л. П. Охрименко).
3. Разработка и стандартизация урологического сбора. // Сб. статей по материалам Всероссийской научно-практической конференции «Современные проблемы фармакологии и фармации». – Новосибирск, 2005. – С. 433-435 (соавт. Г. И. Калинкина, В. Н. Буркова).
4. Сравнительное фитохимическое исследование некоторых видов рода Polygonum // Материалы II Всероссийской научно-практической «Новые достижения в химии и химической технологии растительного сырья». – Барнаул, 2005. – С. 348-349 (Соавт. Г. И. Калинкина, В. Н. Буркова, В. В. Панов).
5. Изучение биоэлементного состава Polygonum calcatum Lindm. // Материалы Всероссийской научно-практической конференции, посвященной 100-летию со дня рождения профессора Л.Н. Березнеговской. – Томск, 2006. – С. 221-222 (Соавт. Г. И. Калинкина, В. Н. Буркова, Л. В. Куликова).
6. Антимикробные свойства экстрактов арбутинсодержащих растений // Материалы Всероссийской научно-практической конференции, посвященной 100-летию со дня рождения профессора Л.Н. Березнеговской. – Томск, 2006. – С. 272-277.
7. Фармакологические свойства нового урологического растительного сбора // Бюллетень Сибирской медицины. – Том 5, 2006. Приложение 2.- С.109-110. (Соавт. Г. И. Калинкина)
8. Проблема урологических заболеваний и основные направления их решения с помощью фитотерапии // Учебное пособие – Томск, 2006. – 30 с. (Соавт. Калинкина Г. И., Коломиец Н. Э., Полуэктова Т. В.)
СПИСОК СОКРАЩЕНИЙ
БАВ – биологически активные вещества;
БФ – бутанольная фракция;
ВФС – временная фармакопейная статья;
ВЭЖХ – высокоэффективная жидкостная хроматография;
ГСО – государственный стандартный образец;
МВП – мочевыводящие пути;
МП – мочеполовая система;
УФ – ультрафиолетовый;
ФСП – фармакопейная статья предприятия;
ХИ – химическая ионизация;
ЭАФ – этилацетатная фракция;

